名校
解题方法
1 . LiFePO4、LiPF6、LiAsF6、LiCl等常用于锂离子聚合物电池。请回答:
(1)PO 的立体构型是
的立体构型是_____ ,Fe2+的价层电子轨道表示式是_____ 。
(2)题干中所给四种物质所含的非金属元素中,电负性最大的是_____ ,基态原子第一电离能最小的是_____ 。
(3)抗坏血酸( )常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是
)常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是_____ 。
(4)电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。

①从化学键角度看,Li+迁移过程发生_____ (填“物理”或“化学”)变化。
②相同条件,Li+在_____ (选填“LiPF6”或“LiAsF6”)中迁移较快。
③图乙中X的杂化方式最可能是_____ (填字母编号)。
a.sp3 b.sp3d c.sp3d2 d.sp3d3
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl•3H2O属于正交晶系(长方体形),晶胞参数为0.75nm、1.0nm、0.56nm,如图1为沿z轴投影的晶胞中所有氯原子的分布图和原子分数坐标。

图1
①据此推断该晶胞中氯原子数目为_____ 。
②图中A、B两原子核间距离为_____ nm(只列计算式)。
(6)铜和锌同周期且相邻,现有几种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10,失去1个电子需要的能量由大到小排序是_____ (填字母)。
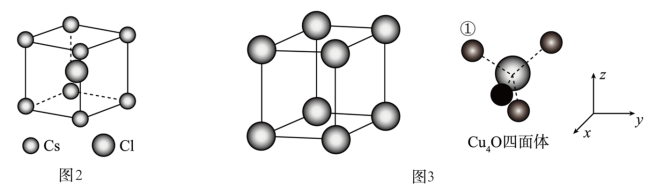
(7)Cu2O晶体结构与CsCl(图2)相似,只是利用Cu4O占据CsCl晶体中Cl的位置,而Cs位置由O原子占据,如图3所示,每个Cu2O晶胞中有_____ 个“Cu2O”;Cu2O晶胞中Cu的配位数是_____ ;若①处Cu原子坐标为( ,
, ,
, ),则Cu2O晶胞中Cu4O四面体中O原子坐标为
),则Cu2O晶胞中Cu4O四面体中O原子坐标为_____ 。
(1)PO
 的立体构型是
的立体构型是(2)题干中所给四种物质所含的非金属元素中,电负性最大的是
(3)抗坏血酸(
 )常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是
)常被用作碳包覆的碳源,以增强电极导电性,其易溶于水的原因是(4)电池工作时,Li+沿聚乙二醇分子中的碳氧链迁移的过程如图甲所示(图中阴离子未画出)。电解质LiPF6或LiAsF6的阴离子结构如图乙所示(X=P、As)。

①从化学键角度看,Li+迁移过程发生
②相同条件,Li+在
③图乙中X的杂化方式最可能是
a.sp3 b.sp3d c.sp3d2 d.sp3d3
(5)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。LiCl•3H2O属于正交晶系(长方体形),晶胞参数为0.75nm、1.0nm、0.56nm,如图1为沿z轴投影的晶胞中所有氯原子的分布图和原子分数坐标。

图1
①据此推断该晶胞中氯原子数目为
②图中A、B两原子核间距离为
(6)铜和锌同周期且相邻,现有几种铜、锌元素的相应状态,①锌:[Ar]3d104s2、②锌:[Ar]3d104s1、③铜:[Ar]3d104s1、④铜:[Ar]3d10,失去1个电子需要的能量由大到小排序是
| A.④②①③ | B.④②③① | C.①②④③ | D.①④③② |
 ,
, ,
, ),则Cu2O晶胞中Cu4O四面体中O原子坐标为
),则Cu2O晶胞中Cu4O四面体中O原子坐标为
您最近一年使用:0次
解题方法
2 . 过渡金属在生产、生活、科技等方面有着广泛的应用。例如仿生簇化合物Mn4XO4(X=Ca2+/Y3+/Gd3+)有望为实现利用太阳能和水获取清洁能源(氢能)开辟新途径,MnOx·Na2WO4·SiO2、钴(Co)的合金及其化合物材料等广泛应用于化工催化剂等领域。
请回答下列问题:
(1)基态钇(39Y)的价层电子排布式为_______ 。
(2)基态Co原子核外有_______ 种运动状态不同的电子,其3d能级上有_______ 对成对电子。
(3)[Co(NO2)6]3-中三种元素的第一电离能由大到小的顺序是_______ (填元素符号)。已知:[Co(CN)6]4-是强还原剂,与水反应能生成[Co(CN)6]3-。[Co(CN)6]4-中含有σ键与π键的数目之比为_______ ,[Co(CN)6]3-中C的杂化方式为_______ 。
(4)[Mn(NH3)2]2+中配体分子的立体构型是_______ 。[Mn(NH3)2]2+中键角∠HNH_______ (填“大于” 、“小于”或“等于”)NH3中键角∠HNH。
(5)MnF2、MnCl2晶体的熔点分别为856 °C、650 °C,二者熔点存在明显差异的主要原因是_______ 。
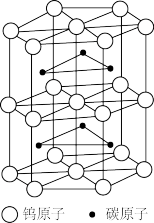
(6)碳化钨是一种由钨(W)和碳组成的晶体,其晶体结构如图所示,晶体的熔点为2870° C,硬度与金刚石相当。碳化钨的晶体类型是_______ ;已知:碳化钨晶体的密度为ρg·cm-3,NA为阿伏加德罗常数的值,六棱柱高为a cm,则底边长为_______ (用含ρ、a、N的表达式表示)nm。
请回答下列问题:
(1)基态钇(39Y)的价层电子排布式为
(2)基态Co原子核外有
(3)[Co(NO2)6]3-中三种元素的第一电离能由大到小的顺序是
(4)[Mn(NH3)2]2+中配体分子的立体构型是
(5)MnF2、MnCl2晶体的熔点分别为856 °C、650 °C,二者熔点存在明显差异的主要原因是
(6)碳化钨是一种由钨(W)和碳组成的晶体,其晶体结构如图所示,晶体的熔点为2870° C,硬度与金刚石相当。碳化钨的晶体类型是

您最近一年使用:0次
2022-05-27更新
|
410次组卷
|
5卷引用:新疆博乐高级中学2022届高三第一次诊断性测试理科综合化学试卷
(已下线)新疆博乐高级中学2022届高三第一次诊断性测试理科综合化学试卷河北省秦皇岛市2022届高三三模化学试题(已下线)专题17 物质结构与性质(综合题)-2022年高考真题模拟题分项汇编河南省2022届高三下学期仿真模拟大联考理科综合化学试题广东省部分学校2022届高三下学期高考冲刺化学试题
名校
解题方法
3 . 金属铜和镍及其化合物在工业、农业、国防以及航天等领域都有广泛的用途。请回答下列有关问题:
(1)胆矾 可写成
可写成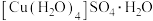 ,其结构示意图如图1所示:
,其结构示意图如图1所示:

①基态 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
② 的空间构型为
的空间构型为_______ 。
③该物质中除了含离子键外,还有_______ 等作用。
(2)某鲜红色含镍物质的结构如图2所示:

①图中非金属元素的电负性由大到小的顺序为_______ (填元素符号)。
②该物质中C原子的杂化轨道类型是_______ 。
(3)镍和铜的第二电离能分别为 、
、 。则
。则
_______  (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是_______ 。
(4)已知氧化镍的晶胞结构如图3所示:

①某缺陷氧化镍的组成为 ,其中
,其中 元素只有
元素只有 和
和 两种价态,则
两种价态,则 和
和 两种价态的镍离子数之比为
两种价态的镍离子数之比为_______ 。
②若该晶体无缺陷,其密度为 ,晶胞中最近的
,晶胞中最近的 之间的距离为
之间的距离为 ,则阿伏加德罗常数
,则阿伏加德罗常数
_______ (用含 、a的代数式表示)。
、a的代数式表示)。
(1)胆矾
 可写成
可写成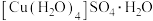 ,其结构示意图如图1所示:
,其结构示意图如图1所示:
①基态
 原子的核外电子排布式为
原子的核外电子排布式为②
 的空间构型为
的空间构型为③该物质中除了含离子键外,还有
(2)某鲜红色含镍物质的结构如图2所示:

①图中非金属元素的电负性由大到小的顺序为
②该物质中C原子的杂化轨道类型是
(3)镍和铜的第二电离能分别为
 、
、 。则
。则
 (填“>”“<”或“=”),其原因是
(填“>”“<”或“=”),其原因是(4)已知氧化镍的晶胞结构如图3所示:

①某缺陷氧化镍的组成为
 ,其中
,其中 元素只有
元素只有 和
和 两种价态,则
两种价态,则 和
和 两种价态的镍离子数之比为
两种价态的镍离子数之比为②若该晶体无缺陷,其密度为
 ,晶胞中最近的
,晶胞中最近的 之间的距离为
之间的距离为 ,则阿伏加德罗常数
,则阿伏加德罗常数
 、a的代数式表示)。
、a的代数式表示)。
您最近一年使用:0次
2022-04-09更新
|
313次组卷
|
2卷引用:新疆石河子第一中学2021-2022学年高二4月月考化学试题



