名校
解题方法
1 . 砷化铝(AlAs)常用作光谱分析试剂和制备电子组件的原料,是一种新型半导体材料。回答下列问题:
(1)基态As原子的核外价电子排布图为_______ ;第一电离能I1(As)_______ I1(Se) (填“大于”或“小于”),其原因是_______ 。
(2)As4S4的分子结构中均为单键,且每个原子最外层均满足8e-稳定结构,则该分子中所含共价键数目为_______ ;分子中As、S原子的杂化轨道类型分别为_______ 、_______ 。
(3)AlF3的熔点约为1 040 ℃,AlCl3的熔点为194 ℃,其晶体类型分别是_______ 、_______ 。
(4)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图1所示,其中的致密保护膜可阻止H2O2刻蚀液与下层GaAs(砷化镓)反应。

已知AlAs的立方晶胞如图2所示,其中As的配位数为_______ ;该晶体密度为ρ g·cm-3,设NA为阿伏加德罗常数的值,晶胞参数为_______ pm。

(1)基态As原子的核外价电子排布图为
(2)As4S4的分子结构中均为单键,且每个原子最外层均满足8e-稳定结构,则该分子中所含共价键数目为
(3)AlF3的熔点约为1 040 ℃,AlCl3的熔点为194 ℃,其晶体类型分别是
(4)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图1所示,其中的致密保护膜可阻止H2O2刻蚀液与下层GaAs(砷化镓)反应。

已知AlAs的立方晶胞如图2所示,其中As的配位数为

您最近一年使用:0次
名校
解题方法
2 . 铜、锌及其化合物在生产生活中有广泛应用。回答下列问题:
(1) 的价层电子排布式为
的价层电子排布式为_______ 。
(2)某锌铁氧体[化学式为ZnxFe(Ⅲ)yOZ制成的磁芯被广泛用于电子行业。
①组成微粒的原子(或离子)中存在未成对电子,该微粒具有顺磁性。指出锌铁氧体晶体中具有顺磁性的离子,并说明理由_______ 。
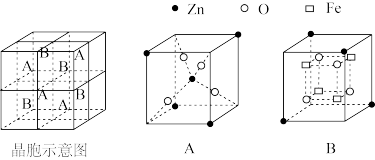
②锌铁氧体晶胞结构如下图所示,该晶胞由4个A型和4个B型小立方体构成。锌铁氧体的化学式为_______ 。
(3)铜离子在水溶液中的结构如图所示。硫酸铜稀溶液中不存在的作用力有_______ (填标号),其中硫酸根的空间构型为_______ 。
A.配位键 B.金属键 C.共价键 D.氢键 E.范德华力

(4) (式量为
(式量为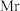 )的晶胞结构如图a所示,阿伏加德罗常数为
)的晶胞结构如图a所示,阿伏加德罗常数为 ,则
,则 晶体的密度为
晶体的密度为_______  (列计算式),图b为
(列计算式),图b为 原子沿z轴方向向x-y平面投影的位置,在图b中画出S原子在该方向的投影位置
原子沿z轴方向向x-y平面投影的位置,在图b中画出S原子在该方向的投影位置_______ (用“●”表示S原子)。
(1)
 的价层电子排布式为
的价层电子排布式为(2)某锌铁氧体[化学式为ZnxFe(Ⅲ)yOZ制成的磁芯被广泛用于电子行业。
①组成微粒的原子(或离子)中存在未成对电子,该微粒具有顺磁性。指出锌铁氧体晶体中具有顺磁性的离子,并说明理由
②锌铁氧体晶胞结构如下图所示,该晶胞由4个A型和4个B型小立方体构成。锌铁氧体的化学式为

(3)铜离子在水溶液中的结构如图所示。硫酸铜稀溶液中不存在的作用力有
A.配位键 B.金属键 C.共价键 D.氢键 E.范德华力

(4)
 (式量为
(式量为 )的晶胞结构如图a所示,阿伏加德罗常数为
)的晶胞结构如图a所示,阿伏加德罗常数为 ,则
,则 晶体的密度为
晶体的密度为 (列计算式),图b为
(列计算式),图b为 原子沿z轴方向向x-y平面投影的位置,在图b中画出S原子在该方向的投影位置
原子沿z轴方向向x-y平面投影的位置,在图b中画出S原子在该方向的投影位置
您最近一年使用:0次
解题方法
3 . M、P、Q三种元素的相关信息如表:
(1)MO3是常见的M的氧化物,液态MO3有单分子MO3和三聚体(MO3)3两种形式;固态MO3主要以三聚体(MO3)3和无限长链(MO3)n两种形式存在。单分子MO3的空间构型为____ 。
②环状(MO3)3和链状(MO3)n的结构如图所示,环状(MO3)3中M原子的杂化轨道类型为____ ,链状(MO3)n中发生杂化的氧原子有____ 个(用含“n”的式于表示)。常温下,单分子MO3是液体,而链状(MO3)n是固体的原因是____ 。

(2)RH3BH3是目前最具潜力的储氢材料之一。
①RH3BH3能溶于水,其主要原因是____ 。
②RH3BH3分子中与R相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键,用“R—H…H—B”表示.以下物质之间可能形成双氢键的是____ (填序号)。
A.LiH和HCN B.C6H6和CHCl3 C.C2H4和C2H2 D.B2H6和NH3
(3)含元素Q、钇(Y)、氧(O)的某正交相晶胞[YaQbOc]结构如图所示。

a:b:c=____ ,已知1号O原子空间坐标为(0,0, ),2号O原子空间坐标为(
),2号O原子空间坐标为( ,
, +m,
+m, +n),则3号Fe原子的空间坐标为
+n),则3号Fe原子的空间坐标为____ 。若晶胞参数分别为apm、bpm和cpm,阿伏加德罗常数的值用NA表示,则该晶体的密度为____ g•cm-3(列表达式)。
| 元素 | 相关信息 |
| M | 基态原子的价电子排布式为3s23p4 |
| R | 空气中含量最多的元素 |
| Q | 常见金属元素,基态原子的M层有4个未成对的电子 |
②环状(MO3)3和链状(MO3)n的结构如图所示,环状(MO3)3中M原子的杂化轨道类型为

(2)RH3BH3是目前最具潜力的储氢材料之一。
①RH3BH3能溶于水,其主要原因是
②RH3BH3分子中与R相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键,用“R—H…H—B”表示.以下物质之间可能形成双氢键的是
A.LiH和HCN B.C6H6和CHCl3 C.C2H4和C2H2 D.B2H6和NH3
(3)含元素Q、钇(Y)、氧(O)的某正交相晶胞[YaQbOc]结构如图所示。

a:b:c=
 ),2号O原子空间坐标为(
),2号O原子空间坐标为( ,
, +m,
+m, +n),则3号Fe原子的空间坐标为
+n),则3号Fe原子的空间坐标为
您最近一年使用:0次
名校
解题方法
4 . A、B、C、D、E是元素周期表中五种短周期元素,原子序数依次增大。A、B、C、D位于同一周期。已知A原子核外有3个能级,且每个能级上的容纳的电子数目相同。C与E同主族,且C的单质为空气中的主要成份。X元素的原子核外有26个运动状态完全不相同的电子。回答下列问题:
(1)C、D、E中第一电离能最大的是___________ (填元素符号)。
(2)B的气态氢化物分子呈___________ 形,该分子的中心原子的杂化方式为___________ 。
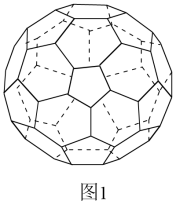
(3)A的一种单质相对分子质量为720,分子构型为如图1所示一个32面体,其中有12个五元环,20个六元环,则1molA的这种单质中π键的数目为___________ 。
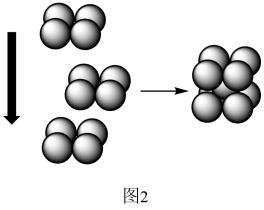
(4)X元素对应的单质在形成晶体时,采用如图2所示的堆积方式,则这种堆积模型的配位数为___________ ,如果X的原子半径为acm,阿伏加德常数的值为NA,则计算此单质的密度表达式为___________ g/cm3(不必化简)。
(1)C、D、E中第一电离能最大的是
(2)B的气态氢化物分子呈
(3)A的一种单质相对分子质量为720,分子构型为如图1所示一个32面体,其中有12个五元环,20个六元环,则1molA的这种单质中π键的数目为

(4)X元素对应的单质在形成晶体时,采用如图2所示的堆积方式,则这种堆积模型的配位数为

您最近一年使用:0次
5 . 2022年春晚中舞蹈诗剧《只此青绿》生动还原了北宋名画,《千里江山图》之所以色彩艳丽,璀璨夺目,与所使用矿物颜料有关。回答下列问题:
(1)石青,又名蓝矿石,化学式为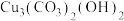 ,基态
,基态 核外电子的空间运动状态有
核外电子的空间运动状态有______ 种, 的空间构型为
的空间构型为________ 。原子中电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数,则
表示,称为电子的自旋磁量子数,则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为________ 。
(2)亚铁氰化钾,化学式为 ,呈黄色结晶性粉末。
,呈黄色结晶性粉末。 中配体
中配体 的配位原子是
的配位原子是________ (填元素符号), 中C原子的杂化方式
中C原子的杂化方式_______ , 中σ键和π键的数目之比为
中σ键和π键的数目之比为________ 。
(3) 呈黑色或灰黑色,已知:晶胞中
呈黑色或灰黑色,已知:晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,晶胞的侧视图如图2所示。
所构成的四面体中心,晶胞的侧视图如图2所示。
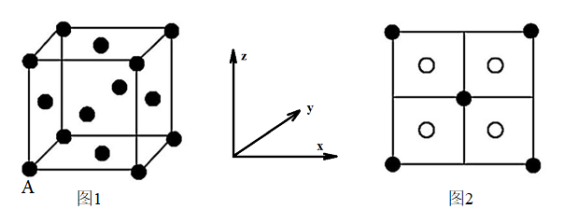
 填充了晶胞中四面体空隙的百分率是
填充了晶胞中四面体空隙的百分率是______ , 配位数为
配位数为________ 。已知图1中A原子的原子分数坐标为(0,0,0),则与A原子距离最近的 的原子分数坐标为
的原子分数坐标为________ 。若晶胞参数anm,晶体的密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为________ (用含a和d的式子表示)。
(1)石青,又名蓝矿石,化学式为
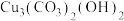 ,基态
,基态 核外电子的空间运动状态有
核外电子的空间运动状态有 的空间构型为
的空间构型为 和
和 表示,称为电子的自旋磁量子数,则
表示,称为电子的自旋磁量子数,则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为(2)亚铁氰化钾,化学式为
 ,呈黄色结晶性粉末。
,呈黄色结晶性粉末。 中配体
中配体 的配位原子是
的配位原子是 中C原子的杂化方式
中C原子的杂化方式 中σ键和π键的数目之比为
中σ键和π键的数目之比为(3)
 呈黑色或灰黑色,已知:晶胞中
呈黑色或灰黑色,已知:晶胞中 的位置如图1所示,
的位置如图1所示, 位于
位于 所构成的四面体中心,晶胞的侧视图如图2所示。
所构成的四面体中心,晶胞的侧视图如图2所示。
 填充了晶胞中四面体空隙的百分率是
填充了晶胞中四面体空隙的百分率是 配位数为
配位数为 的原子分数坐标为
的原子分数坐标为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为
您最近一年使用:0次
2022-03-06更新
|
1124次组卷
|
3卷引用:福建省连城县第一中学2022-2023学年高三上学期第二次月考化学试题
福建省连城县第一中学2022-2023学年高三上学期第二次月考化学试题山东省日照市 2022届高三第一次模拟考试化学试题(已下线)专题13 物质结构与性质—2022年高考化学二轮复习讲练测(全国版)-测试



