解题方法
1 . 第四周期某些过渡元素在工业生产中有着极其重要的作用。
(1)铬是最硬的金属单质,被称为“不锈钢的添加剂”。写出Cr原子价电子排布图___________ 。
(2)钒广泛用于催化及钢铁工业,被称之为“工业的味精”。 常用作
常用作 转化为
转化为 的催化剂。
的催化剂。 分子VSEPR模型是
分子VSEPR模型是___________ ; 气态为单分子,
气态为单分子, 的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为
的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为___________ ;该结构中S-O键长有两类,一类键长约140pm,另一类键长约为160pm,较长的键为___________ (填图中字母a或者b)。

(3)镍是一种优良的有机反应催化剂,Ni能与CO形成正四面体形的配合物 ,其中配原子是C,原因是
,其中配原子是C,原因是___________ 。
(4)钛称之为21世纪金属,具有一定的生物功能。钙钛矿( )晶体是工业获取钛的重要原料。
)晶体是工业获取钛的重要原料。 晶胞如图,晶胞参数为a nm,晶胞中Ti、Ca、O分别处于顶角、体心、面心位置。Ti与O间的最短距离为
晶胞如图,晶胞参数为a nm,晶胞中Ti、Ca、O分别处于顶角、体心、面心位置。Ti与O间的最短距离为___________ nm,与Ti紧邻的O个数为___________ 。

(5)在 晶胞结构的另一种表示形式中,Ti处于体心位置,则Ca处于
晶胞结构的另一种表示形式中,Ti处于体心位置,则Ca处于___________ 位置,O处于___________ 位置。
(1)铬是最硬的金属单质,被称为“不锈钢的添加剂”。写出Cr原子价电子排布图
(2)钒广泛用于催化及钢铁工业,被称之为“工业的味精”。
 常用作
常用作 转化为
转化为 的催化剂。
的催化剂。 分子VSEPR模型是
分子VSEPR模型是 气态为单分子,
气态为单分子, 的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为
的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为
(3)镍是一种优良的有机反应催化剂,Ni能与CO形成正四面体形的配合物
 ,其中配原子是C,原因是
,其中配原子是C,原因是(4)钛称之为21世纪金属,具有一定的生物功能。钙钛矿(
 )晶体是工业获取钛的重要原料。
)晶体是工业获取钛的重要原料。 晶胞如图,晶胞参数为a nm,晶胞中Ti、Ca、O分别处于顶角、体心、面心位置。Ti与O间的最短距离为
晶胞如图,晶胞参数为a nm,晶胞中Ti、Ca、O分别处于顶角、体心、面心位置。Ti与O间的最短距离为
(5)在
 晶胞结构的另一种表示形式中,Ti处于体心位置,则Ca处于
晶胞结构的另一种表示形式中,Ti处于体心位置,则Ca处于
您最近一年使用:0次
解题方法
2 . 胆矾(CuSO4·5H2O)可用于泳池杀菌消毒。回答下列问题:
(1)铜元素位于元素周期表的_____ 区,基态Cu原子的核外电子排布式为_____ 。
(2)CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,其结构示意图如图:
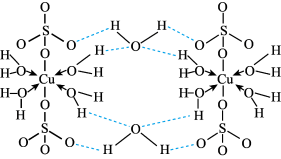
① 的空间构型为
的空间构型为_____ ,其中硫原子的杂化方式为_____ 。
②硫酸铜晶体中Cu2+的配位数为_____ ,[Cu(H2O)4]2+中配位原子是_____ 。
③在上述结构示意图中,存在的化学键有_____ 。
(3)向CuSO4溶液中逐滴加入氨水,溶液最终变为深蓝色,原因是_____ 。
(1)铜元素位于元素周期表的
(2)CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,其结构示意图如图:

①
 的空间构型为
的空间构型为②硫酸铜晶体中Cu2+的配位数为
③在上述结构示意图中,存在的化学键有
(3)向CuSO4溶液中逐滴加入氨水,溶液最终变为深蓝色,原因是
您最近一年使用:0次
2023-04-06更新
|
180次组卷
|
2卷引用:湖北省宜昌市协作体2022-2023学年高二下学期期中考试化学试题
名校
解题方法
3 . 碳氮硫共脱除工艺可以协同除去工业废水中的S2-、NO 和CH3COO-,过程如图所示。已知:成键原子共平面,每个原子能提供一个相互平行的p轨道且p轨道电子数小于参加成键的p轨道数的两倍时可形成离域π键。下列说法错误的是
和CH3COO-,过程如图所示。已知:成键原子共平面,每个原子能提供一个相互平行的p轨道且p轨道电子数小于参加成键的p轨道数的两倍时可形成离域π键。下列说法错误的是
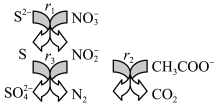
 和CH3COO-,过程如图所示。已知:成键原子共平面,每个原子能提供一个相互平行的p轨道且p轨道电子数小于参加成键的p轨道数的两倍时可形成离域π键。下列说法错误的是
和CH3COO-,过程如图所示。已知:成键原子共平面,每个原子能提供一个相互平行的p轨道且p轨道电子数小于参加成键的p轨道数的两倍时可形成离域π键。下列说法错误的是
| A.N2和CO2都是非极性分子 |
B.NO 和NO 和NO 的空间构型相同 的空间构型相同 |
C.NO 中存在离域π键 中存在离域π键 |
| D.冰醋酸中CH3COOH分子间存在范德华力和氢键 |
您最近一年使用:0次
2023-01-15更新
|
579次组卷
|
4卷引用:湖北省部分重点中学(武汉市,十堰市,襄阳市,恩施土家族苗族自治州)2022-2023学年高二下学期三月智学联合检测化学试题
名校
解题方法
4 . 推广磷酸亚铁锂电池的新能源汽车对减少二氧化碳排放和大气污染具有重要意义。工业上用FeCl3、NH4H2PO4、LiCl及苯胺( )为原料制磷酸亚铁锂材料。
)为原料制磷酸亚铁锂材料。
回答下列问题:
(1)基态铁原子核外电子运动状态有______ 种;基态Fe3+较基态Fe2+稳定的原因是______ 。
(2)在NH4H2PO4中的N、P、O三种元素的电负性由大到小的顺序是______ ;NH 的空间构型为
的空间构型为______ ;H2PO 中P原子的杂化轨道类型为
中P原子的杂化轨道类型为______ 。
(3)1mol 中含有
中含有______ molσ键;苯胺水溶性大于苯的主要原因是______ 。
(4)构想某锂电池的负极材料晶体是锂原子嵌入石墨烯层间,晶体结构如图。

①石墨的硬度小、熔沸点高的原因分别是______ 。
②如图晶体的化学式为______ ;该晶体中最近的两个碳原子核间距离为142pm,石墨烯层间距离为335pm,则该晶体的密度为______ g•cm-3(用NA表示阿伏加德罗常数,列式即可)。
 )为原料制磷酸亚铁锂材料。
)为原料制磷酸亚铁锂材料。回答下列问题:
(1)基态铁原子核外电子运动状态有
(2)在NH4H2PO4中的N、P、O三种元素的电负性由大到小的顺序是
 的空间构型为
的空间构型为 中P原子的杂化轨道类型为
中P原子的杂化轨道类型为(3)1mol
 中含有
中含有(4)构想某锂电池的负极材料晶体是锂原子嵌入石墨烯层间,晶体结构如图。

①石墨的硬度小、熔沸点高的原因分别是
②如图晶体的化学式为
您最近一年使用:0次
2021-12-30更新
|
1453次组卷
|
6卷引用:湖北省部分重点中学(武汉市,十堰市,襄阳市,恩施土家族苗族自治州)2022-2023学年高二下学期三月智学联合检测化学试题
湖北省部分重点中学(武汉市,十堰市,襄阳市,恩施土家族苗族自治州)2022-2023学年高二下学期三月智学联合检测化学试题四川省成都市2021-2022学年高三上学期第一次诊断性检测理综化学试题(已下线)回归教材重难点11 物质结构与性质-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点11 物质结构与性质(选考)-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)押新高考卷15题 物质结构与性质综合题-备战2022年高考化学临考题号押题(新高考通版)宁夏回族自治区石嘴山市平罗中学2022届高三第三次模拟理科综合化学试题



