1 . 如表为四种短周期元素的相关信息
回答下列问题(注:涉及元素的均要用对应元素的元素符号书写作答)
(1)Y元素的最简单氢化物的空间构型是___ 。
(2)Z、Q、R相比,其原子半径由大到小的顺序是___ 。
(3)最高价的R与Z元素组成的化合物中R原子的杂化方式为___ ,其中R在周期表中的位置是__ ,R的基态原子电子排布式为___ 。
(4)与O3分子互为等电子体的一种分子为___ ,阴离子为__ 。
(5)Y与R相比,非金属性较强的是___ ,能证明这一结论的事实是___ 。(用化学方程式表示)
| 元素 | 元素的相关信息 |
| Y | 原子最外层电子数是次外层电子数的2倍 |
| Z | 地壳中含量最多的元素 |
| Q | 短周期中金属性最强 |
| R | 常温下,R的单质是淡黄色固体,常在火山喷口附近沉积 |
(1)Y元素的最简单氢化物的空间构型是
(2)Z、Q、R相比,其原子半径由大到小的顺序是
(3)最高价的R与Z元素组成的化合物中R原子的杂化方式为
(4)与O3分子互为等电子体的一种分子为
(5)Y与R相比,非金属性较强的是
您最近一年使用:0次
名校
2 . 锰及其化合物用途非常广泛。回答下列问题:
(1)Al70Pd21Mn9是一种准晶体(介于晶体和非晶体之间的固体),能准确证明其不是晶体的方法是___________ 。
(2)基态Mn原子的价电子排布式为_________ ,未成对电子数为_____ 个。
(3)MnS熔点(1610℃)比MnO熔点(1650℃)低,其原因是____________ 。
(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]Br。
①配合物中锰元素的价态为________ 。
②配体CH3CN与中心原子形成配位键时,提供孤对电子的原子是_____ ,该分子中碳原子的杂化方式为_______ ;C、H、N的电负性从大到小的顺序为________ 。
(5)锰的含氧酸有HMnO4(高锰酸)、H2MnO3(亚锰酸),高锰酸的酸性比亚锰酸强,理由是_________ 。
(6)某种含锰特殊材料的晶胞结构如下图所示:
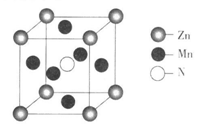
若晶胞参数为a nm,用NA表示阿伏伽德罗常数的值,则该晶胞的密度为____ ( 列出代数式即可)。
(1)Al70Pd21Mn9是一种准晶体(介于晶体和非晶体之间的固体),能准确证明其不是晶体的方法是
(2)基态Mn原子的价电子排布式为
(3)MnS熔点(1610℃)比MnO熔点(1650℃)低,其原因是
(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]Br。
①配合物中锰元素的价态为
②配体CH3CN与中心原子形成配位键时,提供孤对电子的原子是
(5)锰的含氧酸有HMnO4(高锰酸)、H2MnO3(亚锰酸),高锰酸的酸性比亚锰酸强,理由是
(6)某种含锰特殊材料的晶胞结构如下图所示:

若晶胞参数为a nm,用NA表示阿伏伽德罗常数的值,则该晶胞的密度为
您最近一年使用:0次
2018-05-17更新
|
386次组卷
|
2卷引用:河北省石家庄精英中学2020-2021学年高二下学期期末考试化学试题
3 . 高分子化合物在材料领域发挥着重要作用。下列说法错误的是
A.芳纶( )的两种单体核磁共振氢谱峰数、峰面积之比均相等 )的两种单体核磁共振氢谱峰数、峰面积之比均相等 |
B.酚醛树脂( )的单体中C原子的杂化方式均为 )的单体中C原子的杂化方式均为 |
C.全降解塑料( )可由 )可由 和 和 通过加聚反应制得 通过加聚反应制得 |
D.塑料王( )耐高温、耐腐蚀与F的电负性大、 )耐高温、耐腐蚀与F的电负性大、 键能大有关 键能大有关 |
您最近一年使用:0次
名校
4 . 2022年诺贝尔化学奖授予了研究“点击化学和生物正交化学”的三位科学家.已知“点击化学”中的一个经典反应如下:正确 的是

| A.该反应为加成反应 |
| B.上述反应物和产物均属于烃 |
| C.上述反应所涉及的物质中,C原子的杂化方式有两种 |
| D.生成物分子中所有原子可能在同一平面 |
您最近一年使用:0次
2023-04-28更新
|
178次组卷
|
2卷引用:河北省邯郸市武安市第一中学2023-2024学年高二下学期4月期中考试化学试题
名校
解题方法
5 . 共价化合物 中所有原子均满足8电子稳定结构,一定条件下可发生反应:
中所有原子均满足8电子稳定结构,一定条件下可发生反应: ,下列说法
,下列说法不正确 的是
 中所有原子均满足8电子稳定结构,一定条件下可发生反应:
中所有原子均满足8电子稳定结构,一定条件下可发生反应: ,下列说法
,下列说法A. 的结构式为 的结构式为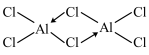 |
B. 为非极性分子 为非极性分子 |
C. 中N是 中N是 杂化 杂化 |
D.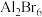 比 比 更难与 更难与 发生反应 发生反应 |
您最近一年使用:0次
2023-04-22更新
|
455次组卷
|
3卷引用:河北省唐县第一中学2022-2023学年高二下学期5月月考化学试题
名校
6 . “年年重午近佳辰,符艾一番新”,端午节常采艾草悬于门户上,艾叶中含有薄荷醇(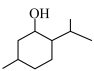 ),下列有关该物质的说法不正确的是
),下列有关该物质的说法不正确的是
 ),下列有关该物质的说法不正确的是
),下列有关该物质的说法不正确的是| A.环上的一氯代物为3种 |
B.与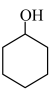 互为同系物 互为同系物 |
| C.该物质能使酸性高锰酸钾溶液褪色 |
| D.该分子中sp3杂化的原子数为11个 |
您最近一年使用:0次
2023-04-05更新
|
1621次组卷
|
3卷引用:河北省张家口市宣化第一中学2022-2023学年高二下学期5月期中化学试题
名校
7 . 法匹拉韦是治疗新冠肺炎的种药物,其结构简式如图所示,下列说法错误的是
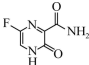

A.该分子中N、O、F的电负性由大到小的顺序为 |
| B.该分子中C—H键的键能大于N—H键的键能 |
| C.该分子中所有C原子都为sp2杂化 |
| D.该分子可形成分子间氢键 |
您最近一年使用:0次
名校
8 . 顺铂,又名顺式-二氯二氨合铂,是第一代铂类抗癌药物,化学式为:[Pt(NH3)2Cl2],其同分异构体反铂则不具有抗癌作用。碳铂是1,1-环丁二羧酸二氨合铂的简称,为第二代铂类抗癌药。奥沙利铂为第三代抗癌药。这三种药物的结构分别如图所示:

则下列说法错误的是

则下列说法错误的是
| A.该三种物质均为配合物,且中心离子为Pt2+,配位原子为Cl原子、N原子和O原子,Pt2+的配位数均为4 |
| B.顺铂与AgNO3溶液混合后可产生白色沉淀 |
| C.1mol碳铂中σ键数目为26NA |
| D.奥沙利铂中所有碳原子和氮原子的杂化均为sp3杂化 |
您最近一年使用:0次
2023-01-13更新
|
224次组卷
|
2卷引用:河北省邢台市第二中学2022-2023学年高二上学期期末考试化学试题
名校
9 . As2O3(砒霜)是两性氧化物,分子结构如图所示,与盐酸反应能生成AsCl3,AsCl3和LiAlH4反应的产物之一为AsH3。下列说法不正确的是
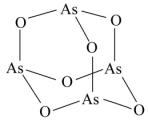

| A.As2O3分子中As原子的杂化方式为sp3 |
B.AlH 的价层电子对互斥模型是四面体形 的价层电子对互斥模型是四面体形 |
| C.AsCl3的空间构型为平面正三角形,As原子的杂化方式为sp3 |
| D.AsH3分子的键角小于109°28′ |
您最近一年使用:0次
2023-01-05更新
|
630次组卷
|
3卷引用:河北省唐山市开滦第一中学2022-2023学年高二上学期12月月考化学试题
名校
解题方法
10 . 白磷( ,结构如图所示)与
,结构如图所示)与 反应得
反应得 ,
, 可继续与
可继续与 反应:
反应:
 。固态
。固态 中含有
中含有 、
、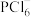 两种离子。下列关于
两种离子。下列关于 、
、 、
、 和
和 的说法正确的是
的说法正确的是
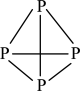
 ,结构如图所示)与
,结构如图所示)与 反应得
反应得 ,
, 可继续与
可继续与 反应:
反应:
 。固态
。固态 中含有
中含有 、
、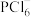 两种离子。下列关于
两种离子。下列关于 、
、 、
、 和
和 的说法正确的是
的说法正确的是
A. 很稳定是因为分子间含有氢键 很稳定是因为分子间含有氢键 |
B. 的空间构型为平面三角形 的空间构型为平面三角形 |
C. 与 与 中的P原子杂化方式均为 中的P原子杂化方式均为 杂化,键角相同 杂化,键角相同 |
D.1  分子中成键电子对与孤电子对的比值为3∶2 分子中成键电子对与孤电子对的比值为3∶2 |
您最近一年使用:0次
2022-12-30更新
|
591次组卷
|
5卷引用:河北省石家庄实验中学2022-2023学年高二上学期期末考试化学试题



