名校
解题方法
1 . 下列关于含氧物质的化学用语正确的是
| A.甲醛(HCHO)的空间结构:平面三角形 | B.中子数为10的氧原子: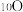 |
C. 分子中O的杂化方式: 分子中O的杂化方式: 杂化 杂化 | D.次氯酸的结构式: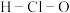 |
您最近一年使用:0次
名校
解题方法
2 . 在酸性或者接近中性的条件下, 易发生歧化反应,将
易发生歧化反应,将 通入
通入 溶液中,其反应为
溶液中,其反应为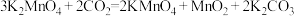 。下列有关说法错误的是
。下列有关说法错误的是
 易发生歧化反应,将
易发生歧化反应,将 通入
通入 溶液中,其反应为
溶液中,其反应为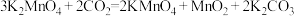 。下列有关说法错误的是
。下列有关说法错误的是A. 的空间结构为平面三角形 的空间结构为平面三角形 |
B. 中心原子的杂化方式是 中心原子的杂化方式是 |
C.基态钾原子的价电子排布式: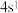 |
D.基态 的价电子轨道表示式: 的价电子轨道表示式: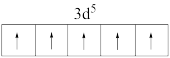 |
您最近一年使用:0次
2023-06-09更新
|
197次组卷
|
4卷引用:河北省沧州市青县等5地八校联盟2022-2023学年高三上学期11月期中考试化学试题
名校
3 . 中国政府承诺:力争CO2的排放在2030年前实现“碳达峰”,2060年前实现“碳中和”,CO2的捕集与利用成为当前研究的热点。回答下面问题:
(1)写出CO2的电子式______ ,CO2分子属于______ (填“极性”或“非极性”)分子,其晶体俗名干冰,属于______ 晶体,其晶体内存在的微粒间相互作用有______ 。
(2)研究发现,在CO2合成甲醇(CH3OH)反应中,Co、Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Mn基态原子核外电子排布式为______ 。Co在周期表中属于______ 区元素。甲醇(CH3OH)能够与水任意比互溶,解释其原因是______ 。
(3)金属Zn属于金属晶体,其导电的原因是是______ 。已知金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为______ 。
(4)CaF2的晶胞结构如图所示,X代表的离子是______ ;若该立方晶胞参数为apm,CaF2的摩尔质量用Mg/mol,阿伏伽德罗常数用NA来表示,则CaF2晶体的密度=______ g/cm3(写出表达式),阴阳离子的核间距最小为______ pm。

(1)写出CO2的电子式
(2)研究发现,在CO2合成甲醇(CH3OH)反应中,Co、Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Mn基态原子核外电子排布式为
(3)金属Zn属于金属晶体,其导电的原因是是
(4)CaF2的晶胞结构如图所示,X代表的离子是

您最近一年使用:0次
名校
解题方法
4 . 金刚石、石墨烯和C60的结构示意图如图,下列说法中错误的是
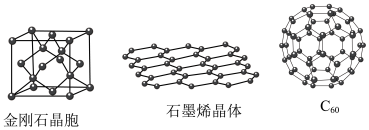

| A.每个金刚石晶胞中包括的C原子个数为8 |
| B.石墨烯属于烃 |
| C.石墨烯中碳原子的杂化轨道类型为sp2,碳碳键的键角是120° |
| D.1个C60分子中含有12个正五边形和20个正六边形 |
您最近一年使用:0次
5 . 氯化铍晶体易吸湿、水解、升华,可溶于有机溶剂。一定条件下有下列存在形式:
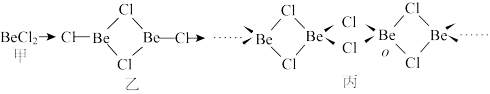
下列有关说法错误 的是

下列有关说法
| A.氯化铍晶体的晶体类型为分子晶体 |
| B.甲的空间结构是直线形 |
C.乙中 的杂化轨道类型是 的杂化轨道类型是 |
D. 丙 丙 中配位键数为 中配位键数为 |
您最近一年使用:0次
解题方法
6 . 硅与碳同主族,是构成地壳的主要元素之一,下列说法正确的是
| A.键能:Si-Si<C-C |
B. 和 和 中C、Si化合价均为-4价 中C、Si化合价均为-4价 |
| C.硅酸盐与碳酸盐中Si、C原子的杂化方式相同 |
D.相比较碳原子,硅与硅之间更易形成 键 键 |
您最近一年使用:0次
2023-04-29更新
|
212次组卷
|
2卷引用:河北省石家庄部分重点高中2022-2023学年高三下学期4月期中化学试题
7 .  ,
, ,
, 都是重要的有机反应中间体,有关它们的说法正确的是
都是重要的有机反应中间体,有关它们的说法正确的是
 ,
, ,
, 都是重要的有机反应中间体,有关它们的说法正确的是
都是重要的有机反应中间体,有关它们的说法正确的是A. 的几何构型为三角锥形 的几何构型为三角锥形 |
B. 中含有7mol电子 中含有7mol电子 |
C. 与 与 形成的化合物中含有离子键 形成的化合物中含有离子键 |
D. 中的碳原子采取 中的碳原子采取 杂化,键角为 杂化,键角为 |
您最近一年使用:0次
8 . 下列有关化学史知识错误的是
| A.英国科学家汤姆生首先发现了电子 |
| B.原子分子学说的建立是近代化学发展的里程碑 |
| C.美国化学家鲍林第一次提出了杂化轨道理论 |
| D.意大利科学家阿伏加德罗在总结气体反应体积比的基础上提出了原子的概念 |
您最近一年使用:0次
9 . 我国自主研发对二甲苯的绿色合成路线如下图所示,有关说法不正确的是
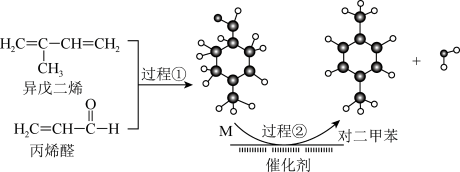
已知: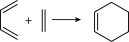 称为狄尔斯−阿德耳反应,又称为双烯合成。
称为狄尔斯−阿德耳反应,又称为双烯合成。

已知:
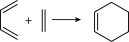 称为狄尔斯−阿德耳反应,又称为双烯合成。
称为狄尔斯−阿德耳反应,又称为双烯合成。| A.过程①发生了加成反应 |
B.过程②中六元环上C原子的杂化方式都是由 变为 变为 |
| C.该反应的副产物可能有间二甲苯 |
D.M的结构简式为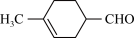 |
您最近一年使用:0次
10 . 已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素,化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)。
(1)A、B、C的第一电离能由小到大的顺序为_______ 。
(2)B的氢化物的分子空间构型是_______ 其中心原于采取_______ 杂化。
(3)写出化合物AC2的电子式_______ ;分子空间构型是_______ ;其中心原子采取_______ 杂化。
(4)E的核外电子排市式是_______ 。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是_______ 。
(1)A、B、C的第一电离能由小到大的顺序为
(2)B的氢化物的分子空间构型是
(3)写出化合物AC2的电子式
(4)E的核外电子排市式是
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
您最近一年使用:0次



