名校
1 . 在一定条件下,[Zn(CN)4]2-与甲醛发生如下反应:[Zn(CN)4]2-+4HCHO+4H2O=[Zn(OH)4]2-+4HOCH2CN
已知:ⅰ. HCN为剧毒、易挥发的气体,其水溶液有极弱的酸性
ⅱ. Zn2++4CN- [Zn(CN)4]2- K1;Zn2++4OH-
[Zn(CN)4]2- K1;Zn2++4OH- [Zn(OH)4]2- K2
[Zn(OH)4]2- K2
下列说法不正确 的是
已知:ⅰ. HCN为剧毒、易挥发的气体,其水溶液有极弱的酸性
ⅱ. Zn2++4CN-
 [Zn(CN)4]2- K1;Zn2++4OH-
[Zn(CN)4]2- K1;Zn2++4OH- [Zn(OH)4]2- K2
[Zn(OH)4]2- K2下列说法
| A.反应前后Zn2+均提供4个空轨道容纳4对孤电子对 |
| B.HOCH2CN的氰基由CN-与甲醛发生反应而来 |
| C.依据上述[Zn(CN)4]2-与甲醛的反应可以证明:K1<K2 |
| D.上述反应必须在碱性条件下进行,既保证安全性,也能提高反应物转化率 |
您最近一年使用:0次
2022-05-31更新
|
783次组卷
|
3卷引用:北京市海淀区北京大学附属中学2022届高三下学期三模化学试题
北京市海淀区北京大学附属中学2022届高三下学期三模化学试题山西省晋中市祁县中学2022-2023学年高三上学期10月月考化学试题(已下线)第37讲 分子结构与性质(练)-2023年高考化学一轮复习讲练测(全国通用)
2 . 向盛有 溶液的试管中滴加浓氨水,先生成难溶物,继续滴加浓氨水,难溶物溶解,得到蓝色透明溶液。下列对此现象的说法正确的是
溶液的试管中滴加浓氨水,先生成难溶物,继续滴加浓氨水,难溶物溶解,得到蓝色透明溶液。下列对此现象的说法正确的是
 溶液的试管中滴加浓氨水,先生成难溶物,继续滴加浓氨水,难溶物溶解,得到蓝色透明溶液。下列对此现象的说法正确的是
溶液的试管中滴加浓氨水,先生成难溶物,继续滴加浓氨水,难溶物溶解,得到蓝色透明溶液。下列对此现象的说法正确的是A.反应后溶液中不存在任何沉淀,所以反应前后 的浓度不变 的浓度不变 |
B.沉淀溶解后,生成深蓝色的配离子 |
C.该实验能证明 比 比 稳定 稳定 |
D.在配离子 中, 中, 提供孤电子对, 提供孤电子对, 提供空轨道 提供空轨道 |
您最近一年使用:0次
2021-02-16更新
|
111次组卷
|
2卷引用:(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 第3节 离子键、配位键与金属键
11-12高二上·江苏泰州·期中
名校
3 . 向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是
| A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B.沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+ |
| C.该实验不能证明[Cu(NH3)4]2+比氢氧化铜稳定 |
| D.在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
您最近一年使用:0次
2019-01-30更新
|
358次组卷
|
5卷引用:2011-2012学年江苏省泰州中学高二上学期期中考试化学(选修)试卷
(已下线)2011-2012学年江苏省泰州中学高二上学期期中考试化学(选修)试卷(已下线)2011-2012学年山西省临汾一中高二第二学期3月月考化学试卷2016-2017学年河南省洛阳市第一高级中学高二(平行班)3月月考化学试卷2020高三总复习二轮复习——物质结构与性质复习卷福建省龙海市第二中学2019-2020学年高二下学期期末考试化学试题
解题方法
4 . 下列实验方案不能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 证明 | 向盛有浓度均为 的 的 和 和 混合溶液的试管中滴加几滴 混合溶液的试管中滴加几滴 溶液,振荡,观察沉淀颜色 溶液,振荡,观察沉淀颜色 |
| B | 制备 晶体 晶体 | 向 溶液中加入95%的乙醇 溶液中加入95%的乙醇 |
| C | 比较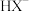 的电离程度与水解程度的大小 的电离程度与水解程度的大小 | 室温下,用 计测量一定浓度某弱酸盐 计测量一定浓度某弱酸盐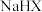 溶液的 溶液的 |
| D | 氧化性: | 向 溶液中通入少量氯气,然后再加入少量苯萃取上层为橙红色 溶液中通入少量氯气,然后再加入少量苯萃取上层为橙红色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-16更新
|
138次组卷
|
2卷引用:2024届名校联盟(T8联盟)高三下学期模拟信息(五)理科综合试题-高中化学
5 . 某中学同学在做铜与浓硫酸(装置如图)的反应实验时,发现有如下的反应现象:加热初期,铜丝表面变黑;继续加热,有大量气泡产生,品红溶液褪色,溶液变为墨绿色浊液,试管底部开始有灰白色沉淀生成;再加热,试管中出现“白雾”,浊液逐渐变为澄清,溶液颜色慢慢变为浅蓝色,试管底部灰白色沉淀增多;冷却,静置,将试管中液体倒入另一支盛水试管中,管壁发汤,溶液略带蓝色,将灰白色固体倒入水中,形成蓝色溶液。

(1)资料:聚四氯乙烯受热分解产生氯化氢,[CuCl4]2-呈黄色,[Cu(H2O)4]2+呈蓝色,两者混合则成绿色,铜的化合物中CuO、CuS、Cu2S都为黑色,其中CuO溶于盐酸;CuS、Cu2S不溶于稀盐酸,但溶于浓盐酸。该反应中,品红溶液褪色,体现SO2的______ 性,NaOH溶液的作用是______ 。
该中学同学分成几个小组分别对上述现象探究:
(2)甲组同学查相关文献资料获知:在较低温度(100℃)下,浓硫酸氧化性相对较弱,生成的黑色沉淀为Cu2S,溶液变蓝,但没有气泡产生。请根据文献资料写出反应的化学方程式:______ 。
(3)乙组同学对实验中形成的墨绿色溶液进行探究,特进行下列实验:
请解释形成墨绿色的原因:______ 。
(4)丙组同学对白雾的成分经检验为H2SO4,请设计实验证明该白雾为硫酸:______ 。溶液的蓝色变浅,灰白色沉淀增多,这现象体现浓硫酸的______ 性。
(5)丁组同学进一步对灰白色沉淀通过加水溶解、过滤,最后沉淀为黑色,取其黑色沉淀,进行成分探究:
滴加适量稀盐酸,则发现黑色沉淀几乎不溶解,溶液也不变蓝,则说明黑色沉淀中不含有______ 。
滴加适量浓盐酸,振荡,加热,观察到黑色沉淀几乎完全溶解,溶液呈略黄色[CuCln]2-n(n=1~4)。写出CuS与浓盐酸反应的离子方程式:______ 。
最后,丁组同学经过实验论证证明黑色沉淀中除了有CuS、Cu2S,还有S等。

(1)资料:聚四氯乙烯受热分解产生氯化氢,[CuCl4]2-呈黄色,[Cu(H2O)4]2+呈蓝色,两者混合则成绿色,铜的化合物中CuO、CuS、Cu2S都为黑色,其中CuO溶于盐酸;CuS、Cu2S不溶于稀盐酸,但溶于浓盐酸。该反应中,品红溶液褪色,体现SO2的
该中学同学分成几个小组分别对上述现象探究:
(2)甲组同学查相关文献资料获知:在较低温度(100℃)下,浓硫酸氧化性相对较弱,生成的黑色沉淀为Cu2S,溶液变蓝,但没有气泡产生。请根据文献资料写出反应的化学方程式:
(3)乙组同学对实验中形成的墨绿色溶液进行探究,特进行下列实验:
| 现象 | ||
| I组 | 取灼烧后的铜丝 | 溶液变蓝 |
| Ⅱ组 | 直接取其铜丝(表面有聚四氯乙烯薄膜) | 溶液变成墨绿色 |
(4)丙组同学对白雾的成分经检验为H2SO4,请设计实验证明该白雾为硫酸:
(5)丁组同学进一步对灰白色沉淀通过加水溶解、过滤,最后沉淀为黑色,取其黑色沉淀,进行成分探究:
滴加适量稀盐酸,则发现黑色沉淀几乎不溶解,溶液也不变蓝,则说明黑色沉淀中不含有
滴加适量浓盐酸,振荡,加热,观察到黑色沉淀几乎完全溶解,溶液呈略黄色[CuCln]2-n(n=1~4)。写出CuS与浓盐酸反应的离子方程式:
最后,丁组同学经过实验论证证明黑色沉淀中除了有CuS、Cu2S,还有S等。
您最近一年使用:0次
解题方法
6 . 下列实验设计、现象和结论都正确的是
| 选项 | 实验目的 | 实验设计 | 现象和结论 |
| A | 探究温度对化学平衡的影响 | 加热0.5mol•L-1CuCl2蓝色溶液 | 加热溶液变为蓝绿色,说明[Cu(H2O)4]2+转化为[CuCl4]2-吸热 |
| B | 比较AgBr和AgCl的Ksp大小 | 向NaCl和NaBr的混合溶液中逐滴加入少量AgNO3溶液 | 产生淡黄色沉淀,说明Ksp(AgBr)<Ksp(AgCl) |
| C | 证明干燥的氯气不具有漂白性 | 将干燥的氯气通入盛放红色鲜花的集气瓶中 | 红色鲜花颜色褪去,说明干燥的氯气有漂白性 |
| D | 探究浓度对反应速率的影响 | 室温下向A、B两支试管中分别装入等体积的稀硫酸和浓硫酸,再加入表面积相等的铁片 | B试管中无明显现象,说明浓度越大反应速率越慢 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 下列实验方案设计、现象和结论都正确的是
选项 | 实验目的 | 实验方案设计 | 现象和结论 |
A | 验证 与 与 在配合物中存在相互竞争 在配合物中存在相互竞争 | 向 溶液中加入少量 溶液中加入少量 固体 固体 | 溶液由蓝色变为黄绿色,说明发生了 到[ 到[ 的转化 的转化 |
B | 探究不同价态硫元素的转化 | 向 和 和 的混合溶液中加入浓硫酸 的混合溶液中加入浓硫酸 | 溶液变浑浊,证明 和 和 发生了氧化还原反应 发生了氧化还原反应 |
C | 实验室中制取并检验乙烯 | 取 乙醇,加入 乙醇,加入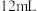 浓硫酸及少量沸石,逐渐升温至 浓硫酸及少量沸石,逐渐升温至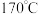 ,将产生的气体依次通过品红和溴水 ,将产生的气体依次通过品红和溴水 | 溴水褪色,说明产物中有乙烯生成 |
D | 检验苯酚中是否混有少量苯甲酸 | 向混合液中加入饱和 溶液 溶液 | 无气泡产生,证明不含苯甲酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 在处理NO废气的过程中,催化剂[Co(NH3)6]2+会逐渐失活变为[Co(NH3)6]3+。某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。
资料:i.Ksp[Co(OH)2]=5.9×10-15,Ksp[Co(OH)3]=1.6×10-44
ii.Co2++6NH3 [Co(NH3)6]2+K1=1.3×105
[Co(NH3)6]2+K1=1.3×105
Co3++6NH3 [Co(NH3)6]3+K2=2×1035
[Co(NH3)6]3+K2=2×1035
iii.[Co(NH3)6]2+和[Co(NH3)6]3+在酸性条件下均能生成NH
(1)探究 的还原性
的还原性
实验I.粉红色的CoCl2溶液或CoSO4溶液在空气中久置,无明显变化。
实验II.向0.1mol/LCoCl2溶液中滴入2滴酸性KMnO4溶液,无明显变化。
实验III.按如图装置进行实验,观察到电压表指针偏转。
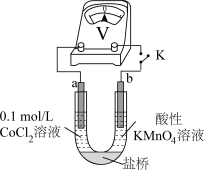
①甲同学根据实验III得出结论:Co2+可以被酸性KMnO4溶液氧化。
乙同学补充实验IV,____ (补全实验操作及现象),否定了该观点。
②探究碱性条件下 的还原性,进行实验。
的还原性,进行实验。
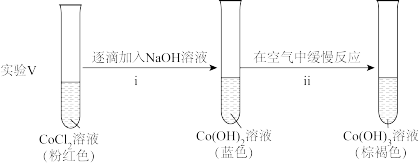
ii中反应的化学方程式是____ 。
③根据氧化还原反应规律解释:还原性Co(OH)2>Co2+:Co2+-e-=Co3+在碱性条件下,OH-与Co2+、Co3+反应,使c(Co2+)和c(Co3+)均降低,但____ 降低的程度更大,还原剂的还原性增强。
(2)探究 的氧化性
的氧化性
①根据实验III和IV推测氧化性:Co3+>Cl2,设计实验证明:向V中得到的棕褐色沉淀中,____ (补全实验操作及现象),反应的离子方程式是____ 。
②向V中得到的棕褐色沉淀中滴加H2SO4溶液,加入催化剂,产生无色气泡,该气体是____ 。
(3)催化剂[Co(NH3)6]2+的失活与再生
①结合数据解释[Co(NH3)6]2+能被氧化为[Co(NH3)6]3+而失活的原因:____ 。
②根据以上实验,设计物质转化流程图实现[Co(NH3)6]2+的再生:____ 。
示例:Co CoCl2
CoCl2 Co(OH)2
Co(OH)2
 和
和 之间的相互转化。
之间的相互转化。资料:i.Ksp[Co(OH)2]=5.9×10-15,Ksp[Co(OH)3]=1.6×10-44
ii.Co2++6NH3
 [Co(NH3)6]2+K1=1.3×105
[Co(NH3)6]2+K1=1.3×105Co3++6NH3
 [Co(NH3)6]3+K2=2×1035
[Co(NH3)6]3+K2=2×1035iii.[Co(NH3)6]2+和[Co(NH3)6]3+在酸性条件下均能生成NH

(1)探究
 的还原性
的还原性实验I.粉红色的CoCl2溶液或CoSO4溶液在空气中久置,无明显变化。
实验II.向0.1mol/LCoCl2溶液中滴入2滴酸性KMnO4溶液,无明显变化。
实验III.按如图装置进行实验,观察到电压表指针偏转。

①甲同学根据实验III得出结论:Co2+可以被酸性KMnO4溶液氧化。
乙同学补充实验IV,
②探究碱性条件下
 的还原性,进行实验。
的还原性,进行实验。
ii中反应的化学方程式是
③根据氧化还原反应规律解释:还原性Co(OH)2>Co2+:Co2+-e-=Co3+在碱性条件下,OH-与Co2+、Co3+反应,使c(Co2+)和c(Co3+)均降低,但
(2)探究
 的氧化性
的氧化性①根据实验III和IV推测氧化性:Co3+>Cl2,设计实验证明:向V中得到的棕褐色沉淀中,
②向V中得到的棕褐色沉淀中滴加H2SO4溶液,加入催化剂,产生无色气泡,该气体是
(3)催化剂[Co(NH3)6]2+的失活与再生
①结合数据解释[Co(NH3)6]2+能被氧化为[Co(NH3)6]3+而失活的原因:
②根据以上实验,设计物质转化流程图实现[Co(NH3)6]2+的再生:
示例:Co
 CoCl2
CoCl2 Co(OH)2
Co(OH)2
您最近一年使用:0次
2022-05-08更新
|
1342次组卷
|
9卷引用:北京市西城区2022届高三第二次模拟测试化学试题
名校
9 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象与结论 | |
| A | 验证压强对化学平衡的影响 | 先将注射器充满NO2气体,然后将活塞往里推压缩体积 | 观察到注射器内气体颜色加深,证明加压平衡朝生成NO2气体的方向移动 |
| B | 铜的电解精炼 | 待精炼的铜和纯铜连接外加直流电源的阳极和阴极,用硫酸铜溶液作电解质电解 | 阳极上铜逐渐溶解,阴极上铜逐渐析出,硫酸铜溶液浓度保持不变 |
| C | 制备[Cu(NH3)4]SO4·H2O晶体 | 向4mL 0.1mol/LCuSO4溶液中滴加氨水,先形成难溶物,并继续滴加沉淀溶解,然后蒸发溶剂析出晶体 | 反应过程中,NH3的N给出孤对电子,Cu2+接受电子对,形成了稳定的配位键[Cu(NH3)4]2+ |
| D | 除去锅炉水垢中的CaSO4 | 先用碳酸钠溶液浸泡水垢,然后再用盐酸除去 | 利用Ksp(CaSO4)> Ksp(CaCO3),实现沉淀的转化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-21更新
|
406次组卷
|
4卷引用:3.4 配合物与超分子-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)
(已下线)3.4 配合物与超分子-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)浙江省富阳区第二中学2021-2022学年高二下学期(3月)检测化学试题 河北鸡泽县第一中学2021-2022学年高二下学期开学考试化学试题浙江省温州市2021-2022学年高二上学期期末教学质量统一检测化学试题
解题方法
10 . 工业盐酸(俗称粗盐酸)呈亮黄色,已证明了这是配合物 的颜色。请分析这种配合物的中心离子和配体,并用实验定性证明这种配合物只有在高浓度
的颜色。请分析这种配合物的中心离子和配体,并用实验定性证明这种配合物只有在高浓度 的条件下才是稳定的。
的条件下才是稳定的。___________
 的颜色。请分析这种配合物的中心离子和配体,并用实验定性证明这种配合物只有在高浓度
的颜色。请分析这种配合物的中心离子和配体,并用实验定性证明这种配合物只有在高浓度 的条件下才是稳定的。
的条件下才是稳定的。
您最近一年使用:0次



