解题方法
1 . 物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
| 选项 | 性质差异 | 结构因素 |
| A | 沸点:正戊烷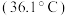 高于新戊烷 高于新戊烷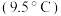 | 分子间作用力 |
| B | 熔点: | 晶体类型 |
| C | 酸性: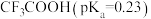 远强于 远强于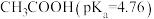 | 羟基极性 |
| D | 溶解度:甘油(丙三醇)与水互溶 | 分子间氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 根据下列实验操作和现象,得出的相应结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 乙醇和浓硫酸共热至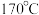 ,产生的气体使溴水褪色 ,产生的气体使溴水褪色 | 乙烯发生了加成反应 |
| B | 在 和 和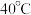 时,测得 时,测得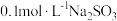 溶液的 溶液的 分别是9.66和9.37 分别是9.66和9.37 |  的水解程度随温度升高而增大 的水解程度随温度升高而增大 |
| C | 向 溶液中加入少量 溶液中加入少量 溶液,只有 溶液,只有 沉淀生成 沉淀生成 |  |
| D | 常温下,分别向无水乙醇和冰醋酸中加入大小相同的金属钠,前者反应更剧烈 | 分子中氢氧键的极性:乙醇 乙酸 乙酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . W、X、Y、Z为原子序数依次增大的短周期主族元素,基态W原子的s轨道电子数是p轨道电子数的2倍,X和Y形成的一种化合物是常用干燥剂,X、Z同主族且能构成如图所示的阴离子(R2—),下列说法正确的是


| A.简单离子半径:Z>Y>X | B.沸点:ZX2>WX2 |
| C.R2—中Z的化合价是—3 | D.第二电离能:Y>Z |
您最近一年使用:0次
4 . 氯化硼(BCl3)熔点为-107℃,沸点为12.5℃,其分子中键与键之间的夹角为120°,下列有关叙述错误的是
| A.氯化硼晶体属于离子晶体 |
| B.BCl3中B—Cl键的键长大于BF3中B—F键的键长 |
| C.氯化硼分子呈正三角形 |
| D.氯化硼分子属非极性分子 |
您最近一年使用:0次
5 .  可用于制备
可用于制备 (氟利昂的一种主要成分),制备方法如下:
(氟利昂的一种主要成分),制备方法如下:
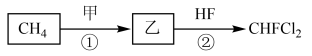
若甲为 ,下列说法不正确的是
,下列说法不正确的是
 可用于制备
可用于制备 (氟利昂的一种主要成分),制备方法如下:
(氟利昂的一种主要成分),制备方法如下:
若甲为
 ,下列说法不正确的是
,下列说法不正确的是| A.反应①的条件是光照 |
B.乙的结构式为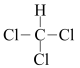 |
| C.反应②是取代反应 |
| D.上述流程中属于极性分子的有机物有3种 |
您最近一年使用:0次
6 . 氮化硼 是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到
是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到 和
和 ,如图所示。下列叙述正确的是
,如图所示。下列叙述正确的是

 是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到
是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到 和
和 ,如图所示。下列叙述正确的是
,如图所示。下列叙述正确的是
A.硼酸具有片层状结构,层与层之间, 单元间都以范德华力连接 单元间都以范德华力连接 |
| B.立方氮化硼结构与金刚石相似。立方氮化硼晶胞中每个氮原子周围有4个硼原子 |
C. 与 与 反应后再用氨气中和得到 反应后再用氨气中和得到 , , 含有配位键的数目为 含有配位键的数目为 |
D. 与 与 都是由极性键构成的极性分子 都是由极性键构成的极性分子 |
您最近一年使用:0次
2023-02-18更新
|
449次组卷
|
5卷引用:山东省蒙阴第一中学等5校2023届高三开学摸底联考化学试题
7 . 亚铁氰化钾属于欧盟批准使用的食品添加剂,受热易分解:3K4[Fe(CN)6] 12KCN+Fe3C+2(CN)2↑+N2↑+C,下列关于该反应说法错误的是
12KCN+Fe3C+2(CN)2↑+N2↑+C,下列关于该反应说法错误的是
 12KCN+Fe3C+2(CN)2↑+N2↑+C,下列关于该反应说法错误的是
12KCN+Fe3C+2(CN)2↑+N2↑+C,下列关于该反应说法错误的是| A.基态Fe2+的价层电子排布式为3d6 |
| B.N2和(CN)2均为非极性分子 |
| C.(CN)2分子中σ键和π键数目比为3∶4 |
| D.配合物K4[Fe(CN)6]中配位原子是氮原子 |
您最近一年使用:0次
8 . 已知A、B、C、D、E是原子序数依次增大且位于周期表中前四周期的元素,其中A、B、C是同一周期的非金属元素,化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构,AC2为非极性分子,B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高,E的基态原子中有6个未成对电子。下列说法正确的是
| A.A、B、C三种元素的第一电离能依次增大 |
| B.D的二价阳离子半径比C的阴离子半径大 |
| C.元素C与氢元素形成的化合物都是极性分子 |
D.E的基态原子的价层电子排布为 |
您最近一年使用:0次
解题方法
9 . 甲烷在一定条件下可生成碳正离子( )、碳负离子(
)、碳负离子( )、甲基(
)、甲基(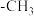 )和碳烯(
)和碳烯(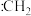 )等微粒。下列说法错误的是
)等微粒。下列说法错误的是
 )、碳负离子(
)、碳负离子( )、甲基(
)、甲基(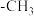 )和碳烯(
)和碳烯(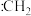 )等微粒。下列说法错误的是
)等微粒。下列说法错误的是A. 为非极性分子 为非极性分子 | B. 和 和 的空间结构均为平面三角形 的空间结构均为平面三角形 |
C.键角: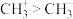 | D. 和 和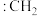 中碳原子杂化方式相同 中碳原子杂化方式相同 |
您最近一年使用:0次
解题方法
10 . (E)一丁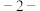 烯二醛的某种结构如图所示,关于该物质的下列说法错误的是
烯二醛的某种结构如图所示,关于该物质的下列说法错误的是

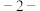 烯二醛的某种结构如图所示,关于该物质的下列说法错误的是
烯二醛的某种结构如图所示,关于该物质的下列说法错误的是
| A.分子间无法形成氢键 | B.分子中有9个 键和1个 键和1个 键 键 |
C.该分子在水中的溶解度大于 丁烯 丁烯 | D.该物质不存在顺反异构 |
您最近一年使用:0次

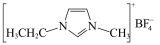 低于
低于


