解题方法
1 . X、Y、Z、W为原子序数依次增大的短周期元素,基态W原子有三种能量不同的电子,且电子数目之比为2∶2∶3,由四种元素可形成一种有机反应的强还原剂,其结构如图所示。下列说法错误的是
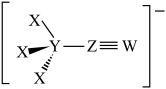
| A.简单氢化物还原性:Y>Z>W |
| B.分子极性:WX3>YX3 |
| C.W氢化物的沸点一定高于Z氢化物的沸点 |
| D.Y、Z的最高价氧化物的水化物均为弱酸 |
您最近半年使用:0次
2 . 下列有关超分子的说法错误的是
| A.超分子具有“分子识别”和“自组装”的特性 |
| B.分子以共价键聚合形成超分子 |
| C.超分子是由两种或多种分子形成的聚集体 |
| D.分子形成超分子的作用可能是分子间作用力 |
您最近半年使用:0次
解题方法
3 . 根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论不正确的是
实验目的 | 方案设计 | 现象 | 结论 | |
A | 验证NaCl、Na2SO4混合溶液中的Cl- | 取少量混合溶液于试管中,加入过量Ba(NO3)2溶液,静置,向上层清液中滴加稀硝酸酸化AgNO3溶液 | 若上层清液变浑浊 | 则混合溶液中含有Cl- |
B | 探究CF2Cl2分子的极性与非极性 | 用毛皮摩擦过的带电橡胶棒靠近CF2Cl2液流 | 液流方向改变 | CF2Cl2是极性分子 |
C | 比较HCOOH和H2S的酸性 | 分别测等物质的量浓度的HCOONH4和(NH4)2S溶液的pH | 前者的pH小 | 酸性:HCOOH>H2S |
D | 探究SO2和Fe3+的反应{已知[Fe(SO2)6]3+呈红棕色} | 将SO2气体通入FeCl3溶液中 | 溶液先变为红棕色,过一段时间又变成浅绿色 | SO2和Fe3+络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
4 . X、Y、Z、M、Q为5种前四周期原子序数逐渐增大的元素。X基态原子的核外电子只有1种运动状态,Y的最高能级中未成对电子数为3,Z的价层电子数是其能层数的3倍,Z与M上下相邻,Q+的价层电子轨道全充满。下列说法正确的是
| A.元素电负性:M>Q>X |
| B.X和Z可以形成既含极性键又含非极性键的极性分子 |
| C.简单氢化物的熔沸点:Y>Z>M |
D.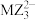 、 、 离子空间结构均为三角锥形 离子空间结构均为三角锥形 |
您最近半年使用:0次
名校
5 . 卤族元素形成物质种类众多,溴化碘(IBr)的化学性质与卤素相似。已知常温下,几种酸的电离常数:
 ,
, ;HClO
;HClO  。
。 和
和 均是化工中重要的化合物。已知
均是化工中重要的化合物。已知 的熔点是-107℃,
的熔点是-107℃, 的熔点是-40℃。下列说法正确的是
的熔点是-40℃。下列说法正确的是

 ,
, ;HClO
;HClO  。
。 和
和 均是化工中重要的化合物。已知
均是化工中重要的化合物。已知 的熔点是-107℃,
的熔点是-107℃, 的熔点是-40℃。下列说法正确的是
的熔点是-40℃。下列说法正确的是A.键角: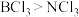 |
| B.两者均为极性分子 |
| C.两者在液态时均具有良好的导电性 |
D. 键能比 键能比 键能大, 键能大, 的熔点高于-40℃ 的熔点高于-40℃ |
您最近半年使用:0次
名校
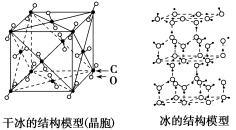
6 . 碳族元素的物质是化学世界中最庞大的家族,“天问一号”轨道飞行器近距离拍摄了火星北极,看到大量白色冰冻区域, 主要是二氧化碳低温凝结形成的干冰,虽然看起来和地球两极很像,但实际温度却比地球两极冷多了!
(1)已知 25℃时,H2CO3的Ka1=4.2×10-7、Ka2=4.8×10- 11,HCN的Ka=4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为___________ 。
(2)下列关于二氧化碳的说法正确的是___________。
(3)干冰和冰的晶体模型如下图存在差别的本质原因___________ 。___________ 。
(5)金刚石晶体中,每个C被___________ 个六元环共用。
(6)晶体硅和碳化硅熔点较高的是___________ (填化学式)。
(7)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为___________ 。
(1)已知 25℃时,H2CO3的Ka1=4.2×10-7、Ka2=4.8×10- 11,HCN的Ka=4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为
(2)下列关于二氧化碳的说法正确的是___________。
A.电子式为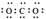 | B.空间填充模型为  |
| C.CO2 是极性分子, 能溶于水 | D.CO2 的水溶液能够导电,但 CO2是非电解质 |
(5)金刚石晶体中,每个C被
(6)晶体硅和碳化硅熔点较高的是
(7)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
您最近半年使用:0次
名校
解题方法
7 . 根据科学人员探测,在海洋深处的沉积物中含有可燃冰,主要成分是甲烷水合物。有关其组成的两种分子的下列说法正确的是
| A.它们之间以氢键结合在一起 | B.它们的中心原子杂化轨道类型相同 |
| C.它们都是极性键构成的极性分子 | D.它们的空间结构相同 |
您最近半年使用:0次
名校
解题方法
8 . 常温下,二氧化氯(ClO2)是一种黄绿色气体,具有强氧化性,其中心原子Cl为sp2杂化已被联合国卫生组织(WTO)列为Al级高效安全消毒剂,其中心原子Cl为sp2杂化。已知,工业上制备二氧化氯的方法之一是用甲醇在酸性条件下与氯酸钠反应,其反应的化学方程式:CH3OH+6NaClO3+3H2SO4=CO2↑+6ClO2↑+3Na2SO4+5H2O,则下列说法错误的是
| A.CO2是非极性分子 | B.键角: < < |
| C.CH3OH在反应中发生氧化反应 | D.ClO2分子空间构型为V形 |
您最近半年使用:0次
名校
解题方法
9 . 科学家已获得极具理论研究意义的N4分子,其结构为正四面体(如下图所示),与白磷分子相似。已知断裂1 mol N-N键吸收193 kJ热量 ,形成1 mol N≡N叁键放出941 kJ热量,则
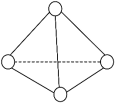
| A.N4分子中的N是sp2杂化 | B.N4是极性分子 |
| C.N4和N2互为同分异构体 | D.1 mol N4气体转化为N2时放出724 kJ 能量 |
您最近半年使用:0次
名校
10 . 下列对事实的分析正确的是
| 选项 | 事实 | 分析 |
| A | 键角: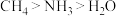 | 电负性:C<N<O |
| B | 第一电离能:P>S | 原子半径:P>S |
| C | 沸点:CO> | CO为极性分子, 为非极性分子 为非极性分子 |
| D | 热稳定性:HF>HCl | HF中存在氢键,HCl中不存在氢键 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



