名校
解题方法
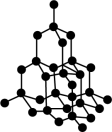
1 . 如图分别表示碘晶胞、硅晶体、 晶胞的结构,下列有关说法正确的是
晶胞的结构,下列有关说法正确的是

 晶胞的结构,下列有关说法正确的是
晶胞的结构,下列有关说法正确的是
| A.每个碘晶胞中含有14个碘分子 |
| B.在硅晶体中,硅原子与硅硅单键的个数之比为1∶2 |
C. 晶体中每个 晶体中每个 周围距离相等且最近的 周围距离相等且最近的 有6个 有6个 |
D.沸点:硅晶体> >碘 >碘 |
您最近一年使用:0次
2 . 中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
下列关于金刚石、石墨、石墨炔的说法正确的是
金刚石 |
石墨 |
石墨炔 |
| A.金刚石中最小环为六元环,通过旋转单键,六元环中六个碳可以在同一平面上 |
| B.石墨晶体中存在共价键、分子间作用力、离子键等多种类型作用力 |
| C.等质量的石墨和金刚石中碳碳σ键数目之比为3:4 |
| D.三种物质均能导电 |
您最近一年使用:0次
3 . 部分晶体及分子结构如图所示,下列说法正确的是
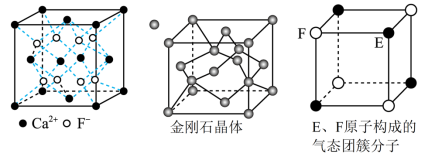

| A.CaF2晶胞中有8个F-,F-配位数是4 |
| B.金刚石晶体中每个碳原子被6个六元环共用,每个六元环最多有4个碳原子共面 |
| C.该气态团簇分子的分子式为E4F4或F4E4 |
| D.三种物质对应的晶体熔沸点最高的是CaF2 |
您最近一年使用:0次
4 . 下列说法正确的是
| A.BF3、NCl3中各原子的最外层电子都满足8电子稳定结构 |
| B.基态57La(镧)原子的价层电子排布式为5d16s2,位于元素周期表的d区 |
| C.CH3OH分子中,碳原子与氧原子之间的共价键为sp3-pσ键 |
| D.6g二氧化硅晶体中含有的Si-O键数为0.4 NA |
您最近一年使用:0次
5 . 下图所示的几种碳单质,关于它们的说法错误的是
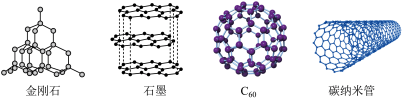

| A.四种碳单质互为同素异形体,其中石墨和碳纳米管均可导电 |
B.金刚石晶体中每个 原子被6个六元环所共用 原子被6个六元环所共用 |
C. 石墨晶体中含有的六元环的数目为 石墨晶体中含有的六元环的数目为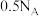 |
D. 晶体中每个 晶体中每个 分子周围与它最近且等距的 分子周围与它最近且等距的 分子有12个 分子有12个 |
您最近一年使用:0次
6 . 氮化硼(BN)可形成类似石墨的平面六角形层状结构a,在一定条件下a可转化为类似金刚石的立方氮化硼b,如图所示。下列说法错误的是


A.第一电离能: |
| B.a、b两种晶体硬度和熔点均不同 |
| C.a、b中所有化学键均为极性键,二者中B原子的杂化方式不同 |
D.a、b中每个B原子分别被m、n个六元环共有,则 |
您最近一年使用:0次
解题方法
7 . 下列关于“碳”的说法错误的是
A.自然界中的14C来自宇宙射线(中子)撞击14N,其过程可表示为 |
| B.高压下制得的CO2共价晶体结构与SiO2晶体相似,其硬度和熔沸点均高于SiO2晶体 |
| C.石墨烯、石墨炔都是全碳二维平面结构材料,二者碳原子杂化方式完全相同 |
| D.用风能、光能等清洁能源代替煤和石油,有利于实现“双碳”目标 |
您最近一年使用:0次
名校
8 . 下列关于共价晶体、分子晶体的叙述中,不正确的是
A.在 晶体中,1个硅原子和4个氧原子形成4个共价键 晶体中,1个硅原子和4个氧原子形成4个共价键 |
| B.混合晶体石墨的熔点高于金刚石 |
C. 的相对分子质量大于 的相对分子质量大于 ,所以 ,所以 的沸点高于 的沸点高于 |
| D.金刚石为网状结构,由共价键形成的碳原子环中,最小环上最多4个碳原子共面 |
您最近一年使用:0次
名校
解题方法
9 . 硅是构成矿物和岩石的主要成分,单质硅及其化合物具有广泛的用途。
(1)某些硅酸盐具有筛选分子的功能。一种硅酸盐的组成为:M2O·R2O3·2SiO2·nH2O,已知元素M、R均位于元素周期表的第3周期,两元素原子的质子数之和为24。
①写出R原子核外能量最高的电子的电子排布式:___________ 。
②常温下,不能与R单质发生反应的是___________ (选填序号)。
a.CuCl2溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)氮化硅(Si3N4)陶瓷材料硬度大、熔点高,不溶于水。可由下列反应制得:SiO2+C+N2 Si3N4+CO
Si3N4+CO
①C3N4的结构与Si3N4相似,请比较二者熔点高低,并说明理由:___________ 。
②配平上述反应的化学方程式:___________ 。
(3)一种用工业硅(含少量铁、铜等金属的氧化物)制备Si3N4的主要流程如下:
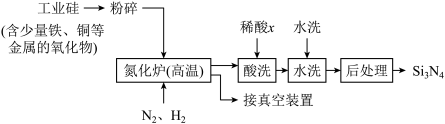
适量的H2是为了排尽设备中的空气,但H2在高温下也能还原工业硅中的某些金属化物。x可能是___________ (选填:“盐酸”“硝酸”或“硫酸”),理由是___________ 。
(1)某些硅酸盐具有筛选分子的功能。一种硅酸盐的组成为:M2O·R2O3·2SiO2·nH2O,已知元素M、R均位于元素周期表的第3周期,两元素原子的质子数之和为24。
①写出R原子核外能量最高的电子的电子排布式:
②常温下,不能与R单质发生反应的是
a.CuCl2溶液 b.Fe2O3 c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
(2)氮化硅(Si3N4)陶瓷材料硬度大、熔点高,不溶于水。可由下列反应制得:SiO2+C+N2
 Si3N4+CO
Si3N4+CO①C3N4的结构与Si3N4相似,请比较二者熔点高低,并说明理由:
②配平上述反应的化学方程式:
(3)一种用工业硅(含少量铁、铜等金属的氧化物)制备Si3N4的主要流程如下:

适量的H2是为了排尽设备中的空气,但H2在高温下也能还原工业硅中的某些金属化物。x可能是
您最近一年使用:0次
10 . 下列叙述中正确的个数是
①s−s σ键与s−p σ键的电子云形状相同
②CHCl=CH2分子中,C−Cl键采用的成键轨道是sp2−p
③基态C原子的电子排布图:
④若将基态15P原子的核外电子排布式写成1s22s22p63s23p 3p
3p ,则违背了洪特规则
,则违背了洪特规则
⑤处于最低能量状态原子叫基态原子,1s22s22p →1s22s22p
→1s22s22p 形成的是吸收光谱
形成的是吸收光谱
⑥冠醚可识别碱金属离子,冠醚与碱金属离子之间形成的配位键属于离子键
⑦含2.4g碳原子的金刚石晶体中共价键个数为0.4NA
⑧31g白磷中含有的孤电子对数为NA
①s−s σ键与s−p σ键的电子云形状相同
②CHCl=CH2分子中,C−Cl键采用的成键轨道是sp2−p
③基态C原子的电子排布图:

④若将基态15P原子的核外电子排布式写成1s22s22p63s23p
 3p
3p ,则违背了洪特规则
,则违背了洪特规则⑤处于最低能量状态原子叫基态原子,1s22s22p
 →1s22s22p
→1s22s22p 形成的是吸收光谱
形成的是吸收光谱⑥冠醚可识别碱金属离子,冠醚与碱金属离子之间形成的配位键属于离子键
⑦含2.4g碳原子的金刚石晶体中共价键个数为0.4NA
⑧31g白磷中含有的孤电子对数为NA
| A.3 | B.4 | C.5 | D.6 |
您最近一年使用:0次