1 . 锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]____ ,有____ 个未成对电子。
(2)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因________________________________ 。
(3)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是____________ 。
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为____ ,微粒之间存在的作用力是____ 。
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(1/2,0,1/2);C为(1/2,1/2,0)。则D原子的坐标参数为____ 。
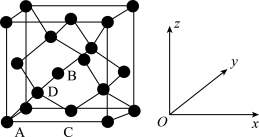
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a pm,其密度为_________ g·cm-3(列出计算式即可)。
(1)基态Ge原子的核外电子排布式为[Ar]
(2)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(3)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(1/2,0,1/2);C为(1/2,1/2,0)。则D原子的坐标参数为

②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a pm,其密度为
您最近半年使用:0次
2 . X是核外电子数最少的元素,Y是地壳中含量最丰富的元素,Z在地壳中的含量仅次于Y,W可以形成自然界中最硬的原子晶体。下列叙述错误的是( )
| A.WX4是沼气的主要成分 | B.固态X2Y是分子晶体 |
| C.W可以形成原子晶体 | D.玛瑙、水晶和玻璃的成分都是ZY2 |
您最近半年使用:0次
3 . (1)请将下列变化过程中破坏的微粒间作用力名称的编号填在横线上:
A.共价键 B.离子键 C.金属键 D.分子间作用力
①氢氧化钠熔化_____ ;②干冰升华_____ ;
③二氧化硅熔化_____ ;④钠熔化_____ 。
(2)单质硼有无定形和晶体两种,参考下表数据。
①根据表中数据判断晶体硼的晶体类型属于_______ 晶体;
②请解释金刚石的熔沸点高于晶体硅的原因是_________ 。
A.共价键 B.离子键 C.金属键 D.分子间作用力
①氢氧化钠熔化
③二氧化硅熔化
(2)单质硼有无定形和晶体两种,参考下表数据。
| 金刚石 | 晶体硅 | 晶体硼 | |
| 熔点(K) | >3823 | 1683 | 2573 |
| 沸点(K) | 5100 | 2628 | 2823 |
| 硬度 | 10 | 7.0 | 9.5 |
①根据表中数据判断晶体硼的晶体类型属于
②请解释金刚石的熔沸点高于晶体硅的原因是
您最近半年使用:0次
4 . 下列有关晶体的叙述中,正确的是( )
| A.氯化钠和氯化铯晶体中,阳离子的配位数均为6 |
| B.金刚石为三维网状结构,由碳原子以sp3杂化轨道形成共价键 |
| C.金属钠的晶体采用体心立方堆积,每个晶胞含2个原子,配位数为8 |
| D.干冰晶体中,每个CO2分子周围紧邻8个CO2分子 |
您最近半年使用:0次
名校
5 . 下列有关性质的比较中,正确的是
| A.硬度:白磷>冰>二氧化硅;在水中的溶解度:NH3> CO2> SO2 >H2 |
| B.非金属性:N>O>P>S;碱性:KOH>NaOH>Al(OH)3>Ca(OH)2 |
| C.共价键的键能:硅>碳化硅>金刚石;晶格能:CsCl >NaCl> CaO |
| D.氢键强弱:N···H<O···H<F···H;范德华力强弱:NH3< PH3< AsH3 |
您最近半年使用:0次
2019-07-15更新
|
221次组卷
|
3卷引用:宁夏银川一中2018-2019学年高二下学期期末考试化学试题
名校
6 . 下面有关晶体的叙述中,不正确的是
| A.氯化铯晶体中,每个Cs+周围紧邻8个Cl- |
| B.SiO2晶体为空间网状结构,由共价键形成的原子环中,最小的环上有12个原子 |
| C.干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |
| D.金属铜属于六方最密堆积结构,金属镁属于面心立方最密堆积结构 |
您最近半年使用:0次
7 . 根据下表给出的几种物质的熔沸点数据,判断下列说法中错误的是
晶体 | NaCl | MgCl2 | AlCl3 | SiCl4 | 单质R |
熔点/℃ | 801 | 714 | 190 | -70 | 2300 |
沸点/℃ | 1465 | 1418 | 177.8 | 57 | 2500 |
| A.SiCl4 和A1Cl3都是分子晶体 ,熔融状态下不导电 |
| B.MgCl2和NaCl都是离子晶体,熔融状态能导电且易溶于水 |
| C.若单质R是原子晶体,其熔沸点的高低是由共价键的键能决定的 |
| D.固态时可导电的一定是金属晶体 |
您最近半年使用:0次
8 . 下列有关化学用语使用正确的是
A.基态碳原子的价电子轨道表示式为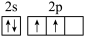 |
B.NH4Cl 的电子式: 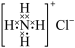 |
| C.Br原子的基态简化电子排布式为4s24p5 |
| D.石英的分子式:SiO2 |
您最近半年使用:0次
2019-07-15更新
|
139次组卷
|
2卷引用:宁夏银川一中2018-2019学年高二下学期期末考试化学试题
9 . 干冰、石墨、C60、氟化钙和金刚石的结构模型如图所示(石墨仅表示出其中的一层结构):
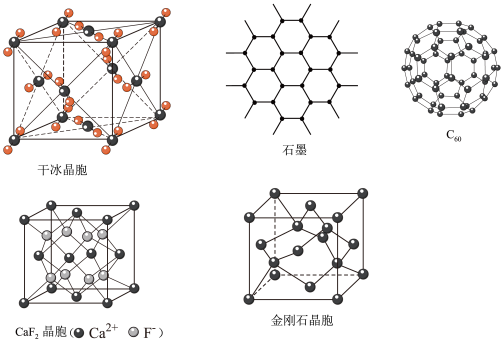
回答下列问题:
(1)干冰晶胞中,每个CO2分子周围有________ 个与之紧邻且等距的CO2分子。
(2)由金刚石晶胞可知,每个金刚石晶胞占有________ 个碳原子。
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是________ 。
(4)在CaF2晶体中,Ca2+的配位数是________ ,F-的配位数是________ 。
(5)固态时,C60属于________ (填“原子”或“分子”)晶体。

回答下列问题:
(1)干冰晶胞中,每个CO2分子周围有
(2)由金刚石晶胞可知,每个金刚石晶胞占有
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是
(4)在CaF2晶体中,Ca2+的配位数是
(5)固态时,C60属于
您最近半年使用:0次
10 . 下面的排序中,不正确 的是
| A.熔点由高到低:Rb>K>Na |
| B.熔点由高到低:GeH4>SiH4>CH4 |
| C.硬度由大到小:金刚石>碳化硅>晶体硅 |
| D.晶格能由大到小: AlF3>MgF2>NaF |
您最近半年使用:0次



