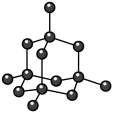
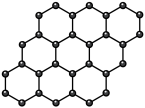
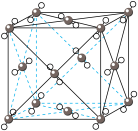
1 . 观察下列模型,判断下列说法错误的是
金刚石 | 碳化硅 | 二氧化硅 | 石墨烯 | 干冰 |
|
|
|
|
|
| A.原子数相同的金刚石和碳化硅,共价键个数之比为1∶2 |
B. 晶体中Si和Si-O键个数比为1∶4 晶体中Si和Si-O键个数比为1∶4 |
| C.石墨烯中碳原子和六元环个数比为2∶1 |
| D.干冰晶体堆积属于分子密堆积 |
您最近一年使用:0次
解题方法
2 . 下列元素或化合物的性质变化顺序不正确 的是
A.共价键的极性: |
B.元素的第一电离能: |
C.卤素单质的熔点: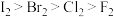 |
| D.共价键的键能:金刚石>碳化硅>晶体硅 |
您最近一年使用:0次
3 . 最近我国科学家预测并据此合成了新型碳材料:T-碳。可以看作金刚石结构中的一个碳原子被四个碳原子构成的一个正四面体结构单元替代(如图所示,所有小球都代表碳原子)。下列说法正确的是
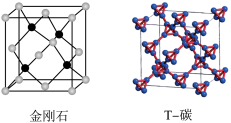

| A.T-碳晶胞中含16个碳原子 |
| B.T-碳与石墨、金刚石互为同分异构体 |
| C.T-碳晶体和金刚石晶体中含有的化学键不同 |
| D.T-碳晶体与金刚石晶体类似,熔点高硬度大 |
您最近一年使用:0次
2023-05-03更新
|
266次组卷
|
3卷引用:福建省宁德市一级达标校五校联合体2022-2023学年高二下学期4月期中考试化学试题
解题方法
4 . 根据下列物质的性质判断为原子晶体的是
A.微溶于水,硬度小,熔点 ,固体或液体不导电 ,固体或液体不导电 |
B.熔点 ,电的良导体,加压可变形 ,电的良导体,加压可变形 |
C.熔点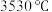 ,不导电,不溶于水和有机溶剂,硬度大 ,不导电,不溶于水和有机溶剂,硬度大 |
D.熔点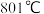 ,易溶于水,熔化时导电 ,易溶于水,熔化时导电 |
您最近一年使用:0次
名校
解题方法
5 . 下列对一些实验事实的理论解释正确的是
| 选项 | 实验事实 | 理论解释 |
| A | CsCl晶体中阳离子和阴离子都有确定的配位数 | 离子键具有饱和性 |
| B | 环状 分子结构如图 分子结构如图 | 原子采取的杂化方式为 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-06-30更新
|
181次组卷
|
2卷引用:福建省福州第一中学2021-2022学年高二下学期期中考试化学试题
解题方法
6 . 观察下列模型并结合有关信息,判断下列说法正确的是
| 干冰 | BN | SiO2 | NaCl | |
| 结构模型示意图 | 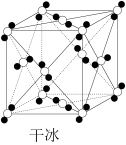 | 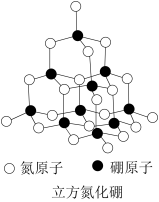 |  | 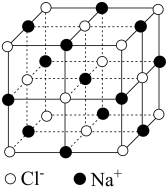 |
| A.44g干冰中含有NA个晶胞结构单元 |
| B.立方氮化硼含有σ键和π键,所以硬度大 |
| C.SiO2晶体和NaCl晶体中微粒的排列方式均为紧密堆积形式 |
| D.NaCl晶体中每个Na+周围距离相等且最近的Na+有12个 |
您最近一年使用:0次
7 . 下列关于晶体结构和性质的叙述错误的是


A.在 晶体中,Cs+的配位数为8 晶体中,Cs+的配位数为8 |
B.在 晶体中,距Na+最近的Cl-形成正八面体 晶体中,距Na+最近的Cl-形成正八面体 |
| C.干冰晶体中,每个CO2分子周围紧邻6个CO2分子 |
D.在二氧化硅晶体中,平均每个 原子形成4个 原子形成4个 键,且每个Si被12个环共用 键,且每个Si被12个环共用 |
您最近一年使用:0次
2022-04-25更新
|
160次组卷
|
2卷引用:福建省南安市侨光中学、昌财实验中学2021-2022学年高二下学期第4次联考(期中)化学试题
名校
解题方法
8 . 下列各物质中,按熔点由高到低的顺序排列正确的是
| A.CH4>SiH4>GeH4>SnH4 | B.KCl>NaCl>MgCl2>MgO |
| C.SiCl4>MgBr2>BN | D.金刚石>晶体硅>钠 |
您最近一年使用:0次
2022-04-25更新
|
118次组卷
|
3卷引用:福建省南安市侨光中学、昌财实验中学2021-2022学年高二下学期第4次联考(期中)化学试题
解题方法
9 . 下列说法正确的是
| 物质 | 氧化铝 | 氯化铝 |
| 沸点/K | 2323 | 455.7 |
| A.氧化铝、氯化铝沸点相差极大,如表所示,是因为它们的晶体类型不同 |
B. 晶体中存在Na原子和氯原子 晶体中存在Na原子和氯原子 |
C.水从液态变成气态, 键断裂 键断裂 |
| D.同一主族的C和Si的最高价氧化物晶体类型相同,熔沸点相差不大 |
您最近一年使用:0次
解题方法
10 . 下列各物质的熔点按由高到低的顺序排列的是
A.   | B. K Ca K Ca |
C.Si   | D.金刚石 硫磺 干冰 |
您最近一年使用:0次