名校
解题方法
1 . 碳族中的碳、硅、锗及其化合物在多领域有重要用途。
(1)基态 的电子排布式为
的电子排布式为___________ 。
(2)我国科学家研发的“液态阳光”计划是通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。 分子中存在
分子中存在___________ 个 键和
键和___________ 个 键,
键, 分子是
分子是___________ 分子(填“极性”或“非极性”)。
(3)关于 、
、 及其化合物的结构与性质,下列论述
及其化合物的结构与性质,下列论述不正确 的是___________。
(4) 与
与 -甲基咪唑(
-甲基咪唑(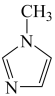 )反应可以得到
)反应可以得到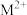 ,其结构如下图所示:
,其结构如下图所示:

 -甲基咪唑中碳原子的杂化轨道类型有
-甲基咪唑中碳原子的杂化轨道类型有___________ 。
(5)汞( )、锗(
)、锗( )、锑(
)、锑( )形成的一种新物质
)形成的一种新物质 为潜在的拓扑绝缘体材料。
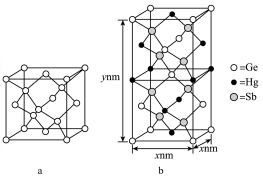
为潜在的拓扑绝缘体材料。 的晶体(晶胞为下图
的晶体(晶胞为下图 )可视为
)可视为 晶体(晶胞为下图
晶体(晶胞为下图 )中部分
)中部分 原子被
原子被 和
和 取代后形成。
取代后形成。
 的最简式的相对分子质量为
的最简式的相对分子质量为 ,阿伏加德罗常数的数值为
,阿伏加德罗常数的数值为 ,则
,则 晶体的密度为
晶体的密度为___________  (列出计算式)。注:
(列出计算式)。注:
(1)基态
 的电子排布式为
的电子排布式为(2)我国科学家研发的“液态阳光”计划是通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。
 分子中存在
分子中存在 键和
键和 键,
键, 分子是
分子是(3)关于
 、
、 及其化合物的结构与性质,下列论述
及其化合物的结构与性质,下列论述A.键能 、 、 ,因此 ,因此 稳定性小于 稳定性小于 |
B. 是与金刚石结构相似的共价晶体,因此 是与金刚石结构相似的共价晶体,因此 具有较高的硬度 具有较高的硬度 |
C. 中 中 的化合价为 的化合价为 , , 中 中 的化合价为 的化合价为 ,因此 ,因此 还原性小于 还原性小于 |
D. 原子间难形成双键和三键而 原子间难形成双键和三键而 原子间可以,是因为 原子间可以,是因为 的原子半径大于 的原子半径大于 ,因此难以形成 ,因此难以形成 键 键 |
 与
与 -甲基咪唑(
-甲基咪唑( )反应可以得到
)反应可以得到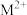 ,其结构如下图所示:
,其结构如下图所示:
 -甲基咪唑中碳原子的杂化轨道类型有
-甲基咪唑中碳原子的杂化轨道类型有(5)汞(
 )、锗(
)、锗( )、锑(
)、锑( )形成的一种新物质
)形成的一种新物质 为潜在的拓扑绝缘体材料。
为潜在的拓扑绝缘体材料。 的晶体(晶胞为下图
的晶体(晶胞为下图 )可视为
)可视为 晶体(晶胞为下图
晶体(晶胞为下图 )中部分
)中部分 原子被
原子被 和
和 取代后形成。
取代后形成。
 的最简式的相对分子质量为
的最简式的相对分子质量为 ,阿伏加德罗常数的数值为
,阿伏加德罗常数的数值为 ,则
,则 晶体的密度为
晶体的密度为 (列出计算式)。注:
(列出计算式)。注:
您最近一年使用:0次
2 . 据古籍《燕闲清赏笺》记载:“宣窑之青,乃苏勃泥青”,说明宣德时期青花瓷使用的颜料是“苏勃泥青”,它是从一种钻毒砂[主要成分:( ,
, )
) ]中提取出来的。回答下列问题:
]中提取出来的。回答下列问题:
(1)基态S原子的价层电子排布图为_______ ,其原子核外电子共有_______ 种空间运动状态。
(2)比较元素第一电离能:S_______ P(填“>”、“<”或=)。
(3) 位于周期表的第
位于周期表的第_______ 周期 _______ 族,_______ (填“d”或“ds”)区。
(4)区分晶体与非晶体最可靠的科学方法是_______ 。
(5)砷化镓晶胞结构如图所示。晶胞中 与周围最近且等距的
与周围最近且等距的 形成的空间结构为
形成的空间结构为_______ 。已知 晶胞棱长为apm,其密度
晶胞棱长为apm,其密度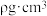 ,则阿伏加德罗常数的数值为
,则阿伏加德罗常数的数值为_______ (列出计算式即可, 的摩尔质量为
的摩尔质量为 )。
)。

(6) 的熔点为
的熔点为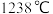 ,
, 与
与 晶体类型相同,
晶体类型相同, 的熔点
的熔点_______ (填“>”、“<”或“=”)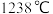 。
。
 ,
, )
) ]中提取出来的。回答下列问题:
]中提取出来的。回答下列问题:(1)基态S原子的价层电子排布图为
(2)比较元素第一电离能:S
(3)
 位于周期表的第
位于周期表的第(4)区分晶体与非晶体最可靠的科学方法是
(5)砷化镓晶胞结构如图所示。晶胞中
 与周围最近且等距的
与周围最近且等距的 形成的空间结构为
形成的空间结构为 晶胞棱长为apm,其密度
晶胞棱长为apm,其密度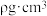 ,则阿伏加德罗常数的数值为
,则阿伏加德罗常数的数值为 的摩尔质量为
的摩尔质量为 )。
)。
(6)
 的熔点为
的熔点为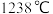 ,
, 与
与 晶体类型相同,
晶体类型相同, 的熔点
的熔点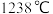 。
。
您最近一年使用:0次
名校
解题方法
3 . 如图所示,NaCl是一种重要的化工原料,可以制备一系列物质。以下是钠法(液氨法)制备NaN3的工艺流程:

(1)工业可通过电解熔融NaCl制得金属钠,请写出电解时阳极的电极反应式:____ 。
(2)用电子式表示NH3分子的形成过程____ 。
(3)工业上在210-220℃合成NaN3,请写出该合成反应的化学方程式____ 。
(4)NaN3是一种易溶于水、有爆炸性的白色固体,销毁NaN3可用NaClO溶液,该销毁反应的离子方程式为____ ( 被氧化为N2)。
被氧化为N2)。
(5)生成过程中产生的Cl2、H2用途广泛,其中可用于生产高纯硅。
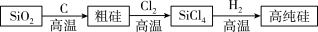
①硅元素位于周期表第____ 周期____ 族。
②SiO2熔点1723℃,质地硬而脆;SiCl4常温下为液体,易挥发。请根据性质推断SiO2属于____ 晶体,SiCl4晶体微粒间的作用力为____ 。

(1)工业可通过电解熔融NaCl制得金属钠,请写出电解时阳极的电极反应式:
(2)用电子式表示NH3分子的形成过程
(3)工业上在210-220℃合成NaN3,请写出该合成反应的化学方程式
(4)NaN3是一种易溶于水、有爆炸性的白色固体,销毁NaN3可用NaClO溶液,该销毁反应的离子方程式为
 被氧化为N2)。
被氧化为N2)。(5)生成过程中产生的Cl2、H2用途广泛,其中可用于生产高纯硅。

①硅元素位于周期表第
②SiO2熔点1723℃,质地硬而脆;SiCl4常温下为液体,易挥发。请根据性质推断SiO2属于
您最近一年使用:0次
名校
解题方法
4 . 结构决定性质,研究物质的组成、结构对于学习物质的性质至关重要。
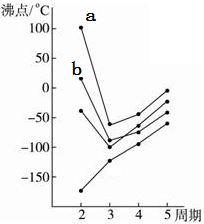
(1)如图中每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点、b点分别代表的是___________ 、___________ (写化学式),a比b的沸点高的原因是__________________________________ 。
(2)在超高压下,科学家用激光器将CO2加热到1800K,成功制得了类似石英的CO2原子晶体。由此推测该CO2晶体中O—C—O键角为__________ ,与石英相比该晶体的熔点、沸点________ (“更高”或“更低”),理由是_________________________________ 。
(3)利用铜萃取剂M可通过如下反应实现铜离子的富集:

①M所含元素的电负性由大到小顺序为____ ,其中氮原子以__ 轨道与氧原子形成σ键。
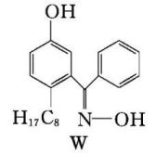
②M与W(右图)相比,M的水溶性较小,更利于Cu2+的萃取。M水溶性较小的主要原因是___________________________________ 。
(4)常用 表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为
表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为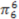 。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为
。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为________ ,吡咯分子中N原子的杂化类型为 ________ ,1mol吡咯分子中所含的σ键数目为________ 。

(1)如图中每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点、b点分别代表的是

(2)在超高压下,科学家用激光器将CO2加热到1800K,成功制得了类似石英的CO2原子晶体。由此推测该CO2晶体中O—C—O键角为
(3)利用铜萃取剂M可通过如下反应实现铜离子的富集:


①M所含元素的电负性由大到小顺序为
②M与W(右图)相比,M的水溶性较小,更利于Cu2+的萃取。M水溶性较小的主要原因是
(4)常用
 表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为
表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为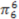 。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为
。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为
您最近一年使用:0次



