2023·湖南衡阳·三模
1 . 73号元素钽(Ta)与砷(As)形成的晶体在室温下拥有超高的空穴迁移率和较低的电子迁移率,其长方体晶胞结构如图所示。下列说法错误的是
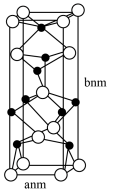

| A.基态As原子核外N层有4种空间运动状态不同的电子 |
| B.该晶胞中As的配位数为4 |
| C.该晶体的化学式为TaAs |
D.TaAs的晶体密度 |
您最近一年使用:0次
2 . 冰晶石 晶胞结构如图甲所示,Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示。下列说法错误的是
晶胞结构如图甲所示,Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示。下列说法错误的是
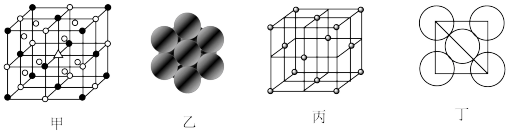
 晶胞结构如图甲所示,Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示。下列说法错误的是
晶胞结构如图甲所示,Al单质的晶体中原子的堆积方式如图乙所示,其晶胞特征如图丙所示,原子之间相互位置关系的平面图如图丁所示。下列说法错误的是
| A.甲图中大立方体的体心处小三角“△”所代表的应该是“小白球” |
| B.Al晶胞中Al原子的配位数为12 |
C.若已知Al的原子半径为dcm, 代表阿伏加德罗常数,Al的相对原子质量为M,Al晶体的密度为 代表阿伏加德罗常数,Al的相对原子质量为M,Al晶体的密度为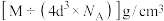 |
D. 中含有离子键、配位键 中含有离子键、配位键 |
您最近一年使用:0次
名校
解题方法
3 . 硒化锌是一种重要的半导体材料;其晶胞结构如图甲所示,已知晶胞参数为pnm,乙图为晶胞的俯视图,下列说法正确的是
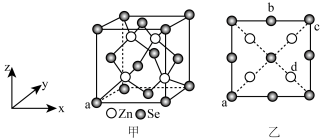
| A.晶胞中硒原子的配位数为12 |
B.晶胞中d点原子分数坐标为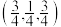 |
C.相邻两个Zn原子的最短距离为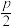 nm nm |
| D.电负性:Zn>Se |
您最近一年使用:0次
2023-03-03更新
|
1862次组卷
|
11卷引用:山东省德州市第一中学2022-2023学年高二下学期3月月考化学试题
山东省德州市第一中学2022-2023学年高二下学期3月月考化学试题河南省郑州市六校联盟2022-2023学年高二下学期4月期中考试化学试题(已下线)专题十 晶胞示意图(练)河北省张家口市宣化第一中学2023届高三模拟试题(三)化学试题河南省驻马店市环际大联考2022-2023学年高二下学期4月期中考试化学试题(已下线)热点08 金属晶体和离子晶体山东省临沂市第二十四中学2023-2024学年高二下学期3月学科素养水平监测化学试题山东省济宁市2023届高三一模考试(3月)化学试题(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(选择题11-15)福建省龙岩市连城县第一中学2022-2023学年高二下学期5月月考化学试题山东省烟台市第一中学2023-2024学年高三下学期3月月考化学试题
解题方法
4 . NiO晶体与NaCl具有相同晶胞结构。在一定温度下,NiO晶体可以自发地分散并形成“单分子层”(如图所示),可以认为 作密置单层排列,
作密置单层排列, 填充其中。设
填充其中。设 为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 半径为r pm。下列说法错误的是
半径为r pm。下列说法错误的是
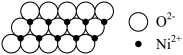
 作密置单层排列,
作密置单层排列, 填充其中。设
填充其中。设 为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 半径为r pm。下列说法错误的是
半径为r pm。下列说法错误的是
| A.Ni位于元素周期表第4周期第Ⅷ族 |
B.NiO晶体中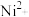 、 、 的配位数均为6 的配位数均为6 |
| C.NiO晶胞中八面体空隙与四面体空隙比为1:2 |
D.该“单分子层”面积密度为 |
您最近一年使用:0次
2022-07-25更新
|
978次组卷
|
3卷引用:第三章 晶体结构与性质(B卷·能力提升练)-2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修2)
名校
解题方法
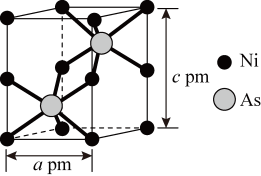
5 . 红砷镍是一种六方晶体(底面为 和
和 的菱形),其晶胞如图所示。下列说法错误的是
的菱形),其晶胞如图所示。下列说法错误的是
 和
和 的菱形),其晶胞如图所示。下列说法错误的是
的菱形),其晶胞如图所示。下列说法错误的是
A.晶胞中 原子个数为2 原子个数为2 |
B.红砷镍晶体的化学式为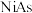 |
C.晶胞中 周围距离最近且等距的 周围距离最近且等距的 有6个 有6个 |
D. 和 和 间的最短距离为 间的最短距离为 |
您最近一年使用:0次
2021-04-24更新
|
1335次组卷
|
5卷引用:吉林省长春市“BEST合作体”2020-2021学年高二下学期期中化学试题
吉林省长春市“BEST合作体”2020-2021学年高二下学期期中化学试题辽宁省实验中学2022届高三第一次阶段性考试化学试题(已下线)第十二章 物质结构与性质(测)-2023年高考化学一轮复习讲练测(全国通用)湖北省第六届2021届高三(4月)调研模拟考试化学试题湖北省宜昌英杰学校2022-2023学年高二3月月考化学试题
解题方法
6 . 金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)NiO、FeO的晶体结构类型均与氯化钠的相同, 和
和 的半径分别为69pm和78pm,则熔点NiO
的半径分别为69pm和78pm,则熔点NiO___________ FeO(填“<”或“>”)。
(2)NiO晶胞中 和
和 的配位数分别为
的配位数分别为___________ 、___________ 。
(3)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构如图所示。该合金的化学式为___________ 。

(4)已知该晶胞的摩尔质量为Mg/mol,密度为 。设
。设 为阿伏加德罗常数的值,则该晶胞的体积是
为阿伏加德罗常数的值,则该晶胞的体积是___________  (用含M、d、
(用含M、d、 的代数式表示)。
的代数式表示)。
(5)该晶体内部具有空隙,且每个晶胞的空隙中储存6个氢原子时比较稳定。已知: ,
, ;标准状况下氢气的密度为
;标准状况下氢气的密度为 ;储氢能力=
;储氢能力= 。若忽略储氢前后晶胞的体积变化,则该储氢材料的储氢能力为
。若忽略储氢前后晶胞的体积变化,则该储氢材料的储氢能力为___________ 。
(1)NiO、FeO的晶体结构类型均与氯化钠的相同,
 和
和 的半径分别为69pm和78pm,则熔点NiO
的半径分别为69pm和78pm,则熔点NiO(2)NiO晶胞中
 和
和 的配位数分别为
的配位数分别为(3)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构如图所示。该合金的化学式为

(4)已知该晶胞的摩尔质量为Mg/mol,密度为
 。设
。设 为阿伏加德罗常数的值,则该晶胞的体积是
为阿伏加德罗常数的值,则该晶胞的体积是 (用含M、d、
(用含M、d、 的代数式表示)。
的代数式表示)。(5)该晶体内部具有空隙,且每个晶胞的空隙中储存6个氢原子时比较稳定。已知:
 ,
, ;标准状况下氢气的密度为
;标准状况下氢气的密度为 ;储氢能力=
;储氢能力= 。若忽略储氢前后晶胞的体积变化,则该储氢材料的储氢能力为
。若忽略储氢前后晶胞的体积变化,则该储氢材料的储氢能力为
您最近一年使用:0次
名校
解题方法
7 . 金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)Ni原子的核外电子排布式为___________ ,该元素位于元素周期表的第___________ 族___________ 区。
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO___________ FeO(填“<”或“>”);
(3)NiO晶胞中Ni和O的配位数分别为___________ 、___________ ;
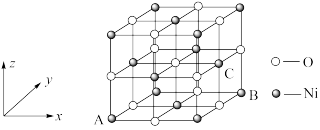
(4)NiO的晶体结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为___________ 。
(5)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图所示。

①该结构中,碳碳之间的共价键类型是σ键,碳氮之间的共价键类型是___________ ,氮镍之间形成的化学键是___________ ;
②该结构中,氧氢之间除共价键外还可存在___________ ;
③该结构中,碳原子的杂化方式为___________ 。
(1)Ni原子的核外电子排布式为
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO
(3)NiO晶胞中Ni和O的配位数分别为
(4)NiO的晶体结构如图甲所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为

(5)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图所示。

①该结构中,碳碳之间的共价键类型是σ键,碳氮之间的共价键类型是
②该结构中,氧氢之间除共价键外还可存在
③该结构中,碳原子的杂化方式为
您最近一年使用:0次
8 . 如图是某活泼金属元素A与活泼非金属元素B形成的化合物晶体的一个晶胞,则下列说法中正确的是


| A.该晶胞是二维空间粒子非密置层的一层层堆积 |
B.若晶胞边长为a,则该晶体中A与B粒子之间的最短距离为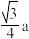 |
| C.该晶胞中与A粒子最近且等距的A粒子有8个 |
| D.该晶胞中A粒子、B粒子的配位数都是8 |
您最近一年使用:0次
2021-02-08更新
|
1484次组卷
|
6卷引用:四川省绵阳市江油中学2020-2021学年高二上学期期中考试化学试题
四川省绵阳市江油中学2020-2021学年高二上学期期中考试化学试题(已下线)第03章 不同聚集状态的物质与性质(A卷基础强化篇)-2020-2021学年高二化学同步单元AB卷(鲁科版2019选择性必修2)山西省长治市第二中学校2020-2021学年高二下学期第一次月考化学试卷(已下线)【知识图鉴】单元讲练测选择性必修2第三章03单元测(已下线)3.3 金属晶体与离子晶体-同步学习必备知识安徽省蚌埠第三中学2021-2022学年高二下学期4月阶段测试化学试题
21-22高三上·江苏常州·期末
解题方法
9 . 铁元素被称为“人类第一元素”,其化合物应用广泛。
Ⅰ.硫化亚铁(FeS)是一种常见的还原剂。用FeS处理模拟含铬废水的流程如下:
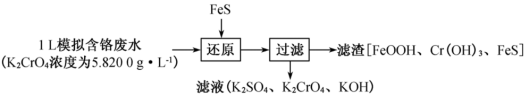
(1)“还原”过程发生反应的离子方程式为______ 。
(2)为测定模拟废水中铬元素的去除率,进行如下实验:将滤渣用蒸馏水洗净后,在低温条件下干燥,称得质量为2.2100g。将上述2.2100g固体在空气中加热,测得固体质量随温度的变化如图所示。

说明:780℃以上的残留固体为Fe2O3、Cr2O3的化合物
① A→B固体质量增加是由滤渣中______ (填化学式)发生反应引起的。
② 在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是______ 。
③ 根据以上实验数据计算上述模拟废水中铬元素的去除率______ (写出计算过程)。
Ⅱ.铁元素是构成人体的必不可少的元素之一,补铁剂种类繁多,其中一种有效成分是琥珀酸亚铁(图1)。

(1) 琥珀酸亚铁中碳原子的杂化轨道类型为______ ,1mol琥珀酸亚铁中含σ键______ mol。
(2) 用邻二氮菲(phen,如图2)与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。[Fe(phen)3]2+中,Fe2+的配位数为______ 。用邻二氮菲测定Fe2+浓度时应控制pH在2~9适宜范围,原因是______ 。
Ⅰ.硫化亚铁(FeS)是一种常见的还原剂。用FeS处理模拟含铬废水的流程如下:

(1)“还原”过程发生反应的离子方程式为
(2)为测定模拟废水中铬元素的去除率,进行如下实验:将滤渣用蒸馏水洗净后,在低温条件下干燥,称得质量为2.2100g。将上述2.2100g固体在空气中加热,测得固体质量随温度的变化如图所示。

说明:780℃以上的残留固体为Fe2O3、Cr2O3的化合物
① A→B固体质量增加是由滤渣中
② 在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是
③ 根据以上实验数据计算上述模拟废水中铬元素的去除率
Ⅱ.铁元素是构成人体的必不可少的元素之一,补铁剂种类繁多,其中一种有效成分是琥珀酸亚铁(图1)。

(1) 琥珀酸亚铁中碳原子的杂化轨道类型为
(2) 用邻二氮菲(phen,如图2)与琥珀酸亚铁生成稳定的橙色配合物,可测定Fe2+的浓度,发生反应:Fe2++3phen=[Fe(phen)3]2+。[Fe(phen)3]2+中,Fe2+的配位数为
您最近一年使用:0次
解题方法
10 . 镍白铜是具有高耐蚀性和良好的力学性能的合金,用于制造在腐蚀性环境中工作的精密仪器零件,Cu和Ni都是常见的合金元素。
(1)Cu的价层电子轨道示意图为___________ 。
(2)单质铜及镍都是由___________ 键形成的晶体;元素铜与镍的第二电离能分别为ICu=1958 kJ·mol-1、INi=1753 kJ·mol-1,ICu>INi;的原因是________ 。
(3)NiO晶胞中Ni2+和O2-的配位数分别为_______ 、_______ 。NiO、FeO的晶体结构类型均与氯化钠的相同:Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO_____ (填“<”或“>”)FeO。
(4)图甲为铜晶体中铜原子堆积模型,图中未标号的铜原子形成晶体后周围最紧邻的铜原子数为___________ 。


(5)某镍白铜合金的立方晶胞结构如乙图所示。
①晶胞中铜原子与镍原子的数量比为___________ 。
②若合金的密度为d g·cm-3,晶胞参数表达式为a=___________ nm。
(1)Cu的价层电子轨道示意图为
(2)单质铜及镍都是由
(3)NiO晶胞中Ni2+和O2-的配位数分别为
(4)图甲为铜晶体中铜原子堆积模型,图中未标号的铜原子形成晶体后周围最紧邻的铜原子数为


(5)某镍白铜合金的立方晶胞结构如乙图所示。
①晶胞中铜原子与镍原子的数量比为
②若合金的密度为d g·cm-3,晶胞参数表达式为a=
您最近一年使用:0次



