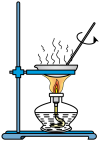
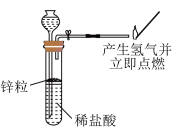
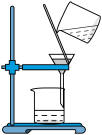
1 . 钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在_______ 中。
(2)除去碳酸钠固体中碳酸氢钠的方法是______________ 。
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入_______ (填“铁粉”或“铜粉”)。
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:_______________ 。
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于__________ (填“碱性”或“两性”)氧化物。
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在
(2)除去碳酸钠固体中碳酸氢钠的方法是
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于
您最近半年使用:0次
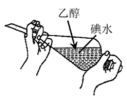
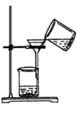
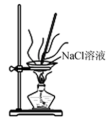
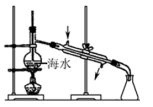
2 . 下列实验方法或操作正确的是
|
|
|
|
| A.萃取碘水中的碘 | B.过滤 | C.获取NaCl | D.制取淡水 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
3 . 黑木耳富含蛋白质、铁、具有还原性的维生素C等,每100 g黑木耳含铁量高达185 mg。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。____________ 。
(2)步骤④检验Fe3+所用试剂是_____________ (填化学式)溶液。
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的阳离子 的离子符号为____________ 。
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。_______ (填序号)。
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为_______________ 。
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是_______________ 。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。
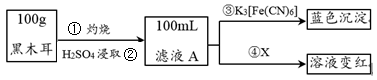
(2)步骤④检验Fe3+所用试剂是
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
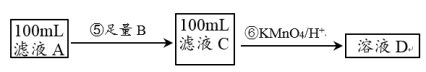
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是
您最近半年使用:0次
4 . 应用下列装置能达到实验目的的是
| A | B | |
| 装置 |
|
|
| 目的 | 从 溶液中制得 溶液中制得 晶体 晶体 | 可用于制备并检验氢气的可燃性 |
| C | D | |
| 装置 |
|
|
| 目的 | 除去 中的HCl并干燥 中的HCl并干燥 | 分离 胶体与NaCl溶液 胶体与NaCl溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
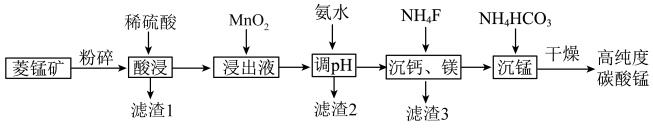
5 . 碳酸钛用作脱硫的催化剂,瓷釉、涂料和清漆的颜料,是合成二氧化锰和制造其他锰盐的原料。工业上制备高纯度碳酸锰的工艺流程如下:
②该工艺下,0.1mol/L的金属离子形成氢氧化物沉淀的pH如下:
③常温下,Ksp(CaF2)=1.60×10-10,Ksp(MgF2)=6.40×10-11.回答下列问题:
(1)基态Mn2+价电子的轨道表示式为___________ 。
(2)滤渣1的主要成份是:___________ ,其附着在矿粉颗粒表面会阻碍菱锰矿与酸的反应,若此时加入H2O2,利用其迅速分解产生的大量气泡可消除其不利影响,导致H2O2分解的因素是___________ 。
(3)在“浸出液”中加入“MnO2”所发生反应的离子方程式为___________ 。
(4)加入氨水调节溶液pH的范围___________ 。
(5)常温下,当溶液中Ca2+、Mg2+完全除去时,则c(F-)≥___________ mol/L。
(6)沉锰步骤发生主要反应的离子方程式为:___________ 。
(7)已知:5 +2Mn2++8H2O=16H++10
+2Mn2++8H2O=16H++10 +2
+2 ,实验室可利用Na2S2O8溶液来检验Mn2+是否反应完全。如何确定Mn2+已完全反应?
,实验室可利用Na2S2O8溶液来检验Mn2+是否反应完全。如何确定Mn2+已完全反应?___________ 。
②该工艺下,0.1mol/L的金属离子形成氢氧化物沉淀的pH如下:
| 金属离子Mn+ | Fe3+ | Al3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀的pH | 1.9 | 3.4 | 7.0 | 8.1 | 9.1 |
| 沉淀完全的pH[c(Mn2+)≤1.0×10-5mol/L] | 3.2 | 4.7 | 9.0 | 10.1 | 11.1 |
(1)基态Mn2+价电子的轨道表示式为
(2)滤渣1的主要成份是:
(3)在“浸出液”中加入“MnO2”所发生反应的离子方程式为
(4)加入氨水调节溶液pH的范围
(5)常温下,当溶液中Ca2+、Mg2+完全除去时,则c(F-)≥
(6)沉锰步骤发生主要反应的离子方程式为:
(7)已知:5
 +2Mn2++8H2O=16H++10
+2Mn2++8H2O=16H++10 +2
+2 ,实验室可利用Na2S2O8溶液来检验Mn2+是否反应完全。如何确定Mn2+已完全反应?
,实验室可利用Na2S2O8溶液来检验Mn2+是否反应完全。如何确定Mn2+已完全反应?
您最近半年使用:0次
解题方法
6 . 丰富多彩的氯家族
18世纪70年代,瑞典化学家舍勒将软锰矿主要成分是MnO2与浓盐酸混合加热。产生了氯气。氯气是一种重要的化工原料,工业上大量用于制造盐酸、次氯酸盐、有机溶剂、农药、染料和药品等,从而形成了品种繁多、功能各异的氯家族。工业上通过电解饱和食盐水的方法制取率气,称为氯碱工业,氯碱工业的产品除应用于化学工业本身之外,还广泛应用于冶金、造纸、农药、有机合成等工业。食盐水在电解前需要精制,主要是为了除去混在氯化钠中的杂质。1.下列物质不能通过单质间的化合反应得到的是________。
| A.FeCl2 | B.FeCl3 | C.CuCl2 | D.HCl |
3.将一瓶新制的氯水长期放置后,溶液中离子取分子浓度不会减少的是________。
| A.Cl2 | B.Cl- | C.H2O | D.HClO |

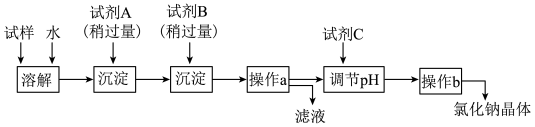
②试剂B是
③试剂C是
④操作b的名称是
您最近半年使用:0次
解题方法
7 . 回答下列问题:
(1)海水制得的粗盐中常常含有泥沙、Ca2+ 、Mg2+ 、SO 等杂质,粗盐提纯的步骤有:①加入过量的 Na2CO3溶液;②加入过量的 NaOH 溶液;③加入过量的 BaCl2溶液;④用适量盐酸调节溶液至中性;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是
等杂质,粗盐提纯的步骤有:①加入过量的 Na2CO3溶液;②加入过量的 NaOH 溶液;③加入过量的 BaCl2溶液;④用适量盐酸调节溶液至中性;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是___________ 。(填选项字母)。
a.⑤⑥③②①⑥④⑦ b.⑤⑥①③②⑥④⑦ c.⑤⑥③①②④⑥⑦ d.⑤⑥②③①⑥④⑦
(2)粗盐提纯实验中用到的盐酸的物质的量浓度为 0.500mol L-1,现实验室某浓盐酸试剂瓶上的有关数据如下:欲用上述浓盐酸配制实验所需浓度的稀盐酸 480mL。
L-1,现实验室某浓盐酸试剂瓶上的有关数据如下:欲用上述浓盐酸配制实验所需浓度的稀盐酸 480mL。
①需量取的浓盐酸的体积为:___________ mL。
②下列操作的正确顺序是___________ (用字母表示)。
B→___________ → ___________→ ___________→ ___________→G
A.上下颠倒摇匀;B.量取;C.洗涤;D.定容;E.稀释;F.移液;G.装瓶
③下列操作会使所配溶液浓度偏低的是___________ 。(填标号)
a.配制前,容量瓶中有少量蒸馏水
b.量取盐酸读数时,仰视刻度线
c.量取盐酸后,洗涤量筒倒入烧杯中
d.定容时水不慎超过了刻度线,用滴管吸出
e.向容量瓶中转移溶液时,不慎有液滴洒在容量瓶外面
(3)配制 500g 0.9%的生理盐水,下列仪器不需要用到的有___________ 。(填仪器名称)
(1)海水制得的粗盐中常常含有泥沙、Ca2+ 、Mg2+ 、SO
 等杂质,粗盐提纯的步骤有:①加入过量的 Na2CO3溶液;②加入过量的 NaOH 溶液;③加入过量的 BaCl2溶液;④用适量盐酸调节溶液至中性;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是
等杂质,粗盐提纯的步骤有:①加入过量的 Na2CO3溶液;②加入过量的 NaOH 溶液;③加入过量的 BaCl2溶液;④用适量盐酸调节溶液至中性;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是a.⑤⑥③②①⑥④⑦ b.⑤⑥①③②⑥④⑦ c.⑤⑥③①②④⑥⑦ d.⑤⑥②③①⑥④⑦
(2)粗盐提纯实验中用到的盐酸的物质的量浓度为 0.500mol
 L-1,现实验室某浓盐酸试剂瓶上的有关数据如下:欲用上述浓盐酸配制实验所需浓度的稀盐酸 480mL。
L-1,现实验室某浓盐酸试剂瓶上的有关数据如下:欲用上述浓盐酸配制实验所需浓度的稀盐酸 480mL。| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19 g/cm3 HCl质量分数/:36.5% |
②下列操作的正确顺序是
B→___________ → ___________→ ___________→ ___________→G
A.上下颠倒摇匀;B.量取;C.洗涤;D.定容;E.稀释;F.移液;G.装瓶
③下列操作会使所配溶液浓度偏低的是
a.配制前,容量瓶中有少量蒸馏水
b.量取盐酸读数时,仰视刻度线
c.量取盐酸后,洗涤量筒倒入烧杯中
d.定容时水不慎超过了刻度线,用滴管吸出
e.向容量瓶中转移溶液时,不慎有液滴洒在容量瓶外面
(3)配制 500g 0.9%的生理盐水,下列仪器不需要用到的有
a. 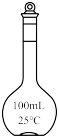 b.
b.  c.
c.  d.
d. 
您最近半年使用:0次
解题方法
8 . 近日,某科研小组制备了新型锂离子电池电极材料——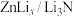 。该小组以废旧锌锰电池为原料合成
。该小组以废旧锌锰电池为原料合成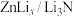 ,简易流程如下:
,简易流程如下: 、Fe、
、Fe、 等)。
等)。
② 在酸性条件下转化成
在酸性条件下转化成 和
和 ;
; 的沸点为78.8℃。
的沸点为78.8℃。
③已知几种金属离子沉淀的pH如表所示:
回答下列问题:
(1)滤渣1的主要成分是___________ (填化学式)。“氧化”步骤除氧化 外还氧化
外还氧化___________ (填微粒符号)。
(2)“调pH”中发生反应的总离子方程式为___________ 。“调pH”最低为___________ 。
(3)“系列操作”是___________ 、___________ 、过滤、洗涤、干燥等。
(4) 的作用是
的作用是___________ (用化学方程式表示)。
(5)合成产品时要隔离空气,在下列___________(填标号)气氛中加热。
(6)工业生产中,氧化剂的实际用量和理论计算量之间的比值称为配氧率。如图是“氧化”中除杂率与配氧率关系。配氧率选择115时除杂率最高的原因是___________ 。
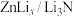 。该小组以废旧锌锰电池为原料合成
。该小组以废旧锌锰电池为原料合成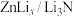 ,简易流程如下:
,简易流程如下: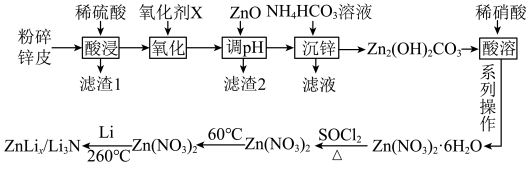
 、Fe、
、Fe、 等)。
等)。②
 在酸性条件下转化成
在酸性条件下转化成 和
和 ;
; 的沸点为78.8℃。
的沸点为78.8℃。③已知几种金属离子沉淀的pH如表所示:
| 金属氢氧化物 |  |  |  |  |
| 开始沉淀的pH | 2.7 | 7.6 | 8.1 | 6.2 |
| 完全沉淀的pH | 3.7 | 9.6 | 10.1 | 8.2 |
(1)滤渣1的主要成分是
 外还氧化
外还氧化(2)“调pH”中发生反应的总离子方程式为
(3)“系列操作”是
(4)
 的作用是
的作用是(5)合成产品时要隔离空气,在下列___________(填标号)气氛中加热。
A. | B. | C.Ar | D. |
(6)工业生产中,氧化剂的实际用量和理论计算量之间的比值称为配氧率。如图是“氧化”中除杂率与配氧率关系。配氧率选择115时除杂率最高的原因是
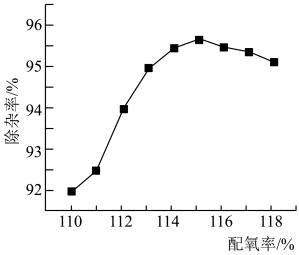
您最近半年使用:0次
9 . 下列装置正确且能达到实验目的的是
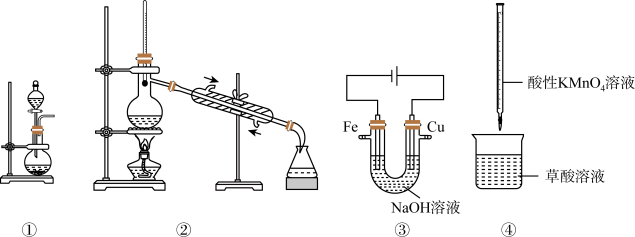
| A.装置①,利用浓盐酸和二氧化锰制备氯气 |
| B.装置②,分离丙酮和2-丙醇混合物 |
C.装置③,制备少量 |
D.装置④,利用已知浓度的酸性 溶液滴定草酸溶液 溶液滴定草酸溶液 |
您最近半年使用:0次
10 . 按要求回答下列问题。
(1)铁盐可用作净水剂,用离子方程式表示其原理:___________ 。配制 溶液时,需将
溶液时,需将 晶体溶解到较浓的
晶体溶解到较浓的___________ 中,然后再加水稀释到所需的浓度。将 溶液蒸干并灼烧,得到的产物是
溶液蒸干并灼烧,得到的产物是___________ (填化学式)。
(2)某 溶液中含有
溶液中含有 杂质,可向溶液中加入足量的
杂质,可向溶液中加入足量的___________ ,充分反应后过滤,即可除去 。
。
(3)在 的
的 溶液中,含有杂质
溶液中,含有杂质 。若通过直接调节
。若通过直接调节 的方法使
的方法使 沉淀完全,是否同时会有
沉淀完全,是否同时会有 沉淀生成?
沉淀生成?___________ (填“是”或“否”)。向溶液中加入 将
将 氧化为
氧化为 ,调节
,调节 使
使 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 ),此时溶液的
),此时溶液的 约为
约为___________ 。(已知 时
时 、
、 、
、 的
的 分别为
分别为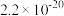 、
、 、
、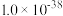 )
)
(1)铁盐可用作净水剂,用离子方程式表示其原理:
 溶液时,需将
溶液时,需将 晶体溶解到较浓的
晶体溶解到较浓的 溶液蒸干并灼烧,得到的产物是
溶液蒸干并灼烧,得到的产物是(2)某
 溶液中含有
溶液中含有 杂质,可向溶液中加入足量的
杂质,可向溶液中加入足量的 。
。(3)在
 的
的 溶液中,含有杂质
溶液中,含有杂质 。若通过直接调节
。若通过直接调节 的方法使
的方法使 沉淀完全,是否同时会有
沉淀完全,是否同时会有 沉淀生成?
沉淀生成? 将
将 氧化为
氧化为 ,调节
,调节 使
使 恰好沉淀完全(浓度等于
恰好沉淀完全(浓度等于 ),此时溶液的
),此时溶液的 约为
约为 时
时 、
、 、
、 的
的 分别为
分别为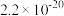 、
、 、
、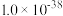 )
)
您最近半年使用:0次