22-23高一下·全国·单元测试
1 . 污水的处理方法
(1)常用的污水处理方法有_______ 、_______ 、和_______ 等。
(2)污水处理常用化学方法:_______ 、_______ 、沉淀法等。
(3)污水处理的流程
①一级处理:通常采用_______ 方法,即用格栅间、沉淀池等除去污水中不溶解的污染物。
②二级处理:采用_______ 方法(又称_______ 法)及某些化学方法,除去水中的可降解有机物等污染物。
③三级处理:主要采用_______ 、_______ 、离子交换法和_______ 等,对污水进行深度处理和净化。经过三级处理后的水可用于_______ 和_______ 用水等。
(1)常用的污水处理方法有
(2)污水处理常用化学方法:
(3)污水处理的流程
①一级处理:通常采用
②二级处理:采用
③三级处理:主要采用
您最近一年使用:0次
2 . 图为某学生进行粗盐提纯实验时过滤操作的示意图。试回答:
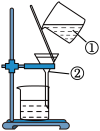
(1)写出标号仪器的名称:
①___________ ;②___________ 。
(2)漏斗中液体的液面应该___________ (填“高”或“低”)于滤纸的边缘。

(1)写出标号仪器的名称:
①
(2)漏斗中液体的液面应该
您最近一年使用:0次
3 . 写出下列物质的除杂方式
Cl2(HCl)____________ CO2(HCl)___________
Cl2(HCl)
您最近一年使用:0次
2023高三·全国·专题练习
4 . 一氯化碘(ICl)是一种卤素互化物。卤素互化物具有强氧化性稀溶液,可与金属直接反应,也可用作有机合成中的碘化剂,一般可由卤素单质直接化合制得。有关一氯化碘制备及性质验证,请回答下列问题:
海藻提碘可得到 的
的 溶液,从其中回收
溶液,从其中回收 的流程如图:
的流程如图:
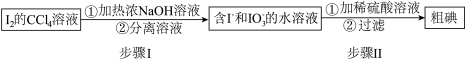
(1)步骤Ⅰ的分离溶液操作中,主要用到的玻璃仪器有烧杯和_______ 。
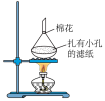
(2)回收获得的粗碘可采用如图所示的简易装置分离提纯。将粉状物放入蒸发皿中并小火加热,碘晶体在扎有小孔的滤纸上凝结,该分离提纯方法的名称是_______ 。
海藻提碘可得到
 的
的 溶液,从其中回收
溶液,从其中回收 的流程如图:
的流程如图:
(1)步骤Ⅰ的分离溶液操作中,主要用到的玻璃仪器有烧杯和
(2)回收获得的粗碘可采用如图所示的简易装置分离提纯。将粉状物放入蒸发皿中并小火加热,碘晶体在扎有小孔的滤纸上凝结,该分离提纯方法的名称是

您最近一年使用:0次
23-24高一上·全国·课时练习
解题方法
5 . 二草酸合铜(Ⅱ)酸钾(K2[Cu(C2O4)2])可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
I.取已知浓度的CuSO4溶液,搅拌下滴加足量NaOH溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
Ⅱ.向草酸(H2C2O4)溶液中加入适量K2CO3固体,制得KHC2O4和K2C2O4混合溶液。
Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入I中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分析。
回答下列问题:
由 配制I中的CuSO4溶液,下列仪器中不需要的是
配制I中的CuSO4溶液,下列仪器中不需要的是_______ (填仪器名称)。

I.取已知浓度的CuSO4溶液,搅拌下滴加足量NaOH溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
Ⅱ.向草酸(H2C2O4)溶液中加入适量K2CO3固体,制得KHC2O4和K2C2O4混合溶液。
Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入I中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分析。
回答下列问题:
由
 配制I中的CuSO4溶液,下列仪器中不需要的是
配制I中的CuSO4溶液,下列仪器中不需要的是
您最近一年使用:0次
解题方法
6 . 除去Na2CO3粉末中混有的少量NaHCO3的方法是___________ 。
您最近一年使用:0次
7 . 怎样除去乙烷中的乙烯?___________
您最近一年使用:0次
8 . 选择完成下列实验的装置。

(1)加热 和
和 固体的混合物制
固体的混合物制 ,用
,用__________ (填序号,下同)。
(2)从盐水中获得食盐,用__________ 。
(3)实验室收集 ,用
,用__________ 。

(1)加热
 和
和 固体的混合物制
固体的混合物制 ,用
,用(2)从盐水中获得食盐,用
(3)实验室收集
 ,用
,用
您最近一年使用:0次
解题方法
9 . 以盐湖锂矿(主要成分为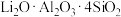 ,还含有
,还含有 及少量有机物等)为原料制备
及少量有机物等)为原料制备 的方法如下:
的方法如下:
(1)酸化:将适量盐湖锂矿粉与水混合,加入一定量浓 ,充分反应后加水稀释,过滤。酸化过程会产生少量
,充分反应后加水稀释,过滤。酸化过程会产生少量 ,原因是
,原因是___________ 。
(2)净化:
①加碱调节滤液的 至弱碱性,使
至弱碱性,使 沉淀;将再加入适量
沉淀;将再加入适量 溶液将
溶液将 转化为沉淀,过滤。
转化为沉淀,过滤。 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
②调节滤液的 ,再加入适量
,再加入适量 粉末,过滤,得
粉末,过滤,得 溶液。过滤所得滤渣的主要成分是
溶液。过滤所得滤渣的主要成分是___________ 。
(3)沉锂:80℃时将饱和 溶液与饱和
溶液与饱和 溶液混合充分反应,过滤,得
溶液混合充分反应,过滤,得 晶体。“沉锂”时选择较高温度,所得
晶体。“沉锂”时选择较高温度,所得 的产率及纯度较高。原因是
的产率及纯度较高。原因是___________ 。
已知 三种物质在不同温度下的溶解度如下表:
三种物质在不同温度下的溶解度如下表:
(4) 样品纯度测定:称取
样品纯度测定:称取 样品置于锥形瓶中,加入
样品置于锥形瓶中,加入 盐酸,搅拌,充分反应(杂质不与酸反应)。再加入几滴酚酞,用
盐酸,搅拌,充分反应(杂质不与酸反应)。再加入几滴酚酞,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的体积为
溶液的体积为 。计算
。计算 样品的纯度
样品的纯度___________ (写出计算过程)。
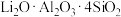 ,还含有
,还含有 及少量有机物等)为原料制备
及少量有机物等)为原料制备 的方法如下:
的方法如下:(1)酸化:将适量盐湖锂矿粉与水混合,加入一定量浓
 ,充分反应后加水稀释,过滤。酸化过程会产生少量
,充分反应后加水稀释,过滤。酸化过程会产生少量 ,原因是
,原因是(2)净化:
①加碱调节滤液的
 至弱碱性,使
至弱碱性,使 沉淀;将再加入适量
沉淀;将再加入适量 溶液将
溶液将 转化为沉淀,过滤。
转化为沉淀,过滤。 与
与 反应的离子方程式为
反应的离子方程式为②调节滤液的
 ,再加入适量
,再加入适量 粉末,过滤,得
粉末,过滤,得 溶液。过滤所得滤渣的主要成分是
溶液。过滤所得滤渣的主要成分是(3)沉锂:80℃时将饱和
 溶液与饱和
溶液与饱和 溶液混合充分反应,过滤,得
溶液混合充分反应,过滤,得 晶体。“沉锂”时选择较高温度,所得
晶体。“沉锂”时选择较高温度,所得 的产率及纯度较高。原因是
的产率及纯度较高。原因是已知
 三种物质在不同温度下的溶解度如下表:
三种物质在不同温度下的溶解度如下表:温度/℃ 物质 | 0 | 20 | 40 | 60 | 80 |
 | 7.0 | 21.5 | 49.0 | 46.0 | 43.9 |
 | 36.1 | 34.8 | 33.7 | 32.6 | 31.4 |
 | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 |
 样品纯度测定:称取
样品纯度测定:称取 样品置于锥形瓶中,加入
样品置于锥形瓶中,加入 盐酸,搅拌,充分反应(杂质不与酸反应)。再加入几滴酚酞,用
盐酸,搅拌,充分反应(杂质不与酸反应)。再加入几滴酚酞,用 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液的体积为
溶液的体积为 。计算
。计算 样品的纯度
样品的纯度
您最近一年使用:0次
10 . 化学与人们的衣食住行密不可分,请回答下列问题:
(1)写出甲烷的电子式___________ ,小汽车使用的汽油主要是通过石油的___________ (填“裂化”或“裂解”)而来。
(2)市场上的衣物琳琅满目,其主要成分有天然的棉、麻、毛、丝等,羊毛的主要成分是___________ (填“糖类”“油脂”或“蛋白质”)。
(3)盐可以影响食物的味道。某粗盐中含有 、
、 、
、 等杂质离子,精制时常用的试剂:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是___________ (填字母)。
等杂质离子,精制时常用的试剂:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是___________ (填字母)。
(4)铝与氢氧化钠溶液反应的离子方程式是___________ 。金刚砂(主要成分SiC),其中的碳原子和硅原子通过___________ 连接(填“离子键”、“极性共价键”、“非极性共价键”)。
(1)写出甲烷的电子式
(2)市场上的衣物琳琅满目,其主要成分有天然的棉、麻、毛、丝等,羊毛的主要成分是
(3)盐可以影响食物的味道。某粗盐中含有
 、
、 、
、 等杂质离子,精制时常用的试剂:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是___________ (填字母)。
等杂质离子,精制时常用的试剂:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是___________ (填字母)。| A.①②③④ | B.②③④① | C.④③②① | D.③④②① |
您最近一年使用:0次



