1 . 阅读下列材料,按要求回答问题。
材料1 酒精、苯、CCl4都是有机溶剂,有机溶剂之间大多能互溶;
材料2 碘(I2)易溶于有机溶剂;
材料3 溴微溶于水,易溶于有机溶剂,其溶液呈橙红色。
在酒精、苯、CCl4、蒸馏水四种试剂中:
(1)能把碘单质从碘水中萃取出来的是___________ ,进行分液之后___________ (填“能”或“不能”)得到纯净的碘单质。
(2)能把溴从溴水中萃取出来,并在分液时使含溴液体从分液漏斗下口流出的是___________ 。
(3)CCl4___________ (填“能”或“不能”)把碘酒中的碘萃取出来,原因是___________ 。
材料1 酒精、苯、CCl4都是有机溶剂,有机溶剂之间大多能互溶;
材料2 碘(I2)易溶于有机溶剂;
材料3 溴微溶于水,易溶于有机溶剂,其溶液呈橙红色。
在酒精、苯、CCl4、蒸馏水四种试剂中:
(1)能把碘单质从碘水中萃取出来的是
(2)能把溴从溴水中萃取出来,并在分液时使含溴液体从分液漏斗下口流出的是
(3)CCl4
您最近一年使用:0次
2 . 回答下列问题
(1)以下物质:①KCl晶体;②液态HCl;③食盐水;④熔融NaCl;⑤蔗糖;⑥铜;⑦ ;能导电的是
;能导电的是___________ (填序号,下同);属于电解质的是___________ ;属于非电解质的是___________ 。
(2)在离子 中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是___________ 。
(3)用___________ 方法将植物油和水的混合体系分离;用___________ 方法分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合液体(四氯化碳和甲苯互溶)。
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打( ),能治疗胃酸过多,请写出其反应的离子方程式:
),能治疗胃酸过多,请写出其反应的离子方程式:___________ ;此时最好用含氢氧化铝的胃药(如胃舒平)离子方程式:___________ 。
(1)以下物质:①KCl晶体;②液态HCl;③食盐水;④熔融NaCl;⑤蔗糖;⑥铜;⑦
 ;能导电的是
;能导电的是(2)在离子
 中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是(3)用
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(
 ),能治疗胃酸过多,请写出其反应的离子方程式:
),能治疗胃酸过多,请写出其反应的离子方程式:
您最近一年使用:0次
3 . 按要求完成下列问题。
(1)可用于分离或提纯物质的方法有:a.过滤;b.结晶;c.蒸馏;d.萃取;e.分液。请将相应分离提纯物质方法的序号填入空白处:
①从碘的氯化钾水溶液提取碘:_______ 。
②分离乙酸(沸点118℃)和乙醚(沸点34℃):_______ 。
③分离水和汽油的混合物:_______ 。
(2)用以下物质的序号填空:①液氨;②硫酸;③熔融氯化钾;④碳酸铵溶液;⑤蔗糖。属于电解质的有_______ ;属于非电解质的有_______ ;能导电的有_______ 。
(1)可用于分离或提纯物质的方法有:a.过滤;b.结晶;c.蒸馏;d.萃取;e.分液。请将相应分离提纯物质方法的序号填入空白处:
①从碘的氯化钾水溶液提取碘:
②分离乙酸(沸点118℃)和乙醚(沸点34℃):
③分离水和汽油的混合物:
(2)用以下物质的序号填空:①液氨;②硫酸;③熔融氯化钾;④碳酸铵溶液;⑤蔗糖。属于电解质的有
您最近一年使用:0次
解题方法
4 . 下列各组物质的分离或提纯,应选用下述方法的哪一种?(填标号)
A.萃取 B.加热 C.结晶 D.分液 E.过滤 F.蒸馏
(1)除去食盐水中的泥沙___________ 。
(2)从含有少量氯化钠的硝酸钾溶液中提取硝酸钾___________ 。
(3)分离水和汽油___________ 。
(4)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物___________ 。
(5)有如下物质:①铁丝 ②NaOH溶液 ③Na2SO4固体 ④CO2 ⑤酒精 ⑥自来水⑦CCl4 ⑧熔融的KNO3 ⑨红褐色的氢氧化铁胶体。其中,属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。鉴别②和⑨最简单有效的物理方法是___________ (写实验名称)。
A.萃取 B.加热 C.结晶 D.分液 E.过滤 F.蒸馏
(1)除去食盐水中的泥沙
(2)从含有少量氯化钠的硝酸钾溶液中提取硝酸钾
(3)分离水和汽油
(4)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物
(5)有如下物质:①铁丝 ②NaOH溶液 ③Na2SO4固体 ④CO2 ⑤酒精 ⑥自来水⑦CCl4 ⑧熔融的KNO3 ⑨红褐色的氢氧化铁胶体。其中,属于电解质的是
您最近一年使用:0次
名校
5 . Ⅰ.根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化
(1)写出碳酸氢钠在水中的电离方程式:________ ;
(2)除去FeSO4溶液中的少量CuSO4时发生的离子方程式:________ ;
(3)已知硼酸(H3BO3)的电离方程式可表示为:H3BO3+H2O B(OH)
B(OH) +H+,请写出硼酸与NaOH反应的离子方程式:
+H+,请写出硼酸与NaOH反应的离子方程式:________ ;
Ⅱ.过滤、结晶、蒸馏、萃取分液、渗析等是物质分离提纯的常用实验操作
(4)除去蛋白质溶液里混有的(NH4)2SO4的实验操作是________ ;
(5)已知硫酸镁和硼酸的溶解度曲线如图,为了分别获取硫酸镁晶体和硼酸晶体,做如下操作:

ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;
ⅱ.将浓缩液加入到高压釜(确保水在200℃不沸腾)中,升温至200℃结晶,________ 分离出硫酸镁,分离后再将母液降温结晶,分离得到硼酸晶体。
Ⅲ.物质的量是联系宏观和微观的桥梁:
(6)一定质量的CH4中含有的原子总数为N,若阿伏伽德罗常数用NA表示,则CH4的物质的量是________ mol
(7)由CO、CO2两气体组成的混合气体12.8g,标准状况下的体积为8.96L。则CO、CO2的物质的量之比为________ 。
(1)写出碳酸氢钠在水中的电离方程式:
(2)除去FeSO4溶液中的少量CuSO4时发生的离子方程式:
(3)已知硼酸(H3BO3)的电离方程式可表示为:H3BO3+H2O
 B(OH)
B(OH) +H+,请写出硼酸与NaOH反应的离子方程式:
+H+,请写出硼酸与NaOH反应的离子方程式:Ⅱ.过滤、结晶、蒸馏、萃取分液、渗析等是物质分离提纯的常用实验操作
(4)除去蛋白质溶液里混有的(NH4)2SO4的实验操作是
(5)已知硫酸镁和硼酸的溶解度曲线如图,为了分别获取硫酸镁晶体和硼酸晶体,做如下操作:

ⅰ.浓缩滤液,使MgSO4和H3BO3接近饱和;
ⅱ.将浓缩液加入到高压釜(确保水在200℃不沸腾)中,升温至200℃结晶,
Ⅲ.物质的量是联系宏观和微观的桥梁:
(6)一定质量的CH4中含有的原子总数为N,若阿伏伽德罗常数用NA表示,则CH4的物质的量是
(7)由CO、CO2两气体组成的混合气体12.8g,标准状况下的体积为8.96L。则CO、CO2的物质的量之比为
您最近一年使用:0次
名校
6 . 回答下列问题。
(1)物质的量是高中化学常用的物理量,请完成以下有关计算:
①标准状况下,含有相同氧原子数的CO和 的体积之比为
的体积之比为___________ 。
②某气体氧化物的化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为___________ ,R的相对原子质量为___________ 。
③某盐混合溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则c(
,则c( )=
)=___________ 。
(2)根据实验要求,从下列物质的分离或提纯方法中,选择恰当的实验方法将其序号填在空格处。
A.萃取分液 B.过滤 C.加热分解 D.蒸馏
①分离食盐水与沙子的混合物:___________ 。
②从碘水中提取碘:___________ 。
③分离四氯化碳(沸点 )和甲苯(沸点
)和甲苯(沸点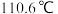 )的混合物:
)的混合物:___________ 。
(1)物质的量是高中化学常用的物理量,请完成以下有关计算:
①标准状况下,含有相同氧原子数的CO和
 的体积之比为
的体积之比为②某气体氧化物的化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为③某盐混合溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则c(
,则c( )=
)=(2)根据实验要求,从下列物质的分离或提纯方法中,选择恰当的实验方法将其序号填在空格处。
A.萃取分液 B.过滤 C.加热分解 D.蒸馏
①分离食盐水与沙子的混合物:
②从碘水中提取碘:
③分离四氯化碳(沸点
 )和甲苯(沸点
)和甲苯(沸点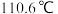 )的混合物:
)的混合物:
您最近一年使用:0次
7 . Ⅰ.利用物质的溶解度对物质进行分离、提纯。图甲、图乙所示为一些物质的溶解度随温度变化的曲线。

(1) 固体中含少量NaCl,提纯
固体中含少量NaCl,提纯 固体的操作方法是加水溶解、
固体的操作方法是加水溶解、______ 、______ 、过滤、洗涤、干燥。
(2)图乙所示为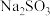 的溶解度随温度的变化曲线.常温下由
的溶解度随温度的变化曲线.常温下由 稀溶液获取
稀溶液获取 固体的方法是
固体的方法是____________ 。
Ⅱ.硫酸钠-过氧化氢加合物( )的组成可通过下列实验测定:
)的组成可通过下列实验测定:
①准确称取17.700 g样品,配制成100.00 mL溶液A
②将A两等份,取一份,加入盐酸酸化的BaCl₂溶液至沉淀完全、过滤、洗涤、干燥至恒重,得到白色固体11.65 g。
③另一份加适量稀硫酸酸化后,与50 mL 0.2 mol/L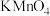 溶液恰好完全反应。
溶液恰好完全反应。
(3)已知 与
与 反应的化学方程式如下:
反应的化学方程式如下:
 ,通过计算确定样品的组成
,通过计算确定样品的组成________ (写出计算过程)。

(1)
 固体中含少量NaCl,提纯
固体中含少量NaCl,提纯 固体的操作方法是加水溶解、
固体的操作方法是加水溶解、(2)图乙所示为
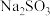 的溶解度随温度的变化曲线.常温下由
的溶解度随温度的变化曲线.常温下由 稀溶液获取
稀溶液获取 固体的方法是
固体的方法是Ⅱ.硫酸钠-过氧化氢加合物(
 )的组成可通过下列实验测定:
)的组成可通过下列实验测定:①准确称取17.700 g样品,配制成100.00 mL溶液A
②将A两等份,取一份,加入盐酸酸化的BaCl₂溶液至沉淀完全、过滤、洗涤、干燥至恒重,得到白色固体11.65 g。
③另一份加适量稀硫酸酸化后,与50 mL 0.2 mol/L
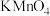 溶液恰好完全反应。
溶液恰好完全反应。(3)已知
 与
与 反应的化学方程式如下:
反应的化学方程式如下:
 ,通过计算确定样品的组成
,通过计算确定样品的组成
您最近一年使用:0次
2023-12-24更新
|
91次组卷
|
2卷引用:江苏省宿迁市沭阳县2023-2024学年高一上学期期中调研测试化学试题
8 . 选择下列实验方法分离物质,将分离方法的字母序号填在横线上。
A.过滤法B.分液法C.蒸馏法D.结晶法
(1)___________ 分离水和豆油的混合物;
(2)___________ 从含有硝酸钾和少量氯化钾的混合溶液中获得硝酸钾;
(3)___________ 分离饱和食盐水和沙子的混合物;
(4)_______ 分离四氯化碳(沸点为 )和甲苯(沸点为
)和甲苯(沸点为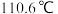 ),已知四氯化碳和甲苯互溶。
),已知四氯化碳和甲苯互溶。
A.过滤法B.分液法C.蒸馏法D.结晶法
(1)
(2)
(3)
(4)
 )和甲苯(沸点为
)和甲苯(沸点为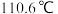 ),已知四氯化碳和甲苯互溶。
),已知四氯化碳和甲苯互溶。
您最近一年使用:0次
9 . 可用于物质分离或提纯物质的方法有:A.过滤 B.萃取 C.分液 D.蒸馏 E.降温结晶 F.高温分解 G.洗气法 H.升华;下列各组混合物的分离或提纯应选用上述哪种方法最合适?(填字母)
(1)分离水和苯的混合物,用___________ 。
(2)分离 固体和碘单质的混合物,用
固体和碘单质的混合物,用___________ 。
(3)分离 (沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物,用
(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物,用___________ 。
(4)除去 中少量的水蒸气,用
中少量的水蒸气,用___________ 。
(5)除去氧化钙中的少量 固体,用
固体,用___________ 。
(1)分离水和苯的混合物,用
(2)分离
 固体和碘单质的混合物,用
固体和碘单质的混合物,用(3)分离
 (沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物,用
(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物,用(4)除去
 中少量的水蒸气,用
中少量的水蒸气,用(5)除去氧化钙中的少量
 固体,用
固体,用
您最近一年使用:0次
名校
10 . 现有下列几种物质:
①Al ②乙醇 ③ ④熔融CaO ⑤
④熔融CaO ⑤ 溶液 ⑥
溶液 ⑥ ⑦
⑦ 固体
固体
(1)上述物质属于电解质的有___________ (填序号,下同),属于非电解质的有___________ 。
(2)Na加入到 溶液反应产生的气体通过足量碱石灰后经检验还有两种气体,它们是:
溶液反应产生的气体通过足量碱石灰后经检验还有两种气体,它们是:___________ 。
(3)Al加入到足量NaOH溶液的离子方程式:___________ 。
(4)乙醇中混有水可以先加入CaO再___________ 而得到比较纯净的乙醇。
(5)向 溶液中逐渐加入A溶液时,溶液导电性的变化趋势如图所示:滴加溶液A至图中曲线最低点时,灯泡熄灭,则溶液A中的溶质是___________(填标号)。
溶液中逐渐加入A溶液时,溶液导电性的变化趋势如图所示:滴加溶液A至图中曲线最低点时,灯泡熄灭,则溶液A中的溶质是___________(填标号)。

①Al ②乙醇 ③
 ④熔融CaO ⑤
④熔融CaO ⑤ 溶液 ⑥
溶液 ⑥ ⑦
⑦ 固体
固体(1)上述物质属于电解质的有
(2)Na加入到
 溶液反应产生的气体通过足量碱石灰后经检验还有两种气体,它们是:
溶液反应产生的气体通过足量碱石灰后经检验还有两种气体,它们是:(3)Al加入到足量NaOH溶液的离子方程式:
(4)乙醇中混有水可以先加入CaO再
(5)向
 溶液中逐渐加入A溶液时,溶液导电性的变化趋势如图所示:滴加溶液A至图中曲线最低点时,灯泡熄灭,则溶液A中的溶质是___________(填标号)。
溶液中逐渐加入A溶液时,溶液导电性的变化趋势如图所示:滴加溶液A至图中曲线最低点时,灯泡熄灭,则溶液A中的溶质是___________(填标号)。
| A.HCl | B. | C. | D. |
您最近一年使用:0次



