解题方法
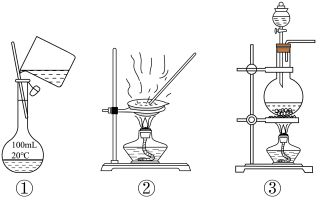
1 . 选择完成下列实验的装置。 溶液中获取
溶液中获取 固体,选用
固体,选用_______ (填序号,下同)。
(2)配制 溶液,选用
溶液,选用_______ 。
(3)加热 和浓盐酸的混合物制
和浓盐酸的混合物制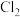 ,选用
,选用_______ 。
 溶液中获取
溶液中获取 固体,选用
固体,选用(2)配制
 溶液,选用
溶液,选用(3)加热
 和浓盐酸的混合物制
和浓盐酸的混合物制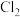 ,选用
,选用
您最近一年使用:0次
名校
2 . 硫酸锌广泛应用于工农业生产中。工业上以粗氧化锌(含 等杂质)为原料生产
等杂质)为原料生产 的一种流程的部分过程如下(各过程需控制适宜条件)。
的一种流程的部分过程如下(各过程需控制适宜条件)。
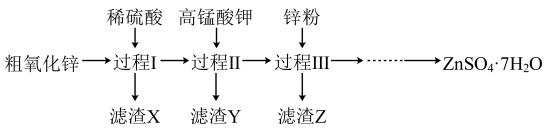
(1)过程Ⅰ、Ⅱ、Ⅲ中,分离出X、Y、Z的实验操作是_______ 。
(2)过程Ⅰ,能与稀硫酸反应的物质有________ 。写出生成氢气的离子方程式:_______ ,因此过程Ⅰ需要持续强制通风,原因是生成的氢气具有______ 性。
(3)过程Ⅱ中,滤渣Y含有 。加入高锰酸钾的主要目的是
。加入高锰酸钾的主要目的是_______ 。
(4)过程Ⅲ中,滤渣Z含铜,生成铜的离子方程式为________ 。
 等杂质)为原料生产
等杂质)为原料生产 的一种流程的部分过程如下(各过程需控制适宜条件)。
的一种流程的部分过程如下(各过程需控制适宜条件)。
(1)过程Ⅰ、Ⅱ、Ⅲ中,分离出X、Y、Z的实验操作是
(2)过程Ⅰ,能与稀硫酸反应的物质有
(3)过程Ⅱ中,滤渣Y含有
 。加入高锰酸钾的主要目的是
。加入高锰酸钾的主要目的是(4)过程Ⅲ中,滤渣Z含铜,生成铜的离子方程式为
您最近一年使用:0次
名校
解题方法
3 . 写出符合下列离子方程式对应的一个化学方程式,按要求写出反应式。
(1)Ba2++ =BaSO4↓
=BaSO4↓___________ 。
(2)Ag++Cl-=AgCl↓___________ 。
(3)除去NaHCO3溶液中的Na2CO3,反应的离子方程式是___________ 。
(1)Ba2++
 =BaSO4↓
=BaSO4↓(2)Ag++Cl-=AgCl↓
(3)除去NaHCO3溶液中的Na2CO3,反应的离子方程式是
您最近一年使用:0次
名校
4 . Na元素相关的物质有很多且具有广泛的用途。
(1)氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。粗盐中一般含有CaCl2、MgCl2、CaSO4和MgSO4杂质。从粗盐制得精盐的过程如下:

①试剂Ⅰ是_____ 。
②加入试剂Ⅱ所发生的离子方程式为:_____
③操作a中,未用到的实验仪器是_____
A.蒸发皿 B.玻璃棒 C.漏斗 D.烧杯
④用到操作c的名称为_____ ,操作b不能省略,理由是_____ 。
(2)Na2CO3、NaHCO3走进千家万户,在食品加工方面有着广泛的用途。
①下列关于Na2CO3的认识正确的是_____ 。
A.受热易分解 B.俗称纯碱、苏打 C.可用于制皂 D.可与酸反应
②传统蒸馒头常采用酵头发面,再用Na2CO3调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。等质量的碳酸钠和碳酸氢钠,消耗酸更多的是_____ 。
③若面团发得不好,面团内的气孔少,略有酸味。可不用Na2CO3而用NaHCO3,继续揉面,上锅蒸后也能蒸出松软的馒头。解释NaHCO3的作用_____ 。
(3)某品牌复合膨松剂的说明书如下图所示。其中葡萄糖酸-δ-内酯和淀粉是助剂,其作用是防止膨松剂吸潮结块而失效。焦磷酸二氢二钠的作用是_____ 。

(1)氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。粗盐中一般含有CaCl2、MgCl2、CaSO4和MgSO4杂质。从粗盐制得精盐的过程如下:

①试剂Ⅰ是
②加入试剂Ⅱ所发生的离子方程式为:
③操作a中,未用到的实验仪器是
A.蒸发皿 B.玻璃棒 C.漏斗 D.烧杯
④用到操作c的名称为
(2)Na2CO3、NaHCO3走进千家万户,在食品加工方面有着广泛的用途。
①下列关于Na2CO3的认识正确的是
A.受热易分解 B.俗称纯碱、苏打 C.可用于制皂 D.可与酸反应
②传统蒸馒头常采用酵头发面,再用Na2CO3调节面团酸度。查阅资料得知,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。等质量的碳酸钠和碳酸氢钠,消耗酸更多的是
③若面团发得不好,面团内的气孔少,略有酸味。可不用Na2CO3而用NaHCO3,继续揉面,上锅蒸后也能蒸出松软的馒头。解释NaHCO3的作用
(3)某品牌复合膨松剂的说明书如下图所示。其中葡萄糖酸-δ-内酯和淀粉是助剂,其作用是防止膨松剂吸潮结块而失效。焦磷酸二氢二钠的作用是

您最近一年使用:0次
名校
解题方法
5 . 选择完成下列实验的装置。
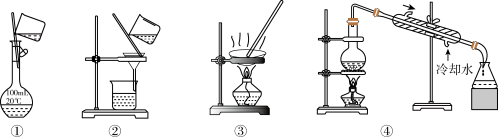
(1)除去水中的泥沙用___________ (填序号,下同)。
(2)配制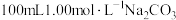 溶液,选用
溶液,选用___________ 。
(3)自来水制备蒸馏水,选用___________ 。
(4)从 溶液中获取
溶液中获取 固体,选用
固体,选用___________ 。

(1)除去水中的泥沙用
(2)配制
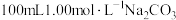 溶液,选用
溶液,选用(3)自来水制备蒸馏水,选用
(4)从
 溶液中获取
溶液中获取 固体,选用
固体,选用
您最近一年使用:0次
6 . 氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。

下列说法中,不正确 的是_______ 。
a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
d.加热至熔融状态的NaCl也可以解离出自由移动的Na+和Cl-
(2)某同学用含钠元素的不同类别 物质制备NaCl。化学反应方程式如下:
a.2Na+Cl2 2NaCl
2NaCl
b.NaOH+HCl=NaCl+H2O
c.Na2O+2HCl=2NaCl+H2O
d._______
①反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为_______ 。
②反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为_______ 。
③反应c中的原料Na2O的物质类别是_______ ,请依据其类别通性,再列举2个能与Na2O反应的其他物质(用化学式表示)_______ 、_______ 。
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO 等可溶性杂质。为得到精制食盐水,某同学设计如下除杂流程,用到的试剂有:BaCl2溶液、NaOH溶液、Na2CO3溶液和盐酸。
等可溶性杂质。为得到精制食盐水,某同学设计如下除杂流程,用到的试剂有:BaCl2溶液、NaOH溶液、Na2CO3溶液和盐酸。

(3)操作a的名称是_______ ,试剂2是_______ 。
(4)溶液A中除Na+和Cl-外,还存在的离子有_______ 。
(5)沉淀B主要成分的化学式是_______ 。
(6)用离子方程式表示盐酸的作用_______ 、_______ 。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。

下列说法中,
a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
d.加热至熔融状态的NaCl也可以解离出自由移动的Na+和Cl-
(2)某同学用
a.2Na+Cl2
 2NaCl
2NaClb.NaOH+HCl=NaCl+H2O
c.Na2O+2HCl=2NaCl+H2O
d._______
①反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为
②反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为
③反应c中的原料Na2O的物质类别是
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO
 等可溶性杂质。为得到精制食盐水,某同学设计如下除杂流程,用到的试剂有:BaCl2溶液、NaOH溶液、Na2CO3溶液和盐酸。
等可溶性杂质。为得到精制食盐水,某同学设计如下除杂流程,用到的试剂有:BaCl2溶液、NaOH溶液、Na2CO3溶液和盐酸。
(3)操作a的名称是
(4)溶液A中除Na+和Cl-外,还存在的离子有
(5)沉淀B主要成分的化学式是
(6)用离子方程式表示盐酸的作用
您最近一年使用:0次
名校
7 . 过氧化钙(CaO2)微溶于水,可作医用防腐剂、消毒剂,以下是制备CaO2的一种方法。

回答下列问题:
(1)CaO2中O元素的化合价为________ 。
(2)步骤Ⅰ中反应的离子方程式是________ 。
(3)步骤Ⅱ中反应的化学方程式是:________ =CaO2•8H2O↓+2NH4Cl,反应在冰水浴 中进行,是为了防止NH3•H2O挥发、________ (答1条即可)。
(4)待CaO2•8H2O结晶析出后通过________ (填操作名称)分离。
(5)CaO2可与水或二氧化碳缓慢反应,同时产生氧气,常用作鱼塘的供氧剂。CaO2与水反应的化学方程式是________ 。CaO2还可用于长途运输鱼苗,推测CaO2可能具有________ (填字母)性质。
a.可缓慢供氧 b.能吸收鱼苗呼出的CO2 c.可抑菌

回答下列问题:
(1)CaO2中O元素的化合价为
(2)步骤Ⅰ中反应的离子方程式是
(3)步骤Ⅱ中反应的化学方程式是:
(4)待CaO2•8H2O结晶析出后通过
(5)CaO2可与水或二氧化碳缓慢反应,同时产生氧气,常用作鱼塘的供氧剂。CaO2与水反应的化学方程式是
a.可缓慢供氧 b.能吸收鱼苗呼出的CO2 c.可抑菌
您最近一年使用:0次
8 . 黏土钒矿中,钒以+3价、+4价、+5价的化合物存在,还包括SiO2、Fe2O3和铝硅酸盐(Al2O3•SiO2)等。采用以下流程可由黏土钒矿制备V2O5、Fe2O3和硫酸铝铵。

已知:i.有机酸性萃取剂HR的萃取原理为:Mn+(aq)+nHR(org) MR(org)+nH+(aq)(org表示有机溶液)
MR(org)+nH+(aq)(org表示有机溶液)
ii.酸性溶液中,HR对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。
iii.HR能萃取Fe3+而不能萃取Fe2+。
(1)从黏土钒矿到浸出液的流程中,加快浸出速率的措施有_______ 。
(2)浸出液中钒以+4价、+5价的形式存在,简述加入铁粉的原因:_______ 。
(3)从平衡移动原理解释加入20%H2SO4溶液的作用:_______ 。
(4)KClO3和VO2+(反应生成VO 和Cl-的离子方程式是
和Cl-的离子方程式是_______ 。
(5)测定V2O5产品的纯度
称取V2O5产品ag,先加入硫酸将V2O5转化为VO ,加入指示剂后,cmol/L(NH4)2Fe(SO4)2溶液滴定将VO
,加入指示剂后,cmol/L(NH4)2Fe(SO4)2溶液滴定将VO 转化为VO2+至终点,消耗(NH4)2Fe(SO4)2溶液的体积为VmL。假设杂质不参与反应,则V2O5产品中V2O5的质量分数是
转化为VO2+至终点,消耗(NH4)2Fe(SO4)2溶液的体积为VmL。假设杂质不参与反应,则V2O5产品中V2O5的质量分数是_______ (V2O5的摩尔质量为Mg/mol)。
(6)从无机层获得Fe(OH)3的离子方程式是_______ 。
(7)硫酸铝铵固体中含有少量硫酸铵杂质,根据如图的溶解度曲线,进一步提纯硫酸铝铵的操作是加热溶解、_______ 、洗涤、干燥。


已知:i.有机酸性萃取剂HR的萃取原理为:Mn+(aq)+nHR(org)
 MR(org)+nH+(aq)(org表示有机溶液)
MR(org)+nH+(aq)(org表示有机溶液)ii.酸性溶液中,HR对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。
iii.HR能萃取Fe3+而不能萃取Fe2+。
(1)从黏土钒矿到浸出液的流程中,加快浸出速率的措施有
(2)浸出液中钒以+4价、+5价的形式存在,简述加入铁粉的原因:
(3)从平衡移动原理解释加入20%H2SO4溶液的作用:
(4)KClO3和VO2+(反应生成VO
 和Cl-的离子方程式是
和Cl-的离子方程式是(5)测定V2O5产品的纯度
称取V2O5产品ag,先加入硫酸将V2O5转化为VO
 ,加入指示剂后,cmol/L(NH4)2Fe(SO4)2溶液滴定将VO
,加入指示剂后,cmol/L(NH4)2Fe(SO4)2溶液滴定将VO 转化为VO2+至终点,消耗(NH4)2Fe(SO4)2溶液的体积为VmL。假设杂质不参与反应,则V2O5产品中V2O5的质量分数是
转化为VO2+至终点,消耗(NH4)2Fe(SO4)2溶液的体积为VmL。假设杂质不参与反应,则V2O5产品中V2O5的质量分数是(6)从无机层获得Fe(OH)3的离子方程式是
(7)硫酸铝铵固体中含有少量硫酸铵杂质,根据如图的溶解度曲线,进一步提纯硫酸铝铵的操作是加热溶解、

您最近一年使用:0次
2023-10-22更新
|
649次组卷
|
2卷引用:北京市清华大学附属中学2023-2024学年高三上学期10月月考化学试题
9 . 选择完成下列实验的装置。

(1)加热 和
和 固体的混合物制
固体的混合物制 ,用
,用__________ (填序号,下同)。
(2)从盐水中获得食盐,用__________ 。
(3)实验室收集 ,用
,用__________ 。

(1)加热
 和
和 固体的混合物制
固体的混合物制 ,用
,用(2)从盐水中获得食盐,用
(3)实验室收集
 ,用
,用
您最近一年使用:0次
10 . 选择完成下列实验的装置。
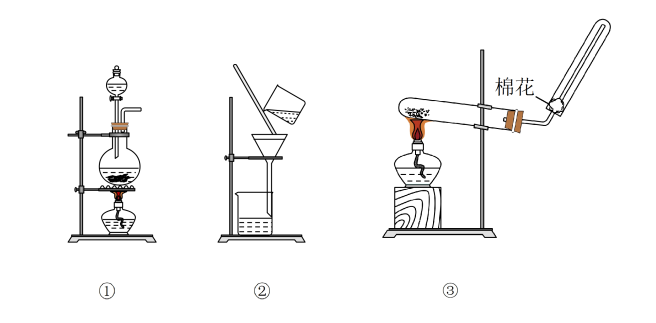
(1)用 和
和 制取
制取 ,用
,用___________ (填序号,下同)。
(2)实验室用二氧化锰和浓盐酸制氯气,用___________ 。
(3)除去粗盐水中的泥沙,用___________ 。

(1)用
 和
和 制取
制取 ,用
,用(2)实验室用二氧化锰和浓盐酸制氯气,用
(3)除去粗盐水中的泥沙,用
您最近一年使用:0次



