名校
解题方法
1 . 完成下列问题。
(1)下列做法中,符合“低碳”理念的是________ (填字母序号)
A.开发使用新能源汽车 B.“焚烧法”处理垃圾 C.大力发展火力发电
D.使用太阳能热水器 E.大力发展风力发电
(2)幼儿和青少年缺___________ 会患佝偻病和发育不良。
(3)如图是A、B、C三种物质的溶解度曲线图。请回答:

①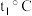 时,溶解度相等的两种物质是
时,溶解度相等的两种物质是________ 。
②B的饱和溶液中混有少量的物质A,要除去A得到较纯的B物质,可采用的结晶方法是___________ 。
③如图所示,在大烧杯中加入一定量的硝酸铵固体后,甲试管内出现的现象是___________ ,乙试管内的溶液为___________ (填“饱和”或“不饱和”)溶液。

(1)下列做法中,符合“低碳”理念的是
A.开发使用新能源汽车 B.“焚烧法”处理垃圾 C.大力发展火力发电
D.使用太阳能热水器 E.大力发展风力发电
(2)幼儿和青少年缺
(3)如图是A、B、C三种物质的溶解度曲线图。请回答:

①
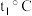 时,溶解度相等的两种物质是
时,溶解度相等的两种物质是②B的饱和溶液中混有少量的物质A,要除去A得到较纯的B物质,可采用的结晶方法是
③如图所示,在大烧杯中加入一定量的硝酸铵固体后,甲试管内出现的现象是

您最近一年使用:0次
名校
解题方法
2 . 经检测,某化工厂排出的废水呈酸性,且其中含有大量  、
、 、
、 、
、 、
、 。回答下列问题:
。回答下列问题:
(1)下列离子中,能大量存在于该废水中的是_______ 填标号
填标号
(2)取 该废水于烧杯,逐滴加入
该废水于烧杯,逐滴加入 溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是
溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是 、
、____  用离子符号表示
用离子符号表示 。
。
(3)某化学社团小组成员欲除去废水样品中的 和
和 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图:

 试剂
试剂 为
为_______  写化学式
写化学式 ;溶液
;溶液 所含溶质离子有
所含溶质离子有 、
、________ 。
 “分离操作”的名称是
“分离操作”的名称是______ ,需用到的玻璃仪器主要有______ 。
 向“白色沉淀
向“白色沉淀 ”中加入足量盐酸,发生反应的离子方程式为
”中加入足量盐酸,发生反应的离子方程式为______ 。
 、
、 、
、 、
、 、
、 。回答下列问题:
。回答下列问题:(1)下列离子中,能大量存在于该废水中的是_______
 填标号
填标号
A. | B. | C. | D. |
 该废水于烧杯,逐滴加入
该废水于烧杯,逐滴加入 溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是
溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是 、
、 用离子符号表示
用离子符号表示 。
。(3)某化学社团小组成员欲除去废水样品中的
 和
和 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图:
 试剂
试剂 为
为 写化学式
写化学式 ;溶液
;溶液 所含溶质离子有
所含溶质离子有 、
、 “分离操作”的名称是
“分离操作”的名称是 向“白色沉淀
向“白色沉淀 ”中加入足量盐酸,发生反应的离子方程式为
”中加入足量盐酸,发生反应的离子方程式为
您最近一年使用:0次
2023-07-30更新
|
533次组卷
|
8卷引用:广西南宁市沛鸿民族中学2023-2024学年高一上学期10月月考化学试题
3 . 唐朝初年,瘟疫频发,人们把它归因于一种叫“年”的怪兽。一位叫李田的人就把硝石、硫磺和木炭装在竹筒里,点燃后驱赶怪兽。后来人们靠此驱散了山林瘴气,战胜了疫情。中国古代四大发明之一的“黑火药”是由“一硫二硝三木炭”混合而成。
(1)写出“黑火药”爆炸的化学反应方程式___________ 。
(2)“黑火药”爆炸时,空气中还弥漫着一层淡淡的刺鼻的 气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是
气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是___________ (用文字表述,任写一条合理途径)。
(3)某同学将足量的 通入一支装有氯化钡溶液的试管,未见沉淀生成。若向该试管中加入足量___________(填序号),能产生白色沉淀。
通入一支装有氯化钡溶液的试管,未见沉淀生成。若向该试管中加入足量___________(填序号),能产生白色沉淀。
(4)古代曾用硝土[含有 、少量NaCl等]和草木灰(含有
、少量NaCl等]和草木灰(含有 )作原料制取
)作原料制取 。某化学兴趣小组设计了如下实验流程:
。某化学兴趣小组设计了如下实验流程:

①“反应”过程中的离子反应方程式为___________ 。
②如图所示是硝酸钾和氯化钠的溶解度曲线。“一系列操作”包括将滤液___________ 、过滤洗涤、干燥等步骤。

(5)现代国防开矿等使用的烈性炸药,主要成分为硝化甘油 (
(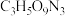 ),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸)。
),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸)。
①硝化甘油在人体内能缓慢分解出一种双原子明星分子,其相对分子量是30,少量的该分子在人体内会促进血管扩张,防止血管栓塞,因此,被广泛用于治疗心绞痛,该明星分子的化学式为___________ ;
②实验室制备硝化甘油的化学方程式为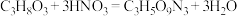 ,用足量浓硝酸、浓硫酸和
,用足量浓硝酸、浓硫酸和 mL
mL  g/cm
g/cm 甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。该装置中仪器a名称为
甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。该装置中仪器a名称为___________ 。

③反应得到16g硝化甘油,则产率为___________ (保留整数)。
(1)写出“黑火药”爆炸的化学反应方程式
(2)“黑火药”爆炸时,空气中还弥漫着一层淡淡的刺鼻的
 气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是
气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是(3)某同学将足量的
 通入一支装有氯化钡溶液的试管,未见沉淀生成。若向该试管中加入足量___________(填序号),能产生白色沉淀。
通入一支装有氯化钡溶液的试管,未见沉淀生成。若向该试管中加入足量___________(填序号),能产生白色沉淀。| A.硝酸钾溶液 | B.稀盐酸 | C.氨水 | D.硫化钠溶液 |
 、少量NaCl等]和草木灰(含有
、少量NaCl等]和草木灰(含有 )作原料制取
)作原料制取 。某化学兴趣小组设计了如下实验流程:
。某化学兴趣小组设计了如下实验流程:
①“反应”过程中的离子反应方程式为
②如图所示是硝酸钾和氯化钠的溶解度曲线。“一系列操作”包括将滤液

(5)现代国防开矿等使用的烈性炸药,主要成分为硝化甘油
 (
(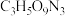 ),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸)。
),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸)。①硝化甘油在人体内能缓慢分解出一种双原子明星分子,其相对分子量是30,少量的该分子在人体内会促进血管扩张,防止血管栓塞,因此,被广泛用于治疗心绞痛,该明星分子的化学式为
②实验室制备硝化甘油的化学方程式为
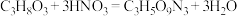 ,用足量浓硝酸、浓硫酸和
,用足量浓硝酸、浓硫酸和 mL
mL  g/cm
g/cm 甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。该装置中仪器a名称为
甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。该装置中仪器a名称为
③反应得到16g硝化甘油,则产率为
您最近一年使用:0次
名校
解题方法
4 . 钇是稀土元素之一。我国蕴藏着丰富的钇矿石(Y2FeBe2Si2O10),用NaOH初步处理钇矿石可以得到Y(OH)3、Fe2O3、Na2SiO3和Na2BeO2的共熔物。工业上利用该共熔物制取氧化钇,并获得副产物铍,流程如图:
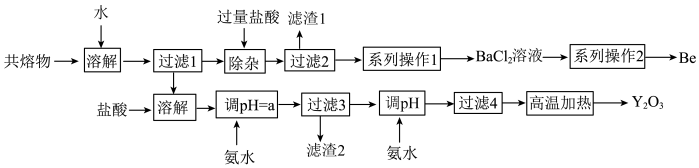
已知i.铍和铝处于元素周期表的对角线位置,化学性质相似;
ii.Fe3+、Y3+形成氢氧化物沉淀时的pH如表:
(1)滤渣1的主要成分是_______ 。
(2)过滤2所得滤液中含有NaCl、BeCl2和少量HCl。为提纯BeCl2。选择合理步骤并排序完成系列操作1_______ 。
a.加入适量的盐酸
b.通入过量的CO2
c.过滤
d.加入过量的NaOH溶液
e.加入过量的氨水
f.洗涤
(3)由BeCl2溶液制得BeCl2固体的操作为_______ 。
(4)用氨水调节pH=a时,a的取值范围是_______ 。
(5)计算常温下Y3++3H2O Y(OH)3+3H+的平衡常数K=
Y(OH)3+3H+的平衡常数K=_______ 。(常温下Ksp[Y(OH)3]=8.0×10-23)
(6)“除杂”中Na2BeO2与过量盐酸反应的离子方程式为_______ 。
(7)常见的由BeCl2固体生产Be的工业方法有两种:①电解法:电解NaCl-BeCl2混合熔融盐制备Be;②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并说明理由_______ 。

已知i.铍和铝处于元素周期表的对角线位置,化学性质相似;
ii.Fe3+、Y3+形成氢氧化物沉淀时的pH如表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.1 | 3.1 |
| Y3+ | 6.0 | 8.3 |
(2)过滤2所得滤液中含有NaCl、BeCl2和少量HCl。为提纯BeCl2。选择合理步骤并排序完成系列操作1
a.加入适量的盐酸
b.通入过量的CO2
c.过滤
d.加入过量的NaOH溶液
e.加入过量的氨水
f.洗涤
(3)由BeCl2溶液制得BeCl2固体的操作为
(4)用氨水调节pH=a时,a的取值范围是
(5)计算常温下Y3++3H2O
 Y(OH)3+3H+的平衡常数K=
Y(OH)3+3H+的平衡常数K=(6)“除杂”中Na2BeO2与过量盐酸反应的离子方程式为
(7)常见的由BeCl2固体生产Be的工业方法有两种:①电解法:电解NaCl-BeCl2混合熔融盐制备Be;②热还原法:熔融条件下,钾还原BeCl2制备Be。以上两种方法你认为哪种更好并说明理由
您最近一年使用:0次
解题方法
5 . 回答下列问题:
(1)浓硫酸有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的性质是_______。
(2)海水中所得粗盐中通常含 、
、 、
、 等杂质。
等杂质。
①为了得到精盐,下列试剂加入的先后顺序正确的是_______ 。
A.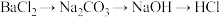 B.
B.
C. D.
D.
②为了检验精盐中是否含有 ,正确的方法是
,正确的方法是_______ 。
(3)月壤中含有丰富的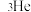 ,从月壤中提炼
,从月壤中提炼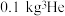 同时可得
同时可得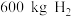 和
和 ,若以所得
,若以所得 和
和 为原料经一系列反应最多可制得碳酸氢铵
为原料经一系列反应最多可制得碳酸氢铵_______  。
。
(4)将 溶液和
溶液和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液温度,实验结果如图所示
溶液混合均匀后测量并记录溶液温度,实验结果如图所示 已知:实验中始终保持
已知:实验中始终保持 ,酸碱恰好完全反应时,体系的温度最高
,酸碱恰好完全反应时,体系的温度最高 。请按要求填空:
。请按要求填空:
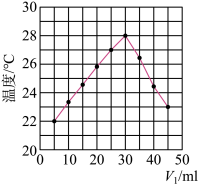
该实验表明此反应_______  填“吸收”或“释放”
填“吸收”或“释放” 能量,由图示分析可以得出做该实验时,环境温度
能量,由图示分析可以得出做该实验时,环境温度_______  填“高于”“低于”或“等于
填“高于”“低于”或“等于 。根据图示计算该
。根据图示计算该 溶液的浓度约是
溶液的浓度约是_______  。
。
(5)设计实验方案:选择合适的试剂,用二氧化硅制硅酸_______ 。(用流程图表达,例:A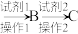 ……)
……)
(1)浓硫酸有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的性质是_______。
| A.酸性 | B.脱水性 | C.强氧化性 | D.吸水性 |
 、
、 、
、 等杂质。
等杂质。①为了得到精盐,下列试剂加入的先后顺序正确的是
A.
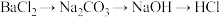 B.
B.
C.
 D.
D.
②为了检验精盐中是否含有
 ,正确的方法是
,正确的方法是(3)月壤中含有丰富的
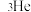 ,从月壤中提炼
,从月壤中提炼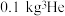 同时可得
同时可得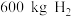 和
和 ,若以所得
,若以所得 和
和 为原料经一系列反应最多可制得碳酸氢铵
为原料经一系列反应最多可制得碳酸氢铵 。
。(4)将
 溶液和
溶液和 未知浓度的
未知浓度的 溶液混合均匀后测量并记录溶液温度,实验结果如图所示
溶液混合均匀后测量并记录溶液温度,实验结果如图所示 已知:实验中始终保持
已知:实验中始终保持 ,酸碱恰好完全反应时,体系的温度最高
,酸碱恰好完全反应时,体系的温度最高 。请按要求填空:
。请按要求填空:
该实验表明此反应
 填“吸收”或“释放”
填“吸收”或“释放” 能量,由图示分析可以得出做该实验时,环境温度
能量,由图示分析可以得出做该实验时,环境温度 填“高于”“低于”或“等于
填“高于”“低于”或“等于 。根据图示计算该
。根据图示计算该 溶液的浓度约是
溶液的浓度约是 。
。(5)设计实验方案:选择合适的试剂,用二氧化硅制硅酸
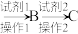 ……)
……)
您最近一年使用:0次



