解题方法
1 . 海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示:

(1)写出工业上由食盐制备
 的离子方程式:
的离子方程式:(2)步骤Ⅰ中已获得
 ,步骤Ⅱ中又将
,步骤Ⅱ中又将 转化为
转化为 和
和 ,其目的是
,其目的是(3)步骤Ⅱ中通入热空气吹出
 ,利用了
,利用了 的___________(填标号)。
的___________(填标号)。| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
(4)步骤Ⅱ中用纯碱溶液吸收
 ,该反应的化学方程式为
,该反应的化学方程式为(5)从理论上考虑,下列物质也能吸收
 的是___________(填标号)。
的是___________(填标号)。A. | B.NaCl溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
(6)查阅资料知,
 的沸点为58.8 ℃,微溶于水,有毒性和强腐蚀性。步骤Ⅲ中对蒸馏烧瓶采取的加热方式是
的沸点为58.8 ℃,微溶于水,有毒性和强腐蚀性。步骤Ⅲ中对蒸馏烧瓶采取的加热方式是
您最近一年使用:0次
名校
2 . 现有甲、乙、丙三名同学分别进行 胶体的制备实验。
胶体的制备实验。
甲同学:向饱和 溶液中加少量NaOH溶液。乙同学:直接加热饱和
溶液中加少量NaOH溶液。乙同学:直接加热饱和 溶液。
溶液。
丙同学:向25mL沸水中逐滴加入5~6滴 饱和溶液,继续煮沸至溶液呈红褐色,停止加热。回答下列问题:
饱和溶液,继续煮沸至溶液呈红褐色,停止加热。回答下列问题:
(1)操作正确的同学是_______ (填“甲”“乙”或“丙”),该正确操作的化学方程式为_______ 。
(2)证明有 胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是
胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是_______ 。
(3)丙同学在做实验时加热时间过长,结果形成了悬浊液,导致胶体发生了_______ 现象。
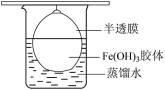
(4)戊同学认为制备的 胶体中混有
胶体中混有 杂质,采用如图所示装置进行提纯,该操作名称为
杂质,采用如图所示装置进行提纯,该操作名称为_______ ,放置2min后,取少量半透膜(完好)外的液体于试管中,向试管中加入用稀硝酸酸化的 溶液,可观察到的现象为
溶液,可观察到的现象为_______ 。
 胶体的制备实验。
胶体的制备实验。甲同学:向饱和
 溶液中加少量NaOH溶液。乙同学:直接加热饱和
溶液中加少量NaOH溶液。乙同学:直接加热饱和 溶液。
溶液。丙同学:向25mL沸水中逐滴加入5~6滴
 饱和溶液,继续煮沸至溶液呈红褐色,停止加热。回答下列问题:
饱和溶液,继续煮沸至溶液呈红褐色,停止加热。回答下列问题:(1)操作正确的同学是
(2)证明有
 胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是
胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是(3)丙同学在做实验时加热时间过长,结果形成了悬浊液,导致胶体发生了
(4)戊同学认为制备的
 胶体中混有
胶体中混有 杂质,采用如图所示装置进行提纯,该操作名称为
杂质,采用如图所示装置进行提纯,该操作名称为 溶液,可观察到的现象为
溶液,可观察到的现象为
您最近一年使用:0次
3 . 自1943年侯德榜先生发明侯氏制碱法以来,我国纯碱工业高速发展。纯碱作为基本化工原料,被广泛应用于造纸、冶金、纺织、石油、国防、医药等领域,纯碱同时也是制造其他化学品的原料。可以用如图装置模拟侯氏制碱法,根据所学知识回答下列问题:

(1)仪器 的名称为
的名称为_____ ;仪器 的作用为
的作用为_____ 。
(2)装置 中生成
中生成 的反应的化学方程式为
的反应的化学方程式为_____ 。装置C中反应的离子方程式为_____ 。
(3)通过对粗盐(含有 杂质,杂质在实际生产中还容易造成设备堵塞)进行精制可制得饱和
杂质,杂质在实际生产中还容易造成设备堵塞)进行精制可制得饱和 溶液,涉及步骤如下:
溶液,涉及步骤如下:
①加入过量 溶液②加入过量
溶液②加入过量 溶液③加入足量盐酸④过滤⑤蒸发浓缩⑥加入过量
溶液③加入足量盐酸④过滤⑤蒸发浓缩⑥加入过量 溶液正确的操作顺序为_____(填标号)。
溶液正确的操作顺序为_____(填标号)。
(4)实验室模拟侯氏制碱法首先制得的是 ,然后将其在
,然后将其在_____ (填仪器名称)中,进一步制得纯碱。
(5)在实际生产中为了得到更多的产品,经常加入适量的食盐促进产品的析出,这会导致所得的 产品中混有少量
产品中混有少量 。为了确定加热后固体的组成,某化学兴趣小组准确称取
。为了确定加热后固体的组成,某化学兴趣小组准确称取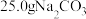 产品,配制成
产品,配制成 溶液,向所得溶液中加入
溶液,向所得溶液中加入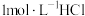 溶液,所得气体体积(已折算为标准状况)与加入盐酸体积的关系如图所示。
溶液,所得气体体积(已折算为标准状况)与加入盐酸体积的关系如图所示。
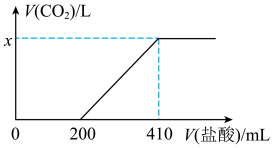
①由已知条件及图像分析, 产品中的杂质为
产品中的杂质为_____ (填化学式)。
②图中
_____ ;若每制得 该样品平均消耗标准状况下
该样品平均消耗标准状况下 ,则在合成
,则在合成 时
时 的转化率为
的转化率为_____ (保留两位小数)%。

(1)仪器
 的名称为
的名称为 的作用为
的作用为(2)装置
 中生成
中生成 的反应的化学方程式为
的反应的化学方程式为(3)通过对粗盐(含有
 杂质,杂质在实际生产中还容易造成设备堵塞)进行精制可制得饱和
杂质,杂质在实际生产中还容易造成设备堵塞)进行精制可制得饱和 溶液,涉及步骤如下:
溶液,涉及步骤如下:①加入过量
 溶液②加入过量
溶液②加入过量 溶液③加入足量盐酸④过滤⑤蒸发浓缩⑥加入过量
溶液③加入足量盐酸④过滤⑤蒸发浓缩⑥加入过量 溶液正确的操作顺序为_____(填标号)。
溶液正确的操作顺序为_____(填标号)。| A.①④⑥④②④③⑤ | B.⑥①②④③⑤ |
| C.②⑥①④③⑤ | D.⑥①②③④⑤ |
(4)实验室模拟侯氏制碱法首先制得的是
 ,然后将其在
,然后将其在(5)在实际生产中为了得到更多的产品,经常加入适量的食盐促进产品的析出,这会导致所得的
 产品中混有少量
产品中混有少量 。为了确定加热后固体的组成,某化学兴趣小组准确称取
。为了确定加热后固体的组成,某化学兴趣小组准确称取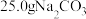 产品,配制成
产品,配制成 溶液,向所得溶液中加入
溶液,向所得溶液中加入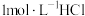 溶液,所得气体体积(已折算为标准状况)与加入盐酸体积的关系如图所示。
溶液,所得气体体积(已折算为标准状况)与加入盐酸体积的关系如图所示。
①由已知条件及图像分析,
 产品中的杂质为
产品中的杂质为②图中

 该样品平均消耗标准状况下
该样品平均消耗标准状况下 ,则在合成
,则在合成 时
时 的转化率为
的转化率为
您最近一年使用:0次
2023-11-22更新
|
444次组卷
|
2卷引用:云南省昆明市部分学校2023-2024学年高二上学期期中联考化学试题
解题方法
4 . 某溶液只含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子且各离子的浓度均相同。为确定具体离子种类(不考虑溶液中微量的离子),某同学进行了如下实验:
中的几种离子且各离子的浓度均相同。为确定具体离子种类(不考虑溶液中微量的离子),某同学进行了如下实验:
i.向100mL溶液中加入过量的 溶液,有白色沉淀产生,过滤、洗涤、干燥,所得沉淀的总质量为19.7g。
溶液,有白色沉淀产生,过滤、洗涤、干燥,所得沉淀的总质量为19.7g。
ii.将i中沉淀加入足量稀盐酸中,沉淀完全消失,有气体产生。
回答下列问题:
(1)i中生成的白色沉淀为_______ ;过滤使用到的玻璃仪器有玻璃棒、烧杯、________ 。
(2)ii中发生反应的离子方程式为___________ ,生成的气体的体积为___________ L(换算成标准状况)。
(3)该溶液中含有的离子为________ (填离子符号),离子浓度均为___________  。
。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子且各离子的浓度均相同。为确定具体离子种类(不考虑溶液中微量的离子),某同学进行了如下实验:
中的几种离子且各离子的浓度均相同。为确定具体离子种类(不考虑溶液中微量的离子),某同学进行了如下实验:i.向100mL溶液中加入过量的
 溶液,有白色沉淀产生,过滤、洗涤、干燥,所得沉淀的总质量为19.7g。
溶液,有白色沉淀产生,过滤、洗涤、干燥,所得沉淀的总质量为19.7g。ii.将i中沉淀加入足量稀盐酸中,沉淀完全消失,有气体产生。
回答下列问题:
(1)i中生成的白色沉淀为
(2)ii中发生反应的离子方程式为
(3)该溶液中含有的离子为
 。
。
您最近一年使用:0次
解题方法
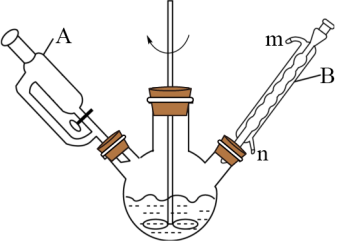
5 . 山梨酸酯具有解毒作用,可以减轻肝脏负担,促进肝细胞修复,保护肝脏健康。实验室用如图1所示装置(夹持、加热装置省略),依据下面的原理制备山梨酸正丁酯。
实验步骤:
①在三颈烧瓶中加入16.8g山梨酸、7.4g正丁醇、少量催化剂和几粒沸石,水浴加热三颈烧瓶,使反应体系保持微沸。
②回流4小时后停止加热和搅拌,反应液冷却至室温。
③滤去催化剂和沸石,将滤液倒入200mL水中,加入50mL乙醚,倒入分液漏斗中,分液。
④分离出的有机层先用ρ=10mg/L的NaHCO3溶液洗涤至中性,再用水洗涤分液,收集有机层。
⑤在有机层中加入少量无水MgSO4,静置片刻,过滤。
⑥将滤液进行蒸馏,除去杂质得到纯净的山梨酸正丁酯6.0g。回答下列问题:
(1)仪器A的名称是_______ ;仪器B的作用是_______ ,冷却水由_______ (填“m”或“n”)口通入。
(2)洗涤、分液过程中,加入ρ=10mg/L的NaHCO3溶液的目的是_______ ,若改为加入NaOH的浓溶液,是否可行_______ (填“是”或“否”),原因是:_______ 。
(3)在实验步骤④中加入少量无水MgSO₄的目的是_______
(4)在实验步骤⑥中进行蒸馏,蒸馏至120℃除去的杂质是_______ 。
(5)本实验中,山梨酸正丁酯的产率是_______ (精确至0.1%)。
(6)为了提高反应正向进行的程度,实验室常使用如图2所示装置(夹持、加热装置已略去)代替图1装置制备山梨酸正丁酯以提高产物的产率,请结合环己烷的物理性质,解释在该装置中环己烷的主要作用_______ 。
反应方程式如下: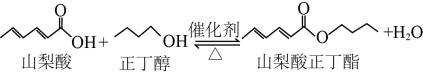
| 物质 | 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 水溶性 |
| 山梨酸 | 112 | 1.204 | 228 | 易溶 |
| 正丁醇 | 74 | 0.8089 | 117 | 溶 |
| 山梨酸正丁酯 | 168 | 0.926 | 195 | 难溶 |
| 乙醚 | 74 | 0.714 | 34.6 | 难溶 |
| 环己烷 | 84 | 0.779 | 80.7 | 难溶 |
①在三颈烧瓶中加入16.8g山梨酸、7.4g正丁醇、少量催化剂和几粒沸石,水浴加热三颈烧瓶,使反应体系保持微沸。
②回流4小时后停止加热和搅拌,反应液冷却至室温。
③滤去催化剂和沸石,将滤液倒入200mL水中,加入50mL乙醚,倒入分液漏斗中,分液。
④分离出的有机层先用ρ=10mg/L的NaHCO3溶液洗涤至中性,再用水洗涤分液,收集有机层。
⑤在有机层中加入少量无水MgSO4,静置片刻,过滤。
⑥将滤液进行蒸馏,除去杂质得到纯净的山梨酸正丁酯6.0g。回答下列问题:
(1)仪器A的名称是
(2)洗涤、分液过程中,加入ρ=10mg/L的NaHCO3溶液的目的是
(3)在实验步骤④中加入少量无水MgSO₄的目的是
(4)在实验步骤⑥中进行蒸馏,蒸馏至120℃除去的杂质是
(5)本实验中,山梨酸正丁酯的产率是
(6)为了提高反应正向进行的程度,实验室常使用如图2所示装置(夹持、加热装置已略去)代替图1装置制备山梨酸正丁酯以提高产物的产率,请结合环己烷的物理性质,解释在该装置中环己烷的主要作用

您最近一年使用:0次
2023-11-04更新
|
488次组卷
|
2卷引用:云南省大理白族自治州2023-2024学年高三上学期第一次复习统一检测理科综合化学试题
6 . 现有 、
、 、
、 和
和 的混合物,选择适当的试剂除去杂质,从而得到纯净的
的混合物,选择适当的试剂除去杂质,从而得到纯净的 晶体,相应的实验流程如图所示。请回答下列问题:
晶体,相应的实验流程如图所示。请回答下列问题:
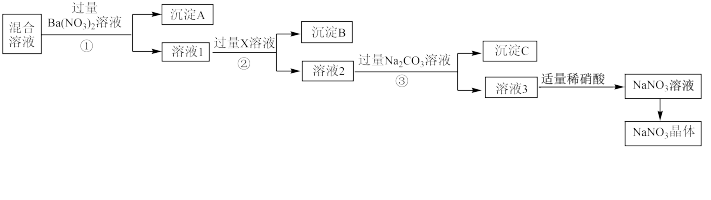
(1)沉淀 的主要成分是
的主要成分是 ___________ 。 填化学式
填化学式
(2)试剂 是
是___________ 。
(3)上述实验流程中 操作名称为
操作名称为___________ ,用到的玻璃仪器有___________ 。
(4)上述实验流程中加入过量 溶液的目的是
溶液的目的是___________ 。
(5)按此实验方案得到的溶液 中肯定含有杂质,可以向溶液
中肯定含有杂质,可以向溶液 中加入适量稀硝酸除去杂质,写出流程④除杂反应的离子方程式:
中加入适量稀硝酸除去杂质,写出流程④除杂反应的离子方程式:___________ 。
 、
、 、
、 和
和 的混合物,选择适当的试剂除去杂质,从而得到纯净的
的混合物,选择适当的试剂除去杂质,从而得到纯净的 晶体,相应的实验流程如图所示。请回答下列问题:
晶体,相应的实验流程如图所示。请回答下列问题:
(1)沉淀
 的主要成分是
的主要成分是  填化学式
填化学式
(2)试剂
 是
是(3)上述实验流程中
 操作名称为
操作名称为(4)上述实验流程中加入过量
 溶液的目的是
溶液的目的是(5)按此实验方案得到的溶液
 中肯定含有杂质,可以向溶液
中肯定含有杂质,可以向溶液 中加入适量稀硝酸除去杂质,写出流程④除杂反应的离子方程式:
中加入适量稀硝酸除去杂质,写出流程④除杂反应的离子方程式:
您最近一年使用:0次



