1 . 下列物质是生产、生活中常见的物质。
① 固体 ②葡萄糖 ③稀硫酸 ④铝箔 ⑤
固体 ②葡萄糖 ③稀硫酸 ④铝箔 ⑤ 固体 ⑥粒子直径为1nm~100nm的
固体 ⑥粒子直径为1nm~100nm的 ⑦乙醇(
⑦乙醇( ) ⑧饱和食盐水
) ⑧饱和食盐水
请回答下列问题:
(1)以上物质中属于电解质的是___________ (填序号,下同)。
(2)以上物质在该状态下能导电的是___________ 。
(3)将⑥均匀地分散在水中,形成的分散系属于___________ ,可用的鉴别原理是___________ 。
(4) 在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
在实验室和工业上均有重要应用,其工业制备的部分工艺如下:

资料:软锰矿的主要成分为 ,
, 。为暗绿色固体,在强碱性溶液中稳定存在,在近中性或酸性溶液中易发生歧化反应(Mn的化合价既升高又降低)。
。为暗绿色固体,在强碱性溶液中稳定存在,在近中性或酸性溶液中易发生歧化反应(Mn的化合价既升高又降低)。
a.写出“焙烧”时生成 的化学方程式:
的化学方程式:___________ 。
b.过滤需要使用的玻璃仪器除漏斗外,还有___________ 。
c.通入 可发生歧化反应,有
可发生歧化反应,有 生成,写出
生成,写出 与
与 反应的化学方程式:
反应的化学方程式:___________ 。
d.高锰酸钾在酸性介质中的强氧化性广泛应用于分析化学中,配平以下反应方程式。___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
①
 固体 ②葡萄糖 ③稀硫酸 ④铝箔 ⑤
固体 ②葡萄糖 ③稀硫酸 ④铝箔 ⑤ 固体 ⑥粒子直径为1nm~100nm的
固体 ⑥粒子直径为1nm~100nm的 ⑦乙醇(
⑦乙醇( ) ⑧饱和食盐水
) ⑧饱和食盐水请回答下列问题:
(1)以上物质中属于电解质的是
(2)以上物质在该状态下能导电的是
(3)将⑥均匀地分散在水中,形成的分散系属于
(4)
 在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
在实验室和工业上均有重要应用,其工业制备的部分工艺如下:
资料:软锰矿的主要成分为
 ,
, 。为暗绿色固体,在强碱性溶液中稳定存在,在近中性或酸性溶液中易发生歧化反应(Mn的化合价既升高又降低)。
。为暗绿色固体,在强碱性溶液中稳定存在,在近中性或酸性溶液中易发生歧化反应(Mn的化合价既升高又降低)。a.写出“焙烧”时生成
 的化学方程式:
的化学方程式:b.过滤需要使用的玻璃仪器除漏斗外,还有
c.通入
 可发生歧化反应,有
可发生歧化反应,有 生成,写出
生成,写出 与
与 反应的化学方程式:
反应的化学方程式:d.高锰酸钾在酸性介质中的强氧化性广泛应用于分析化学中,配平以下反应方程式。
___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
您最近一年使用:0次
名校
解题方法
2 . 铈(Ce)是一种典型的稀土元素,属于国家战略资源。以某废料(主要含 ,还含少量
,还含少量 、
、 、
、 及微量MnO)为原料可制备无水氯化铈
及微量MnO)为原料可制备无水氯化铈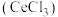 ,主要步骤如下:
,主要步骤如下:
(1)酸浸:用稀硫酸和双氧水的混合溶液浸取废料粉末,浸取液中含有 、
、 、
、 、
、 等金属阳离子。已知
等金属阳离子。已知 不溶于水,写出其发生反应的离子方程式:
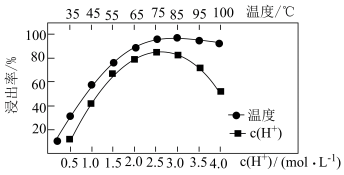
不溶于水,写出其发生反应的离子方程式:________ 。Ce的浸出率与 、温度的关系如图所示。生产中应选择的适宜条件为
、温度的关系如图所示。生产中应选择的适宜条件为________ 。
(2)除杂:向浸出液中加入NaOH溶液调节pH除去 、
、 。注:当
。注:当 时,
时, 沉淀开始溶解。有关沉淀数据(25℃)如下表(“完全沉淀”时金属离子浓度
沉淀开始溶解。有关沉淀数据(25℃)如下表(“完全沉淀”时金属离子浓度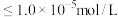 )。
)。
则 的
的
________ ,若浸取液中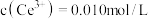 ,则须调节溶液pH的范围是
,则须调节溶液pH的范围是________ (加入NaOH溶液过程忽略体积变化)。
(3)萃取与反萃取:向除杂后的溶液中,加入有机物HT,发生反应: (水层)+3HT(有机层)
(水层)+3HT(有机层)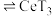 (有机层)
(有机层)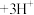 (水层)。向分离所得有机层中加入
(水层)。向分离所得有机层中加入_______ 能获得较纯的 溶液。
溶液。
结晶析出:将 溶液蒸发浓缩、冷却结晶,过滤,得到
溶液蒸发浓缩、冷却结晶,过滤,得到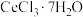 晶体。
晶体。
(4)加热脱水:将 固体和
固体和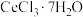 混合,在真空中加热可得无水
混合,在真空中加热可得无水 。加入
。加入 固体的作用是
固体的作用是________ 。
(5)对 样品纯度进行测定的方法:准确称取样品62.50g,配成1000mL溶液,取50.00mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵
样品纯度进行测定的方法:准确称取样品62.50g,配成1000mL溶液,取50.00mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵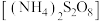 溶液使
溶液使 被氧化为
被氧化为 ,萃取剂萃取
,萃取剂萃取 ,再用
,再用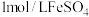 标准溶液滴定至终点,重复2~3次,平均消耗标准液10.00mL,则
标准溶液滴定至终点,重复2~3次,平均消耗标准液10.00mL,则 样品的纯度为
样品的纯度为________ %(保留小数点后两位)。
 ,还含少量
,还含少量 、
、 、
、 及微量MnO)为原料可制备无水氯化铈
及微量MnO)为原料可制备无水氯化铈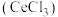 ,主要步骤如下:
,主要步骤如下:(1)酸浸:用稀硫酸和双氧水的混合溶液浸取废料粉末,浸取液中含有
 、
、 、
、 、
、 等金属阳离子。已知
等金属阳离子。已知 不溶于水,写出其发生反应的离子方程式:
不溶于水,写出其发生反应的离子方程式: 、温度的关系如图所示。生产中应选择的适宜条件为
、温度的关系如图所示。生产中应选择的适宜条件为
(2)除杂:向浸出液中加入NaOH溶液调节pH除去
 、
、 。注:当
。注:当 时,
时, 沉淀开始溶解。有关沉淀数据(25℃)如下表(“完全沉淀”时金属离子浓度
沉淀开始溶解。有关沉淀数据(25℃)如下表(“完全沉淀”时金属离子浓度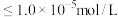 )。
)。沉淀 |
|
|
|
|
恰好完全沉淀时pH | 5.2 | 2.8 | 9.0 | 10.1 |
 的
的
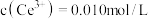 ,则须调节溶液pH的范围是
,则须调节溶液pH的范围是(3)萃取与反萃取:向除杂后的溶液中,加入有机物HT,发生反应:
 (水层)+3HT(有机层)
(水层)+3HT(有机层)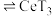 (有机层)
(有机层)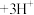 (水层)。向分离所得有机层中加入
(水层)。向分离所得有机层中加入 溶液。
溶液。结晶析出:将
 溶液蒸发浓缩、冷却结晶,过滤,得到
溶液蒸发浓缩、冷却结晶,过滤,得到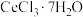 晶体。
晶体。(4)加热脱水:将
 固体和
固体和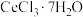 混合,在真空中加热可得无水
混合,在真空中加热可得无水 。加入
。加入 固体的作用是
固体的作用是(5)对
 样品纯度进行测定的方法:准确称取样品62.50g,配成1000mL溶液,取50.00mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵
样品纯度进行测定的方法:准确称取样品62.50g,配成1000mL溶液,取50.00mL上述溶液置于锥形瓶中,加入稍过量的过二硫酸铵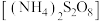 溶液使
溶液使 被氧化为
被氧化为 ,萃取剂萃取
,萃取剂萃取 ,再用
,再用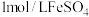 标准溶液滴定至终点,重复2~3次,平均消耗标准液10.00mL,则
标准溶液滴定至终点,重复2~3次,平均消耗标准液10.00mL,则 样品的纯度为
样品的纯度为
您最近一年使用:0次
2023-08-08更新
|
434次组卷
|
2卷引用:辽宁省丹东市等2地大石桥市第三高级中学等2校2022-2023学年高三上学期1月期末考试化学试题
名校
解题方法
3 . 硅是带来人类文明的重要元素之一,硅与二氧化硅广泛应用于通讯行业。
(1)工业上常用石英砂与焦炭在高温下反应制粗硅,其化学方程式是___________ 。
(2)工业上可以通过如图所示的流程制取纯硅:___________ 。
②整个过程中必须严格控制无氧。在有氧环境下,除了有不安全因素外还可能使产品中混有杂质___________ 。整个过程中可以循环利用的物质是___________ (填化学式)。
(3)如图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。___________ 。
②将洗净的石英砂研磨成粉末,目的是___________ 。
③在以上流程中,能否将盐酸改为NaOH溶液,请说明理由___________ 。
(1)工业上常用石英砂与焦炭在高温下反应制粗硅,其化学方程式是
(2)工业上可以通过如图所示的流程制取纯硅:
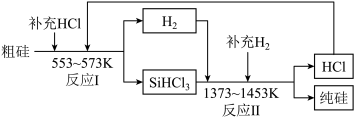
②整个过程中必须严格控制无氧。在有氧环境下,除了有不安全因素外还可能使产品中混有杂质
(3)如图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。
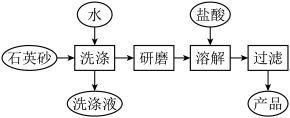
②将洗净的石英砂研磨成粉末,目的是
③在以上流程中,能否将盐酸改为NaOH溶液,请说明理由
您最近一年使用:0次
2023-07-06更新
|
199次组卷
|
4卷引用:辽宁省沈阳市第二中学2022-2023学年高一下学期第一阶段测试化学试题
4 . 海洋中蕴含着丰富的资源,我们通过“浓缩、氧化、提取”等步骤获取溴、碘单质等资源。回答下列问题:
Ⅰ.为研究海水提溴工艺,甲、乙两同学分别设计了如下实验流程:
甲:苦卤 含溴海水
含溴海水 含溴空气
含溴空气 溴水混合物
溴水混合物 溴蒸气
溴蒸气 液溴
液溴
乙:苦卤 含溴海水
含溴海水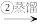 溴蒸气
溴蒸气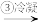 液溴
液溴
(1)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中较符合实际工业生产要求且能耗较低的是___________ (填“甲”或“乙”)。
(2)甲同学设计的流程中,步骤③通入热空气或水蒸气吹出Br2,利用了溴的___________ 性;步骤④中发生反应的化学方程式为 ___________ 。
Ⅱ.对比溴元素的提取,碘元素是从海洋植物如海带、海藻中提取,某提取碘单质的工艺流程如图。___________ ;步骤④的离子方程式为 ___________ 。
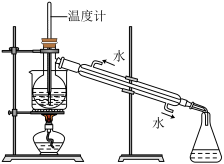
(4)从含碘的某溶液中提取碘,还要经过蒸馏,指出下列蒸馏装置中的错误之处:________ (任写两点)。
Ⅰ.为研究海水提溴工艺,甲、乙两同学分别设计了如下实验流程:
甲:苦卤
 含溴海水
含溴海水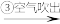 含溴空气
含溴空气 溴水混合物
溴水混合物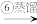 溴蒸气
溴蒸气 液溴
液溴乙:苦卤
 含溴海水
含溴海水 溴蒸气
溴蒸气 液溴
液溴(1)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中较符合实际工业生产要求且能耗较低的是
(2)甲同学设计的流程中,步骤③通入热空气或水蒸气吹出Br2,利用了溴的
Ⅱ.对比溴元素的提取,碘元素是从海洋植物如海带、海藻中提取,某提取碘单质的工艺流程如图。

(4)从含碘的某溶液中提取碘,还要经过蒸馏,指出下列蒸馏装置中的错误之处:
您最近一年使用:0次
2023-05-30更新
|
231次组卷
|
6卷引用:辽宁省凌源市普通高中2022-2023学年高一下学期6月月考化学试题
辽宁省凌源市普通高中2022-2023学年高一下学期6月月考化学试题河南省洛阳强基联盟2022-2023学年高一下学期5月联考化学试题黑龙江省哈尔滨市2022-2023学年高一下学期学业质量检测化学试题青海省西宁市大通回族土族自治县2022-2023学年高一下学期期末考试化学试题甘肃省永昌县第一高级中学2022-2023学年高一下学期期末考试化学试题(已下线)专题06 化学与可持续发展-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)





