名校
1 . 化学实验 化学是一门以实验为基础的学科。请回答以下问题:
(1)对下列事实的解释正确的是
(2)将盛有 12 mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积是
(3)CuBr 是一种白色晶体,见光或潮湿时受热易分解。实验室制备CuBr的反应原理为SO2+2CuSO4+2NaBr+2H2O=2CuBr+2H2SO4+Na2SO4,用下列装置进行实验,不能达到实验目的的是

(4)实验室中要制取少量蒸馏水,其装置如下图所示:
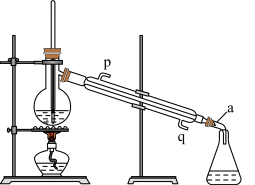
①仪器 a 的名称为_______ ,冷凝水应从_______ (选填“p”或“q”)口进入冷凝管。
②请指出图中装置的一处明显错误:_______ 。
③现需480 mL 0.1 mol/L 的CuSO4溶液,所需的玻璃仪器有烧杯、胶头滴管、_____ 、_____ ; 在配制过程中,需要用电子天平称取胆矾的质量为_______ g。
(5)某校为了改进碳与浓硝酸反应的实验,设计了如图所示的装置。实验步骤:先预热盛有无水氯化钙的烧瓶,然后投入几小块红热的炭块,再缓缓向炭块上滴加浓硝酸,反应即可连续发生。请完成下列空白。
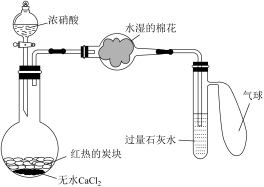
①烧瓶中反应的化学方程式为_______ ,烧瓶中的现象是_______ 。
②水湿棉花的作用是_______ ,气球的作用是_______ 。
(1)对下列事实的解释正确的是
| A.蘸有浓硫酸和蘸有浓氨水的玻璃棒靠近没有白烟,说明硫酸与氨气不反应 |
| B.医疗上可用硫酸钡作 X 射线透视肠胃的内服药,是因为硫酸钡不溶于酸 |
| C.向 50 mL 18 mol·L-1的H2SO4溶液中加入足量的铜片加热充分反应后,被还原的H2SO4的物质的量为0.45 mol |
| D.常温下,浓H2SO4可以用铝制容器贮存,说明铝与浓硫酸不反应 |
| A.1.2mL | B.2.4 mL | C.3.6mL | D.4mL |

| A.用装置甲制取 SO2 | B.用装置乙制取 CuBr |
| C.用装置丙避光将 CuBr 与母液分离 | D.用装置丁干燥 CuBr |

①仪器 a 的名称为
②请指出图中装置的一处明显错误:
③现需480 mL 0.1 mol/L 的CuSO4溶液,所需的玻璃仪器有烧杯、胶头滴管、
(5)某校为了改进碳与浓硝酸反应的实验,设计了如图所示的装置。实验步骤:先预热盛有无水氯化钙的烧瓶,然后投入几小块红热的炭块,再缓缓向炭块上滴加浓硝酸,反应即可连续发生。请完成下列空白。

①烧瓶中反应的化学方程式为
②水湿棉花的作用是
您最近一年使用:0次
名校
解题方法
2 . 将少量饱和 溶液分别滴加到下列物质中,得到三种不同的分散系,回答下列问题。
溶液分别滴加到下列物质中,得到三种不同的分散系,回答下列问题。
甲:将饱和 溶液滴加到冷水中。
溶液滴加到冷水中。
乙:将饱和 溶液滴加到NaOH溶液中。
溶液滴加到NaOH溶液中。
丙:将饱和 溶液滴加到沸水中。
溶液滴加到沸水中。
(1)甲属于_______ (填“溶液”或“胶体”或“浊液”),其颜色是_______ 。
(2)乙中分散质粒子直径范围是_______ 。
(3)将乙分散系过滤,向滤渣中加入盐酸,反应的离子方程式为_______ 。
(4)将丙继续加热煮沸得到红褐色透明液体,反应的离子方程式为_______ 。可以用简单的方法判断丙中是否成功制备胶体,该方法是_______ 。
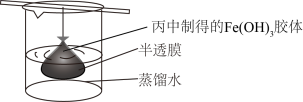
(5)可用如图所示的装置除去 胶体中的杂质离子来提纯
胶体中的杂质离子来提纯 胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入
胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入 溶液,若
溶液,若_______ (填实验现象),则说明该 胶体中的杂质离子已经完全除去。
胶体中的杂质离子已经完全除去。
 溶液分别滴加到下列物质中,得到三种不同的分散系,回答下列问题。
溶液分别滴加到下列物质中,得到三种不同的分散系,回答下列问题。甲:将饱和
 溶液滴加到冷水中。
溶液滴加到冷水中。乙:将饱和
 溶液滴加到NaOH溶液中。
溶液滴加到NaOH溶液中。丙:将饱和
 溶液滴加到沸水中。
溶液滴加到沸水中。(1)甲属于
(2)乙中分散质粒子直径范围是
(3)将乙分散系过滤,向滤渣中加入盐酸,反应的离子方程式为
(4)将丙继续加热煮沸得到红褐色透明液体,反应的离子方程式为
(5)可用如图所示的装置除去
 胶体中的杂质离子来提纯
胶体中的杂质离子来提纯 胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入
胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入 溶液,若
溶液,若 胶体中的杂质离子已经完全除去。
胶体中的杂质离子已经完全除去。
您最近一年使用:0次
解题方法
3 . 亚铁盐由于具有较强的还原性,久置于空气中容易氧化变质,日常实验中常以复盐硫酸亚铁铵晶体 代替绿矾(
代替绿矾( )等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
)等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
(1)①在制备硫酸亚铁铵晶体时,为了防止被氧化,需除去溶解氧,所配制 溶液、
溶液、 溶液等都必须预先经过
溶液等都必须预先经过___________ (操作)处理后再使用。向 溶液中加入饱和
溶液中加入饱和 溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
②在上述洗涤操作步骤中,下列蒸馏水最适合作为洗涤剂的是___________ (填字母)。
A.沸水 B.冰水 C.温水 D.常温
(2)取少量制得晶体按下图进行实验,
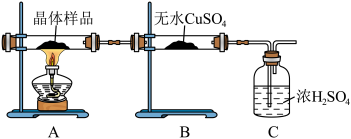
①若B装置中无水 变蓝证明含有结晶水,C装置的作用是
变蓝证明含有结晶水,C装置的作用是___________ 。
②另取少量晶体于试管中,加水溶解,___________ (填操作与现象),证明晶体中有 ,用相关的离子方程式说明产生该现象的原理:
,用相关的离子方程式说明产生该现象的原理:___________ 。
 代替绿矾(
代替绿矾( )等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
)等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:| 溶剂 | 蒸馏水 | ||||
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 9.8 | 22.0 | 28.2 | 35.7 | 45.2 |
(1)①在制备硫酸亚铁铵晶体时,为了防止被氧化,需除去溶解氧,所配制
 溶液、
溶液、 溶液等都必须预先经过
溶液等都必须预先经过 溶液中加入饱和
溶液中加入饱和 溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。②在上述洗涤操作步骤中,下列蒸馏水最适合作为洗涤剂的是
A.沸水 B.冰水 C.温水 D.常温
(2)取少量制得晶体按下图进行实验,

①若B装置中无水
 变蓝证明含有结晶水,C装置的作用是
变蓝证明含有结晶水,C装置的作用是②另取少量晶体于试管中,加水溶解,
 ,用相关的离子方程式说明产生该现象的原理:
,用相关的离子方程式说明产生该现象的原理:
您最近一年使用:0次
名校
4 . FeCl3是实验室常见的药品,将少量FeCl3饱和溶液分别滴加到下列物质中,可得到三种分散系。

回答下列问题:
(1)可判断丙中成功制备胶体的是_________
(2)关于分散系的下列说法中,正确的是_________
(3)用括号中注明的方法分离下列各组混合物,其中正确的是_________
(4)丙中溶液液体呈透明的红褐色,发生反应的化学方程式为___________ 。
(5)现有另一胶体丁,向丁中插入电极通电,胶体粒子移向电源正极相连的一极,说明该胶体粒子带___________ 电荷;将丁与丙混合,可观察到___________ 现象。
(6)用如图所示的装置来提纯丙中制得的胶体,实验过程中需不断更换烧杯中的蒸馏水。证明胶体中杂质离子已经完全除去的方法是___________ 。

(7)四氯化碳也是一种重要的含氯化合物,其沸点约为76℃。碘单质沸点为184℃。若要从含碘的四氯化碳中提取碘和回收四氯化碳,还需要经过蒸馏,装置如图(加热和夹持装置已略去)。冷凝水应从___________ (填a或b)口通入,该装置使用水浴加热的优点是___________ ,最后晶态碘在___________ 里聚集(填仪器名称)。


回答下列问题:
(1)可判断丙中成功制备胶体的是_________
| A.布朗运动 | B.丁达尔现象 |
| C.形成分散系 | D.形成澄清透明的液体 |
(2)关于分散系的下列说法中,正确的是_________
| A.分散系一定是混合物 | B.分散剂一定是液体 |
| C.一种分散系里只能有一种分散质 | D.胆矾、空气、有色玻璃都是分散系 |
(3)用括号中注明的方法分离下列各组混合物,其中正确的是_________
| A.溴的四氯化碳溶液(分液) |
| B.淀粉和水(过滤) |
| C.KCl和MnO2(溶解过滤,再蒸发结晶) |
| D.碘和蒸馏水(萃取) |
(4)丙中溶液液体呈透明的红褐色,发生反应的化学方程式为
(5)现有另一胶体丁,向丁中插入电极通电,胶体粒子移向电源正极相连的一极,说明该胶体粒子带
(6)用如图所示的装置来提纯丙中制得的胶体,实验过程中需不断更换烧杯中的蒸馏水。证明胶体中杂质离子已经完全除去的方法是

(7)四氯化碳也是一种重要的含氯化合物,其沸点约为76℃。碘单质沸点为184℃。若要从含碘的四氯化碳中提取碘和回收四氯化碳,还需要经过蒸馏,装置如图(加热和夹持装置已略去)。冷凝水应从

您最近一年使用:0次
名校
5 . 现有甲、乙、丙三名同学分别进行 胶体的制备实验。
胶体的制备实验。
甲同学:向饱和 溶液中加少量NaOH溶液。乙同学:直接加热饱和
溶液中加少量NaOH溶液。乙同学:直接加热饱和 溶液。
溶液。
丙同学:向25mL沸水中逐滴加入5~6滴 饱和溶液,继续煮沸至溶液呈红褐色,停止加热。回答下列问题:
饱和溶液,继续煮沸至溶液呈红褐色,停止加热。回答下列问题:
(1)操作正确的同学是_______ (填“甲”“乙”或“丙”),该正确操作的化学方程式为_______ 。
(2)证明有 胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是
胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是_______ 。
(3)丙同学在做实验时加热时间过长,结果形成了悬浊液,导致胶体发生了_______ 现象。
(4)戊同学认为制备的 胶体中混有
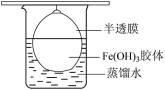
胶体中混有 杂质,采用如图所示装置进行提纯,该操作名称为
杂质,采用如图所示装置进行提纯,该操作名称为_______ ,放置2min后,取少量半透膜(完好)外的液体于试管中,向试管中加入用稀硝酸酸化的 溶液,可观察到的现象为
溶液,可观察到的现象为_______ 。
 胶体的制备实验。
胶体的制备实验。甲同学:向饱和
 溶液中加少量NaOH溶液。乙同学:直接加热饱和
溶液中加少量NaOH溶液。乙同学:直接加热饱和 溶液。
溶液。丙同学:向25mL沸水中逐滴加入5~6滴
 饱和溶液,继续煮沸至溶液呈红褐色,停止加热。回答下列问题:
饱和溶液,继续煮沸至溶液呈红褐色,停止加热。回答下列问题:(1)操作正确的同学是
(2)证明有
 胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是
胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是(3)丙同学在做实验时加热时间过长,结果形成了悬浊液,导致胶体发生了
(4)戊同学认为制备的
 胶体中混有
胶体中混有 杂质,采用如图所示装置进行提纯,该操作名称为
杂质,采用如图所示装置进行提纯,该操作名称为 溶液,可观察到的现象为
溶液,可观察到的现象为
您最近一年使用:0次
名校
解题方法
6 . 氯酸钾为无色或白色晶体,是一种强氧化剂。某化学小组制取氯酸钾并进行有关探究实验。
I.制取氯酸钾
利用如图所示的实验装置进行实验。回答下列问题:
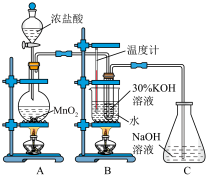
(1)装置A中盛装浓盐酸的仪器名称是___________ 。
(2)装置A中发生反应的离子方程式为___________ 。
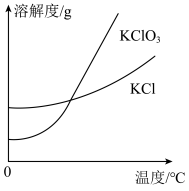
(3)氯气和氢氧化钾溶液在加热的条件下可制得氯酸钾,若装置B中加热温度过低,所得主要氧化产物为___________ (填化学式)。已知氯酸钾和氯化钾的溶解度曲线如图所示,反应结束后,从装置B所得溶液中提取氯酸钾晶体的实验操作是蒸发浓缩、___________ 、洗涤、干燥。
II.探究氯酸钾与碘化钾的反应
(4)在不同条件下KClO3可将KI氧化为I2或KIO3.室温下,该小组设计了系列实验研究硫酸浓度对反应产物的影响,实验记录如下表:
①3号试管实验中x的值为___________ ;1号试管实验的作用是___________ 。
②假设氧化产物唯一,还原产物为KCl,2号试管中主要反应的离子方程式为___________ 。
③由该系列实验可得出的结论是___________ 。
I.制取氯酸钾
利用如图所示的实验装置进行实验。回答下列问题:

(1)装置A中盛装浓盐酸的仪器名称是
(2)装置A中发生反应的离子方程式为
(3)氯气和氢氧化钾溶液在加热的条件下可制得氯酸钾,若装置B中加热温度过低,所得主要氧化产物为

II.探究氯酸钾与碘化钾的反应
(4)在不同条件下KClO3可将KI氧化为I2或KIO3.室温下,该小组设计了系列实验研究硫酸浓度对反应产物的影响,实验记录如下表:
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol·L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol·L-1H2SO4/mL | 0 | 3.0 | x | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 5.0 | 0 |
| 取少量反应后溶液滴加淀粉溶液 | 无现象 | 变蓝 | 变蓝 | 无现象 |
②假设氧化产物唯一,还原产物为KCl,2号试管中主要反应的离子方程式为
③由该系列实验可得出的结论是
您最近一年使用:0次
2023-11-13更新
|
433次组卷
|
2卷引用:广东省汕头市潮阳实验学校2024届高三上学期期中考试化学试题
名校
解题方法
7 . 碘化钾( )是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为
)是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为 和
和 )制备碘化钾的实验步骤如下:
)制备碘化钾的实验步骤如下:
步骤Ⅰ:取含碘废液,调节溶液 为
为 ,加入一定量
,加入一定量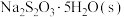 ,溶解,加热至30℃,加入稍过量
,溶解,加热至30℃,加入稍过量 粉末,搅拌,充分反应后,过滤得
粉末,搅拌,充分反应后,过滤得 沉淀;
沉淀;
步骤Ⅱ:在 圆底烧瓶中加入上述制备的
圆底烧瓶中加入上述制备的 沉淀,铁粉(过量),
沉淀,铁粉(过量), 蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入
蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入 烧杯中,加入约
烧杯中,加入约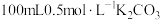 溶液,搅拌,煮沸,静置,过滤,得滤液A;
溶液,搅拌,煮沸,静置,过滤,得滤液A;
步骤Ⅲ:用氢碘酸调滤液A的 ,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到
,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到 晶体。
晶体。
回答下列问题:
(1)步骤Ⅰ中的控温方法为___________ , 与
与 转化为
转化为 的反应为①
的反应为① ,②
,② ,则反应②中氧化剂与还原剂的物质的量之比为
,则反应②中氧化剂与还原剂的物质的量之比为___________ 。
(2)步骤Ⅱ中铁粉转化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(3)步骤Ⅲ中,仪器的名称是___________ ,现象是___________ 。
(4)产品中KI含量的测定
称取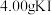 4.00样品,配成
4.00样品,配成 溶液,取
溶液,取 溶液于锥形瓶中,加入
溶液于锥形瓶中,加入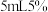 乙酸溶液及3滴曙红钠盐作指示剂,用
乙酸溶液及3滴曙红钠盐作指示剂,用 的
的 标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗
标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗 标准溶液分别为
标准溶液分别为 、
、 、
、 。
。
①用 标准溶液滴定时要避光的原因是
标准溶液滴定时要避光的原因是___________ ,在滴定时 溶液应盛放在
溶液应盛放在___________ (“酸式”或“碱式”)滴定管。
②样品中 的质量分数为
的质量分数为___________ 。
 )是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为
)是实验室常用的化学试剂,用途广泛。一种利用含碘废液(碘的主要存在形式为 和
和 )制备碘化钾的实验步骤如下:
)制备碘化钾的实验步骤如下:步骤Ⅰ:取含碘废液,调节溶液
 为
为 ,加入一定量
,加入一定量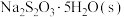 ,溶解,加热至30℃,加入稍过量
,溶解,加热至30℃,加入稍过量 粉末,搅拌,充分反应后,过滤得
粉末,搅拌,充分反应后,过滤得 沉淀;
沉淀;步骤Ⅱ:在
 圆底烧瓶中加入上述制备的
圆底烧瓶中加入上述制备的 沉淀,铁粉(过量),
沉淀,铁粉(过量), 蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入
蒸馏水,搅拌,沸水浴加热1小时,冷却,抽滤。将滤液倒入 烧杯中,加入约
烧杯中,加入约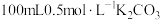 溶液,搅拌,煮沸,静置,过滤,得滤液A;
溶液,搅拌,煮沸,静置,过滤,得滤液A;步骤Ⅲ:用氢碘酸调滤液A的
 ,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到
,将滤液倒入___________(填仪器名称)中加热至___________(填现象),冷却,干燥,得到 晶体。
晶体。回答下列问题:
(1)步骤Ⅰ中的控温方法为
 与
与 转化为
转化为 的反应为①
的反应为① ,②
,② ,则反应②中氧化剂与还原剂的物质的量之比为
,则反应②中氧化剂与还原剂的物质的量之比为(2)步骤Ⅱ中铁粉转化为
 ,该反应的化学方程式为
,该反应的化学方程式为(3)步骤Ⅲ中,仪器的名称是
(4)产品中KI含量的测定
称取
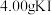 4.00样品,配成
4.00样品,配成 溶液,取
溶液,取 溶液于锥形瓶中,加入
溶液于锥形瓶中,加入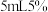 乙酸溶液及3滴曙红钠盐作指示剂,用
乙酸溶液及3滴曙红钠盐作指示剂,用 的
的 标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗
标准溶液避光滴定至沉淀呈红色(终点),平行滴定三次,消耗 标准溶液分别为
标准溶液分别为 、
、 、
、 。
。①用
 标准溶液滴定时要避光的原因是
标准溶液滴定时要避光的原因是 溶液应盛放在
溶液应盛放在②样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2024-01-02更新
|
210次组卷
|
2卷引用:贵州省贵阳市2023-2024学年高三上学期11月质量检测化学试题
名校
8 . 铁及其化合物在日常生产生活中应用广泛,研究铁及其化合物的应用意义重大。
(1)所含铁元素只有还原性的物质是___________。
(2)当人体缺铁时,往往需要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。
①如何检验某固体补铁剂中铁元素已被氧化?写出操作过程、现象及结论。
答:研细后用盐酸溶解,___________ 。
②服用维生素C,可使食物中的三价铁离子转化为二价铁离子。由此可推知,维生素C具有___________ (填化学性质)。
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、C1O-、OH-、FeO 、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:___________
______Fe(OH)3+_______ClO-+_______=_______FeO +_______Cl-+_______
+_______Cl-+_______
(4)工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
①试剂a是___________ ,操作I用到的玻璃仪器有烧杯、玻璃棒和___________ 。
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为___________ 。
③上述流程中操作Ⅲ包括:蒸发浓缩、___________ 、过滤、洗涤。
(1)所含铁元素只有还原性的物质是___________。
| A.Fe | B.FeCl2 | C.FeCl3 | D.Fe2O3 |
(2)当人体缺铁时,往往需要吃补铁保健品。人体能够吸收的是+2价的铁,但是+2价的铁很容易被氧化。
①如何检验某固体补铁剂中铁元素已被氧化?写出操作过程、现象及结论。
答:研细后用盐酸溶解,
②服用维生素C,可使食物中的三价铁离子转化为二价铁离子。由此可推知,维生素C具有
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、C1O-、OH-、FeO
 、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出并配平湿法制高铁酸钾的离子反应方程式:______Fe(OH)3+_______ClO-+_______=_______FeO
 +_______Cl-+_______
+_______Cl-+_______(4)工业上用氯化铁腐蚀铜箔、制造电路板。某工程师为了从使用过的腐蚀废液中回收铜,并获得氯化铁晶体,准备采用下列步骤:

回答下列问题:
①试剂a是
②滤液X、Z中都有同一种溶质,它们转化为溶液W的离子方程式为
③上述流程中操作Ⅲ包括:蒸发浓缩、
您最近一年使用:0次
名校
9 . I.A的结构式如图,完成下列填空。
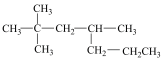
(1)A的一氯代物的同分异构体有___________ 种(不考虑立体异构,下同)。
(2)若A是烯烃B加氢而制得,则这样的烯烃B可能有___________ 种。
Ⅱ.如图,在左试管中先加入2mL95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀。按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验。
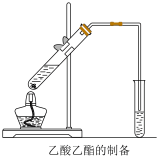
试回答:
(3)在右试管中通常加入___________ 溶液,该溶液的作用是___________ 。分离右试管中所得乙酸乙酯的操作为(只填名称)___________ 。
(4)反应中加入浓硫酸的作用是___________ 。
(5)左试管中发生反应的化学方程式为___________ 。
(6)如果用9.2g的乙醇和18.0g的乙酸反应制得乙酸乙酯10.56g,则本实验的产率是_______ ;(得数保留小数点后一位;产率指的是某种生成物的实际产量与理论产量的比值)。

(1)A的一氯代物的同分异构体有
(2)若A是烯烃B加氢而制得,则这样的烯烃B可能有
Ⅱ.如图,在左试管中先加入2mL95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀。按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验。

试回答:
(3)在右试管中通常加入
(4)反应中加入浓硫酸的作用是
(5)左试管中发生反应的化学方程式为
(6)如果用9.2g的乙醇和18.0g的乙酸反应制得乙酸乙酯10.56g,则本实验的产率是
您最近一年使用:0次
名校
10 . I.如图是利用电化学装置将SO2转化为重要的化工原料H2SO4的原理示意图。
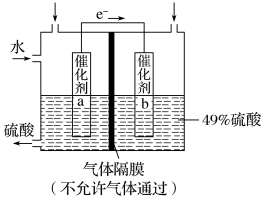
请回答下列问题:
(1)该装置将_______ 能转化为______ 能。
(2)催化剂b表面O2发生_______ 反应,其附近溶液酸性______ (填“增强”、“不变”或“减弱”)。
(3)催化剂a表面的电极反应式:_______ 。
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是______ 。
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是______ 。
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由______ 。
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为______ 。

请回答下列问题:
(1)该装置将
(2)催化剂b表面O2发生
(3)催化剂a表面的电极反应式:
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为
您最近一年使用:0次
2023-05-19更新
|
710次组卷
|
2卷引用:贵州省遵义市仁怀市高中教育联盟2022-2023学年高一下学期5月期中考试化学试题



