名校
1 . FeCl3是实验室常见的药品,将少量FeCl3饱和溶液分别滴加到下列物质中,可得到三种分散系。

回答下列问题:
(1)可判断丙中成功制备胶体的是_________
(2)关于分散系的下列说法中,正确的是_________
(3)用括号中注明的方法分离下列各组混合物,其中正确的是_________
(4)丙中溶液液体呈透明的红褐色,发生反应的化学方程式为___________ 。
(5)现有另一胶体丁,向丁中插入电极通电,胶体粒子移向电源正极相连的一极,说明该胶体粒子带___________ 电荷;将丁与丙混合,可观察到___________ 现象。
(6)用如图所示的装置来提纯丙中制得的胶体,实验过程中需不断更换烧杯中的蒸馏水。证明胶体中杂质离子已经完全除去的方法是___________ 。

(7)四氯化碳也是一种重要的含氯化合物,其沸点约为76℃。碘单质沸点为184℃。若要从含碘的四氯化碳中提取碘和回收四氯化碳,还需要经过蒸馏,装置如图(加热和夹持装置已略去)。冷凝水应从___________ (填a或b)口通入,该装置使用水浴加热的优点是___________ ,最后晶态碘在___________ 里聚集(填仪器名称)。


回答下列问题:
(1)可判断丙中成功制备胶体的是_________
| A.布朗运动 | B.丁达尔现象 |
| C.形成分散系 | D.形成澄清透明的液体 |
(2)关于分散系的下列说法中,正确的是_________
| A.分散系一定是混合物 | B.分散剂一定是液体 |
| C.一种分散系里只能有一种分散质 | D.胆矾、空气、有色玻璃都是分散系 |
(3)用括号中注明的方法分离下列各组混合物,其中正确的是_________
| A.溴的四氯化碳溶液(分液) |
| B.淀粉和水(过滤) |
| C.KCl和MnO2(溶解过滤,再蒸发结晶) |
| D.碘和蒸馏水(萃取) |
(4)丙中溶液液体呈透明的红褐色,发生反应的化学方程式为
(5)现有另一胶体丁,向丁中插入电极通电,胶体粒子移向电源正极相连的一极,说明该胶体粒子带
(6)用如图所示的装置来提纯丙中制得的胶体,实验过程中需不断更换烧杯中的蒸馏水。证明胶体中杂质离子已经完全除去的方法是

(7)四氯化碳也是一种重要的含氯化合物,其沸点约为76℃。碘单质沸点为184℃。若要从含碘的四氯化碳中提取碘和回收四氯化碳,还需要经过蒸馏,装置如图(加热和夹持装置已略去)。冷凝水应从

您最近一年使用:0次
解题方法
2 . 亚铁盐由于具有较强的还原性,久置于空气中容易氧化变质,日常实验中常以复盐硫酸亚铁铵晶体 代替绿矾(
代替绿矾( )等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
)等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
(1)①在制备硫酸亚铁铵晶体时,为了防止被氧化,需除去溶解氧,所配制 溶液、
溶液、 溶液等都必须预先经过
溶液等都必须预先经过___________ (操作)处理后再使用。向 溶液中加入饱和
溶液中加入饱和 溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
②在上述洗涤操作步骤中,下列蒸馏水最适合作为洗涤剂的是___________ (填字母)。
A.沸水 B.冰水 C.温水 D.常温
(2)取少量制得晶体按下图进行实验,
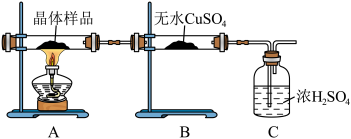
①若B装置中无水 变蓝证明含有结晶水,C装置的作用是
变蓝证明含有结晶水,C装置的作用是___________ 。
②另取少量晶体于试管中,加水溶解,___________ (填操作与现象),证明晶体中有 ,用相关的离子方程式说明产生该现象的原理:
,用相关的离子方程式说明产生该现象的原理:___________ 。
 代替绿矾(
代替绿矾( )等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
)等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:| 溶剂 | 蒸馏水 | ||||
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 9.8 | 22.0 | 28.2 | 35.7 | 45.2 |
(1)①在制备硫酸亚铁铵晶体时,为了防止被氧化,需除去溶解氧,所配制
 溶液、
溶液、 溶液等都必须预先经过
溶液等都必须预先经过 溶液中加入饱和
溶液中加入饱和 溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。②在上述洗涤操作步骤中,下列蒸馏水最适合作为洗涤剂的是
A.沸水 B.冰水 C.温水 D.常温
(2)取少量制得晶体按下图进行实验,

①若B装置中无水
 变蓝证明含有结晶水,C装置的作用是
变蓝证明含有结晶水,C装置的作用是②另取少量晶体于试管中,加水溶解,
 ,用相关的离子方程式说明产生该现象的原理:
,用相关的离子方程式说明产生该现象的原理:
您最近一年使用:0次
3 . 某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取PAFC(聚合氯化铁铝)[AlFe(OH)nCl6-n]m,设计生产流程如下,请回答下列问题:

(1)用10mol/L的浓盐酸配制2mol/L的稀盐酸500mL, 所取浓盐酸的体积________ mL,所用玻璃仪器除量筒、玻璃棒和胶头滴管外,还有_______ 。
A.500mL容量瓶 B.蒸发皿 C.烧瓶
(2)写出Fe2O3粉末与盐酸反应的离子方程式:_______________ 。
(3)取少量酸性溶液滴加几滴KSCN试剂,溶液变为______ 色,证明含有Fe3+。
(4)通入氯气的目的是___________________ 。
(5)加入NaOH调节pH时,氢氧化钠不宜过多,生成一种红褐色沉淀,写出溶液中Fe3+与过量NaOH反应的离子方程式:______________________ 。

(1)用10mol/L的浓盐酸配制2mol/L的稀盐酸500mL, 所取浓盐酸的体积
A.500mL容量瓶 B.蒸发皿 C.烧瓶
(2)写出Fe2O3粉末与盐酸反应的离子方程式:
(3)取少量酸性溶液滴加几滴KSCN试剂,溶液变为
(4)通入氯气的目的是
(5)加入NaOH调节pH时,氢氧化钠不宜过多,生成一种红褐色沉淀,写出溶液中Fe3+与过量NaOH反应的离子方程式:
您最近一年使用:0次
解题方法
4 . 我国拥有很长的海岸线,具有丰富的海洋资源。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。
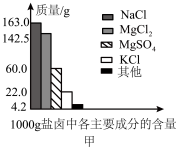
(1)根据图甲所示,写出盐卤中含量最多的盐为___________ (填化学式)其电子式为___________
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到 ℃以上,根据溶解度曲线,首先析出的晶体应是
℃以上,根据溶解度曲线,首先析出的晶体应是___________ 。(填化学式)
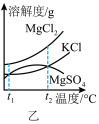
(3)如图是常用于混合物的分离和提纯的装置:
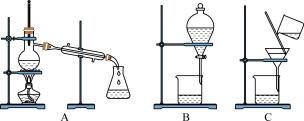
粗盐的提纯应选择图___________ (填字母,下同)装置,若实验中为了除去粗盐中的 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是___________ 。
A.NaOH、Na2CO3、BaCl2、HCl B.NaOH、BaCl2、Na2CO3、HCl
C.Na2CO3、BaCl2、NaOH、HCl D.BaCl2、NaOH、Na2CO3、HCl
Ⅱ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。
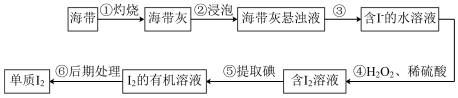
(4)实验步骤①会用到下列仪器中的___________ (填字母)
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中K+的存在,___________ 。
(6)“提取碘”存在以下两种方案。
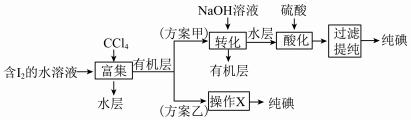
①方案乙中“操作X”的名称是___________ 。
②该流程可循环利用的物质是___________ 。
③采用方案乙得到纯碘的产率较低,原因是___________ 。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。

(1)根据图甲所示,写出盐卤中含量最多的盐为
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到
 ℃以上,根据溶解度曲线,首先析出的晶体应是
℃以上,根据溶解度曲线,首先析出的晶体应是
(3)如图是常用于混合物的分离和提纯的装置:

粗盐的提纯应选择图
 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是A.NaOH、Na2CO3、BaCl2、HCl B.NaOH、BaCl2、Na2CO3、HCl
C.Na2CO3、BaCl2、NaOH、HCl D.BaCl2、NaOH、Na2CO3、HCl
Ⅱ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。

(4)实验步骤①会用到下列仪器中的
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中K+的存在,
(6)“提取碘”存在以下两种方案。

①方案乙中“操作X”的名称是
②该流程可循环利用的物质是
③采用方案乙得到纯碘的产率较低,原因是
您最近一年使用:0次
名校
5 . 现有甲、乙、丙三名同学分别进行 胶体的制备实验。
胶体的制备实验。
甲同学:向饱和 溶液中加少量NaOH溶液。乙同学:直接加热饱和
溶液中加少量NaOH溶液。乙同学:直接加热饱和 溶液。
溶液。
丙同学:向25mL沸水中逐滴加入5~6滴 饱和溶液,继续煮沸至溶液呈红褐色,停止加热。回答下列问题:
饱和溶液,继续煮沸至溶液呈红褐色,停止加热。回答下列问题:
(1)操作正确的同学是_______ (填“甲”“乙”或“丙”),该正确操作的化学方程式为_______ 。
(2)证明有 胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是
胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是_______ 。
(3)丙同学在做实验时加热时间过长,结果形成了悬浊液,导致胶体发生了_______ 现象。
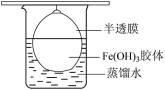
(4)戊同学认为制备的 胶体中混有
胶体中混有 杂质,采用如图所示装置进行提纯,该操作名称为
杂质,采用如图所示装置进行提纯,该操作名称为_______ ,放置2min后,取少量半透膜(完好)外的液体于试管中,向试管中加入用稀硝酸酸化的 溶液,可观察到的现象为
溶液,可观察到的现象为_______ 。
 胶体的制备实验。
胶体的制备实验。甲同学:向饱和
 溶液中加少量NaOH溶液。乙同学:直接加热饱和
溶液中加少量NaOH溶液。乙同学:直接加热饱和 溶液。
溶液。丙同学:向25mL沸水中逐滴加入5~6滴
 饱和溶液,继续煮沸至溶液呈红褐色,停止加热。回答下列问题:
饱和溶液,继续煮沸至溶液呈红褐色,停止加热。回答下列问题:(1)操作正确的同学是
(2)证明有
 胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是
胶体生成的实验操作是用一束强光从侧面照射,观察现象,该过程利用的胶体性质是(3)丙同学在做实验时加热时间过长,结果形成了悬浊液,导致胶体发生了
(4)戊同学认为制备的
 胶体中混有
胶体中混有 杂质,采用如图所示装置进行提纯,该操作名称为
杂质,采用如图所示装置进行提纯,该操作名称为 溶液,可观察到的现象为
溶液,可观察到的现象为
您最近一年使用:0次
名校
6 . I.如图是利用电化学装置将SO2转化为重要的化工原料H2SO4的原理示意图。
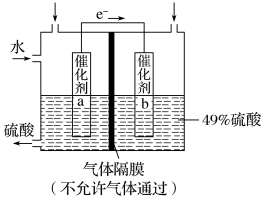
请回答下列问题:
(1)该装置将_______ 能转化为______ 能。
(2)催化剂b表面O2发生_______ 反应,其附近溶液酸性______ (填“增强”、“不变”或“减弱”)。
(3)催化剂a表面的电极反应式:_______ 。
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是______ 。
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是______ 。
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由______ 。
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为______ 。

请回答下列问题:
(1)该装置将
(2)催化剂b表面O2发生
(3)催化剂a表面的电极反应式:
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为
您最近一年使用:0次
2023-05-19更新
|
711次组卷
|
2卷引用:贵州省遵义市仁怀市高中教育联盟2022-2023学年高一下学期5月期中考试化学试题
7 . 海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:
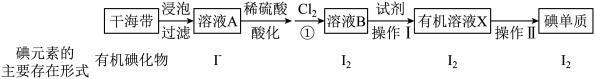
(1)提碘的原料一般选择海带或海藻,是因为_______ 。
(2)在实验室里把有机碘化物转化为碘离子往往需要灼烧操作,灼烧海带需要在_______ 中进行。
(3)若从绿色化学角度考虑,①处选 不好的原因是
不好的原因是_______ 。
(4)操作I中,实验室可用如图仪器将 富集到有机溶液X,该步操作的名称为
富集到有机溶液X,该步操作的名称为_______ ;如图中所选用的有机溶剂可以是_______ (选填编号)。
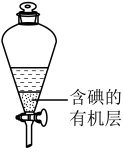
a.酒精b.醋酸c.四氯化碳d.苯
(5)操作I中具体实验步骤为:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.检验分液漏斗旋塞和上口的瓶塞是否漏液;
C.把20mL碘水跟5mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
D.倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收下层溶液;
F.将分液漏斗。上口的玻璃塞打开或使塞上的凹槽对准分液漏斗口上的小孔;
G.从分液漏斗上口倒出上层溶液;
H.静止、分层。
实验步骤的正确顺序为_______ ;_____→_____→_____→A→H→_____→_____→_____。
(6)为寻找氯水的替代品,某同学设计了如下实验来证明 能否代替氯水。实验操作:将
能否代替氯水。实验操作:将 作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,
作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,_______ ,则证明 能代替氯水。请写出此反应的离子方程式
能代替氯水。请写出此反应的离子方程式_______ 。

(1)提碘的原料一般选择海带或海藻,是因为
(2)在实验室里把有机碘化物转化为碘离子往往需要灼烧操作,灼烧海带需要在
(3)若从绿色化学角度考虑,①处选
 不好的原因是
不好的原因是(4)操作I中,实验室可用如图仪器将
 富集到有机溶液X,该步操作的名称为
富集到有机溶液X,该步操作的名称为
a.酒精b.醋酸c.四氯化碳d.苯
(5)操作I中具体实验步骤为:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.检验分液漏斗旋塞和上口的瓶塞是否漏液;
C.把20mL碘水跟5mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
D.倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收下层溶液;
F.将分液漏斗。上口的玻璃塞打开或使塞上的凹槽对准分液漏斗口上的小孔;
G.从分液漏斗上口倒出上层溶液;
H.静止、分层。
实验步骤的正确顺序为
(6)为寻找氯水的替代品,某同学设计了如下实验来证明
 能否代替氯水。实验操作:将
能否代替氯水。实验操作:将 作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中,
作为氧化剂滴加入溶液A中,取少量反应后的溶液于试管中, 能代替氯水。请写出此反应的离子方程式
能代替氯水。请写出此反应的离子方程式
您最近一年使用:0次
名校
8 . “皮鞋很忙”的恶搞段子曾经风靡网络,揭露了某些行业用烂皮鞋制造酸奶或毒胶囊的不法行为。央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铁元素是+2价,则其中铬元素是_______ 价。
(2)明胶的水溶液和K2SO4溶液共同具备的性质是_______ (填序号)。
a.都不稳定,密封放置沉淀 b.分散质粒子可通过滤纸 c.丁达尔效应
(3)制备Fe(OH)3胶体的离子方程式_______ 。
(4)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的方法是_______ ,装置是下列中的_______ (填序号)。

(5)现有10 mL明胶的水溶液与5 mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明SO 能够透过半透膜:
能够透过半透膜:_______ 。
(1)已知Fe(CrO2)2中铁元素是+2价,则其中铬元素是
(2)明胶的水溶液和K2SO4溶液共同具备的性质是
a.都不稳定,密封放置沉淀 b.分散质粒子可通过滤纸 c.丁达尔效应
(3)制备Fe(OH)3胶体的离子方程式
(4)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的方法是

(5)现有10 mL明胶的水溶液与5 mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明SO
 能够透过半透膜:
能够透过半透膜:
您最近一年使用:0次
2022-10-30更新
|
39次组卷
|
2卷引用: 四川省泸州市泸县第四中学2023-2024学年高一上学期10月月考化学试题
名校
9 . 为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格。
| 实验目的 | 试剂及方法 | 供选择的化学试剂及实验方法 |
| 证明炭粉中含有CuO | A.取样,滴加过量氢氧化钠溶液 | |
| 鉴别MgCl2和AlCl3溶液 | B.向溶液中通入足量二氧化碳 | |
| 分离Na2SO4和CaCO3固体混合物 | C.加水溶解、过滤、结晶 | |
| 除去NaHCO3溶液中混有的Na2CO3 | D.取样,滴加稀硫酸 |
您最近一年使用:0次
2022-06-11更新
|
95次组卷
|
2卷引用:福建省泉州市永春第一中学2023-2024学年高三上学期10月阶段检测化学试题
名校
解题方法
10 . 回答下列问题:
I.已知:① ②
② ③
③ ④
④ ⑤稀硫酸 ⑥硼酸 ⑦饱和
⑤稀硫酸 ⑥硼酸 ⑦饱和 溶液 ⑧氨水 ⑨稀硝酸 ⑩硫酸铝。根据上述提供的物质,回答下列问题:
溶液 ⑧氨水 ⑨稀硝酸 ⑩硫酸铝。根据上述提供的物质,回答下列问题:
(1)属于电解质的是_______ 。(填数字序号)
(2) 具有一元弱酸的性质,在水中可产生正四面体结构的离子,写出
具有一元弱酸的性质,在水中可产生正四面体结构的离子,写出 在水中的电离方程式:
在水中的电离方程式:_______ 。
Ⅱ.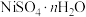 易溶于水,难溶于乙醇,其水溶液显酸性。从电镀污泥中可回收制备
易溶于水,难溶于乙醇,其水溶液显酸性。从电镀污泥中可回收制备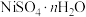 ,采用热重分析法测定所得
,采用热重分析法测定所得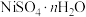 样品所含结晶水数。
样品所含结晶水数。
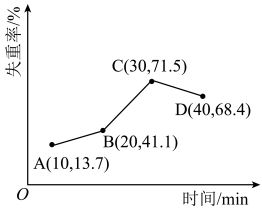
(3)将样品在900℃下进行锻烧,失重率随时间变化如图所示,A点时失掉2个结晶水,n的值为_______ ;C点产物的化学式为_______ 。
(4)高铁酸钾( ,
, 为
为 价)是一种高效水处理剂,具有氧化能力强、安全性好等优点。已知
价)是一种高效水处理剂,具有氧化能力强、安全性好等优点。已知 是紫色固体,可溶于水、微溶于浓
是紫色固体,可溶于水、微溶于浓 溶液。实验室可通过如下反应制取
溶液。实验室可通过如下反应制取 溶液:
溶液: (未配平)。
(未配平)。
①配平反应的方程式,并用单线桥表示电子转移的方向和数目_______ 。
②反应结束后,为从溶液中获得 晶体,可采取的实验操作是
晶体,可采取的实验操作是_______ 。
Ⅲ.锰酸锂离子蓄电池是第二代锂离子动力电池。锰酸锂可充电电池的总反应为 。
。
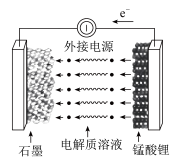
(5)充电时,电池的阳极反应式为_______ ,若此时转移
 ,则石墨电极将增重
,则石墨电极将增重_______ g。
(6)一种锰的硅化物的晶胞结构 如图所示:
如图所示:
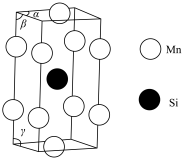
a.基态 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
b.该锰的硅化物的化学式为_______ 。
Ⅳ.我国化学家侯德榜发明了联合制碱法,为世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。
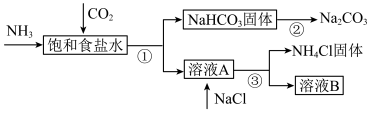
(7)饱和食盐水中通二氧化碳和氨气的离子方程式是_______ 。
(8)下列说法中合理的是_______(填标号)。
I.已知:①
 ②
② ③
③ ④
④ ⑤稀硫酸 ⑥硼酸 ⑦饱和
⑤稀硫酸 ⑥硼酸 ⑦饱和 溶液 ⑧氨水 ⑨稀硝酸 ⑩硫酸铝。根据上述提供的物质,回答下列问题:
溶液 ⑧氨水 ⑨稀硝酸 ⑩硫酸铝。根据上述提供的物质,回答下列问题:(1)属于电解质的是
(2)
 具有一元弱酸的性质,在水中可产生正四面体结构的离子,写出
具有一元弱酸的性质,在水中可产生正四面体结构的离子,写出 在水中的电离方程式:
在水中的电离方程式:Ⅱ.
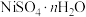 易溶于水,难溶于乙醇,其水溶液显酸性。从电镀污泥中可回收制备
易溶于水,难溶于乙醇,其水溶液显酸性。从电镀污泥中可回收制备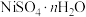 ,采用热重分析法测定所得
,采用热重分析法测定所得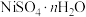 样品所含结晶水数。
样品所含结晶水数。
(3)将样品在900℃下进行锻烧,失重率随时间变化如图所示,A点时失掉2个结晶水,n的值为
(4)高铁酸钾(
 ,
, 为
为 价)是一种高效水处理剂,具有氧化能力强、安全性好等优点。已知
价)是一种高效水处理剂,具有氧化能力强、安全性好等优点。已知 是紫色固体,可溶于水、微溶于浓
是紫色固体,可溶于水、微溶于浓 溶液。实验室可通过如下反应制取
溶液。实验室可通过如下反应制取 溶液:
溶液: (未配平)。
(未配平)。①配平反应的方程式,并用单线桥表示电子转移的方向和数目
②反应结束后,为从溶液中获得
 晶体,可采取的实验操作是
晶体,可采取的实验操作是Ⅲ.锰酸锂离子蓄电池是第二代锂离子动力电池。锰酸锂可充电电池的总反应为
 。
。
(5)充电时,电池的阳极反应式为

 ,则石墨电极将增重
,则石墨电极将增重(6)一种锰的硅化物的晶胞结构
 如图所示:
如图所示:
a.基态
 原子的核外电子排布式为
原子的核外电子排布式为b.该锰的硅化物的化学式为
Ⅳ.我国化学家侯德榜发明了联合制碱法,为世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。

(7)饱和食盐水中通二氧化碳和氨气的离子方程式是
(8)下列说法中合理的是_______(填标号)。
A.副产物 可用作氮肥 可用作氮肥 |
B.溶液B中的主要离子是 、 、 、 、 、 、 |
C.制碱流程中可回收并循环利用的物质只有碳酸氢钠分解产生的 |
| D.饱和食盐水中应该先通二氧化碳至饱和,再通入氨气至饱和 |
您最近一年使用:0次



