1 . 回答下列问题
(1)以下物质:①KCl晶体;②液态HCl;③食盐水;④熔融NaCl;⑤蔗糖;⑥铜;⑦ ;能导电的是
;能导电的是___________ (填序号,下同);属于电解质的是___________ ;属于非电解质的是___________ 。
(2)在离子 中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是___________ 。
(3)用___________ 方法将植物油和水的混合体系分离;用___________ 方法分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合液体(四氯化碳和甲苯互溶)。
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打( ),能治疗胃酸过多,请写出其反应的离子方程式:
),能治疗胃酸过多,请写出其反应的离子方程式:___________ ;此时最好用含氢氧化铝的胃药(如胃舒平)离子方程式:___________ 。
(1)以下物质:①KCl晶体;②液态HCl;③食盐水;④熔融NaCl;⑤蔗糖;⑥铜;⑦
 ;能导电的是
;能导电的是(2)在离子
 中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,氧原子的质子数为8,则R原子核内含有的中子数目是(3)用
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(
 ),能治疗胃酸过多,请写出其反应的离子方程式:
),能治疗胃酸过多,请写出其反应的离子方程式:
您最近一年使用:0次
2 . 为除去粗盐中的Ca2+、Mg2+、Cu2+、SO 以及泥沙等不溶性杂质,某同学设计了一种制备精盐的实验方案,步骤如图
以及泥沙等不溶性杂质,某同学设计了一种制备精盐的实验方案,步骤如图 用于沉淀的试剂稍过量
用于沉淀的试剂稍过量 :
:
称取粗盐 滤液
滤液 粗盐
粗盐
(1)第⑤步过滤后,滤渣中主要含有泥沙、BaSO4、Mg(OH)2、CaCO3、___________ 、___________ (填化学式)。
(2)③、④步所加试剂分别是___________ 、___________ 。
(3)第⑥步中,相关的离子方程式有___________ 。
 以及泥沙等不溶性杂质,某同学设计了一种制备精盐的实验方案,步骤如图
以及泥沙等不溶性杂质,某同学设计了一种制备精盐的实验方案,步骤如图 用于沉淀的试剂稍过量
用于沉淀的试剂稍过量 :
:称取粗盐
 滤液
滤液 粗盐
粗盐(1)第⑤步过滤后,滤渣中主要含有泥沙、BaSO4、Mg(OH)2、CaCO3、
(2)③、④步所加试剂分别是
(3)第⑥步中,相关的离子方程式有
您最近一年使用:0次
3 . (一)现有下列6种物质:①盐酸;②硫酸钠;③二氧化碳;④蔗糖;⑤熔融NaOH;⑥食盐水
(1)上述物质中属于电解质的是__________ (填序号,下同),属于非电解质的是__________ ,
(2)写出②在水中的电离方程式__________ ,请设计实验检验溶液②中的阴离子__________ 。
(二)自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。下列A、B、C、D是中学常见的混合物分离或提纯的装置。
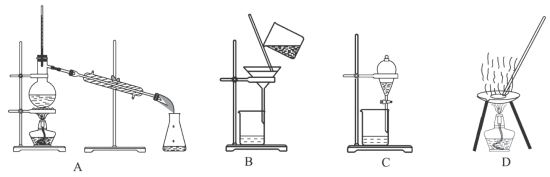
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置,将A、B、C、D序号填入适当的空格中。
(3)碳酸钙悬浊液中分离出碳酸钙__________ ;
(4)分离酒精和水__________ ;
(5)分离植物油和水__________ ;
(6)氯化钠溶液中分离出氯化钠__________ ;
(7)氯化钠溶液中分离出水__________ 。
(1)上述物质中属于电解质的是
(2)写出②在水中的电离方程式
(二)自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。下列A、B、C、D是中学常见的混合物分离或提纯的装置。

请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置,将A、B、C、D序号填入适当的空格中。
(3)碳酸钙悬浊液中分离出碳酸钙
(4)分离酒精和水
(5)分离植物油和水
(6)氯化钠溶液中分离出氯化钠
(7)氯化钠溶液中分离出水
您最近一年使用:0次
解题方法
4 . 化学是一门以实验为基础的学科,化学实验是开展化学研究的重要手段.
(1)检验物质的常用方法有显色法、沉淀法、气体法等。下列物质检验的方法中,不合理的是______ 。
(2)下列物质的分离与提纯的方法中,与物质的溶解度无关的是______ 。
(3)不能用于鉴别Na2CO3和KCl溶液的试剂或方法是______ 。
(4)下列各组溶液中,不用其他试剂就可鉴别的是______ 。
(5)下列检验某无色溶液样品中所含离子的实验,正确的是______ 。
(6)下列关于从碘水中萃取碘的实验中,说法正确的是______ 。
(7)某溶液中存在SO 和Cl-两种负离子,使用以下操作进行检验:①滴加足量的BaCl2溶液;②滴加足量的Ba(NO3)2溶液;③过滤;④加足量的盐酸:⑤滴加AgNO3溶液。正确的操作及顺序是
和Cl-两种负离子,使用以下操作进行检验:①滴加足量的BaCl2溶液;②滴加足量的Ba(NO3)2溶液;③过滤;④加足量的盐酸:⑤滴加AgNO3溶液。正确的操作及顺序是______ 。
(8)某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如表所示,回答:
①三次检测结果中第______ 次检测结果肯定不正确。
②在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子:
第一步:向溶液中滴加过量的______ 溶液(填化学式),其目的是检验CO 并将其除去。
并将其除去。
第二步:加入______ 溶液(填化学式),其目的是______ 。
第三步:过滤,再向滤液中加入______ 溶液(填化学式),其目的是______ 。
(1)检验物质的常用方法有显色法、沉淀法、气体法等。下列物质检验的方法中,不合理的是
| A.酸性溶液:显色法 | B.I2:显色法 |
| C.Cl-:沉淀法 | D.Ca2+:气体法 |
| A.过滤 | B.萃取 | C.结晶 | D.蒸馏 |
| A.盐酸 | B.BaCl2溶液 | C.AgNO3溶液 | D.焰色反应 |
| A.HCl、CuCl2、NaNO3、Na2SO4 |
| B.Na2CO3、Na2SO4、HCl、H2SO4 |
| C.FeCl3、Na2SO4、NaCl、NaOH |
| D.BaCl2、Na2CO3、HCl、NaNO3 |
| A.加AgNO3溶液,生成白色沉淀,可确定有Cl-存在 |
B.加足量稀盐酸,产生无色的气体,可确定有CO 存在 存在 |
C.加足量稀盐酸,无明显现象,再加BaCl2溶液,生成白色沉淀,可确定有SO 存在 存在 |
| D.用洁净的铂丝蘸取溶液,在火焰上灼烧焰色为黄色,可确定含Na+,不含K+ |
| A.萃取剂不能溶于水,且比水更容易使碘溶解 |
| B.注入碘水和萃取剂,倒转分液漏斗反复用力振荡后即可分液 |
| C.萃取时,选用萃取剂的密度必须比水大 |
| D.若没有四氯化碳,可用酒精代替 |
 和Cl-两种负离子,使用以下操作进行检验:①滴加足量的BaCl2溶液;②滴加足量的Ba(NO3)2溶液;③过滤;④加足量的盐酸:⑤滴加AgNO3溶液。正确的操作及顺序是
和Cl-两种负离子,使用以下操作进行检验:①滴加足量的BaCl2溶液;②滴加足量的Ba(NO3)2溶液;③过滤;④加足量的盐酸:⑤滴加AgNO3溶液。正确的操作及顺序是| A.①③⑤ | B.②④③⑤ | C.②③⑤ | D.⑤③① |
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
②在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子:
第一步:向溶液中滴加过量的
 并将其除去。
并将其除去。第二步:加入
第三步:过滤,再向滤液中加入
您最近一年使用:0次
5 . Ⅰ.氯化钠是日常生活必需品和重要的化工原料。海水中含有大量的NaCl。
(1)下列生产过程中只发生物理变化的是__________。
| A.炼铁 | B.海带提碘 | C.氯碱工业 | D.海水晒盐 |
(2)氯化钠属于__________。
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(3)
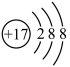 表示__________。
表示__________。| A.氯原子的结构示意图 | B.氯离子的结构示意图 |
| C.氯原子的电子式 | D.氯离子的电子式 |
Ⅱ.实验室提纯粗盐时,将粗盐溶于水后,先除去泥沙等难溶性杂质,再除去 Ca2+、 Mg2+、 等可溶性杂质。
等可溶性杂质。
(4)写出NaCl溶于水时的电离方程式
(5)为了除去可溶性杂质,依次加入稍过量的BaCl2溶液、NaOH溶液和Na2CO3液,加热至70°C左右约2分钟,冷却后过滤,得到的沉淀有BaSO4、Mg(OH)2、CaCO3和
Ⅲ.“84消毒液”是常见的消毒剂,其有效成分是NaClO。
(6)Cl2和NaOH 制备NaClO的化学方程式为
Ⅳ.如图是某品牌“84 消毒液”的使用注意事项。

(7)注意事项4“易使有色衣物脱色”,是因为 “84 消毒液”具有
A.碱性 B.强氧化性
(8)注意事项6“不可与酸性物质同时使用”,例如,若将“84 消毒液”与“洁厕灵”(含盐酸) 同时使用会产生黄绿色有毒气体。写出反应的离子方程式
您最近一年使用:0次
6 . 为除去粗盐中的CaCl2、MgCl2、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):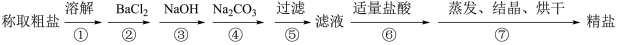
(1)判断BaCl2已过量的方法是___________ 。
(2)第④步中,相关的化学方程式是___________ 。
(3)过滤操作中,需要用到的玻璃仪器有___________ 。
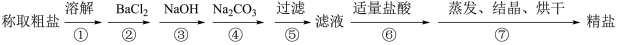
(1)判断BaCl2已过量的方法是
(2)第④步中,相关的化学方程式是
(3)过滤操作中,需要用到的玻璃仪器有
您最近一年使用:0次
解题方法
7 . 亚铁盐由于具有较强的还原性,久置于空气中容易氧化变质,日常实验中常以复盐硫酸亚铁铵晶体 代替绿矾(
代替绿矾( )等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
)等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
(1)①在制备硫酸亚铁铵晶体时,为了防止被氧化,需除去溶解氧,所配制 溶液、
溶液、 溶液等都必须预先经过
溶液等都必须预先经过___________ (操作)处理后再使用。向 溶液中加入饱和
溶液中加入饱和 溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
②在上述洗涤操作步骤中,下列蒸馏水最适合作为洗涤剂的是___________ (填字母)。
A.沸水 B.冰水 C.温水 D.常温
(2)取少量制得晶体按下图进行实验,
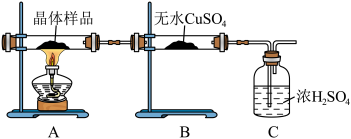
①若B装置中无水 变蓝证明含有结晶水,C装置的作用是
变蓝证明含有结晶水,C装置的作用是___________ 。
②另取少量晶体于试管中,加水溶解,___________ (填操作与现象),证明晶体中有 ,用相关的离子方程式说明产生该现象的原理:
,用相关的离子方程式说明产生该现象的原理:___________ 。
 代替绿矾(
代替绿矾( )等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:
)等亚铁盐使用,这样可以延长保存时间,不易氧化变质。已知:硫酸亚铁铵晶体在蒸馏水中的溶解情况如下表:| 溶剂 | 蒸馏水 | ||||
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 9.8 | 22.0 | 28.2 | 35.7 | 45.2 |
(1)①在制备硫酸亚铁铵晶体时,为了防止被氧化,需除去溶解氧,所配制
 溶液、
溶液、 溶液等都必须预先经过
溶液等都必须预先经过 溶液中加入饱和
溶液中加入饱和 溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。
溶液,经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥后得到一种浅蓝绿色的晶体,此晶体即为硫酸亚铁铵晶体。②在上述洗涤操作步骤中,下列蒸馏水最适合作为洗涤剂的是
A.沸水 B.冰水 C.温水 D.常温
(2)取少量制得晶体按下图进行实验,

①若B装置中无水
 变蓝证明含有结晶水,C装置的作用是
变蓝证明含有结晶水,C装置的作用是②另取少量晶体于试管中,加水溶解,
 ,用相关的离子方程式说明产生该现象的原理:
,用相关的离子方程式说明产生该现象的原理:
您最近一年使用:0次
名校
8 . 生活中无处不化学,请回答下列问题。
I.实验室现有下列物质用于做导电性实验:
①CaO②铜丝③盐酸④稀硫酸⑤二氧化碳气体⑥氨水⑦NaOH粉末⑧蔗糖溶液⑨熔融氯化钠⑩胆矾晶体
请用序号填空:
(1)上述状态下可导电的是___________ 。
(2)属于电解质的是___________ 。
(3)属于非电解质的是___________ 。
II.根据描述书写离子方程式或根据离子方程式写化学方程式:
(4)制备氯气时尾气处理:___________ ;
(5)Na2O2与水反应:___________ ;
(6)Cu2++2OH =Cu(OH)2↓:
=Cu(OH)2↓:___________ 。
III.
(7)为了除去KCl溶液中的CaSO4、MgSO4及泥沙,可将混合物溶于水,然后进行下列五项操作:①过滤;②加过量的KOH溶液;③加适量的盐酸;④加过量的K2CO3溶液;⑤加过量BaCl2溶液。下列操作顺序中最合适的是___________。
I.实验室现有下列物质用于做导电性实验:
①CaO②铜丝③盐酸④稀硫酸⑤二氧化碳气体⑥氨水⑦NaOH粉末⑧蔗糖溶液⑨熔融氯化钠⑩胆矾晶体
请用序号填空:
(1)上述状态下可导电的是
(2)属于电解质的是
(3)属于非电解质的是
II.根据描述书写离子方程式或根据离子方程式写化学方程式:
(4)制备氯气时尾气处理:
(5)Na2O2与水反应:
(6)Cu2++2OH
 =Cu(OH)2↓:
=Cu(OH)2↓:III.
(7)为了除去KCl溶液中的CaSO4、MgSO4及泥沙,可将混合物溶于水,然后进行下列五项操作:①过滤;②加过量的KOH溶液;③加适量的盐酸;④加过量的K2CO3溶液;⑤加过量BaCl2溶液。下列操作顺序中最合适的是___________。
| A.②⑤④①③ | B.④①②⑤③ | C.①④②⑤③ | D.⑤②④③① |
您最近一年使用:0次
名校
9 . 如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
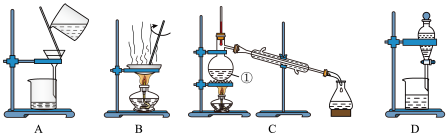
(1)在装置A和装置B中都用到玻璃棒,装置B中玻璃棒的作用是___________ ,防止蒸发皿内溶液因局部过热而溅出。
(2)装置C中①仪器的名称是___________ ,冷却水的方向是___________ 。装置D中分液漏斗使用之前需要___________ 。
(3)从氯化钠溶液中得到氯化钠固体,选择装置___________ (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置___________ ,检验自来水中Cl-是否除净的方法:取少量锥形瓶中的水于洁净试管中,滴加___________ ,不产生白色沉淀表明Cl-已除净;从碘水中分离出I2,选择装置___________ ,该分离方法的名称为___________ 。

(1)在装置A和装置B中都用到玻璃棒,装置B中玻璃棒的作用是
(2)装置C中①仪器的名称是
(3)从氯化钠溶液中得到氯化钠固体,选择装置
您最近一年使用:0次
10 . Ⅰ.现有下列物质:①蔗糖、②Na2CO3溶液、③稀硫酸、④CO2、⑤CuSO4·5H2O固体、⑥石墨棒、⑦含泥沙的氯化钠溶液、⑧淀粉溶液
(1)属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)除去⑦中的泥沙杂质的实验操作方法是___________ 。
(3)将气体④通入②会发生化学反应,其化学方程式为___________ 。
Ⅱ.央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(4)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是___________ 价。Fe(CrO2)2属于___________ (填“酸”、“碱”、“盐”或“氧化物”)。
(5)明胶的水溶液和K2SO4溶液共同具备的性质是___________(填序号)。
(1)属于电解质的是
(2)除去⑦中的泥沙杂质的实验操作方法是
(3)将气体④通入②会发生化学反应,其化学方程式为
Ⅱ.央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(4)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
(5)明胶的水溶液和K2SO4溶液共同具备的性质是___________(填序号)。
| A.都不稳定,密封放置会产生沉淀 | B.分散质粒子可通过滤纸 |
| C.分散质粒子可通过半透膜 | D.二者均有丁达尔效应 |
您最近一年使用:0次



