解题方法
1 . 下列关于容量瓶的操作,不正确的是
A.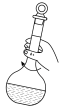 | B.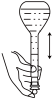 | C. | D.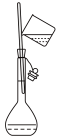 |
您最近一年使用:0次
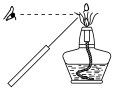
2 . 下列实验能达到目的的是
| A.检验草木灰中含K+ | B.测定氯水的pH | C.验证过氧化钠与水的反应是放热反应 | D.稀释浓硫酸 |
 |  | 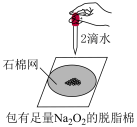 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 三氯化铬是常用的媒染剂和催化剂,易潮解,高温下易被氧气氧化。实验室中用如图所示装置(夹持装置略)制取三氯化铬( 、
、 为气流控制开关)。
为气流控制开关)。

已知:① 气体有毒,能被
气体有毒,能被 溶液吸收,
溶液吸收,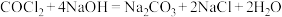 。
。
② 在碱性条件下具有较强还原性,能被
在碱性条件下具有较强还原性,能被 等氧化剂氧化为
等氧化剂氧化为 。
。
③某些物质的颜色、状态、熔点、沸点如下表:
回答下列问题:
(1)制备 的实验步骤如下:
的实验步骤如下:
i.连接装置,检查装置气密性,装入药品,打开 、
、 ,通入
,通入 并通入冷凝水。
并通入冷凝水。
ii.加热管式炉的反应管至 。
。
iii.关闭 (
( 为打开状态),加热
为打开状态),加热 ,温度保持在
,温度保持在 之间。
之间。
iv.加热反应管继续升温至 ,反应所生成的
,反应所生成的 将升华并凝聚在反应管的右端,直到装置
将升华并凝聚在反应管的右端,直到装置 中反应完全,切断管式炉的电源。
中反应完全,切断管式炉的电源。
v.停止加热装置 ,打开
,打开 ,关闭
,关闭 ,继续通入
,继续通入 直至装置
直至装置 中无液滴滴下,停止通入冷凝水。
中无液滴滴下,停止通入冷凝水。
vi.装置冷却后,结束制备实验。
①步骤i中,通 的作用为
的作用为________ 。步骤ⅲ中加热 通常采用的加热方式是
通常采用的加热方式是_________ 。
②步骤iv中装置 中反应完全的标志是
中反应完全的标志是___________ 。
(2)装置 中发生反应的化学方程式为
中发生反应的化学方程式为___________ 。
(3)装置 、
、 的作用是
的作用是___________ 。
(4)准确称取 无水三氯化铬样品置于
无水三氯化铬样品置于 烧杯中,加水定容于
烧杯中,加水定容于 容量瓶中。移取
容量瓶中。移取 于
于 碘量瓶中,加热至沸,慢慢加入
碘量瓶中,加热至沸,慢慢加入 (足量),待溶液变成黄色后,再加水至
(足量),待溶液变成黄色后,再加水至 ,充分加热煮沸,冷却后用
,充分加热煮沸,冷却后用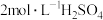 溶液中和至呈橙红色,再加入足量
溶液中和至呈橙红色,再加入足量 溶液,加塞摇匀充分反应后,铬元素只以
溶液,加塞摇匀充分反应后,铬元素只以 存在,暗处静置
存在,暗处静置 后,加入指示剂,用
后,加入指示剂,用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 (已知杂质不参加反应,且
(已知杂质不参加反应,且 )。
)。
①向碘量瓶中加入 后,发生反应的离子方程式为
后,发生反应的离子方程式为___________ 。
②该样品中无水三氯化铬的质量分数为___________ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
 、
、 为气流控制开关)。
为气流控制开关)。
已知:①
 气体有毒,能被
气体有毒,能被 溶液吸收,
溶液吸收,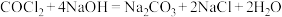 。
。②
 在碱性条件下具有较强还原性,能被
在碱性条件下具有较强还原性,能被 等氧化剂氧化为
等氧化剂氧化为 。
。③某些物质的颜色、状态、熔点、沸点如下表:
| 物质 | 颜色、状态 | 熔点 | 沸点/ |
 | 绿色晶体 | — | — |
 | 紫色晶体 | — | — |
 | 无色液体 | 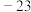 | 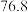 |
(1)制备
 的实验步骤如下:
的实验步骤如下:i.连接装置,检查装置气密性,装入药品,打开
 、
、 ,通入
,通入 并通入冷凝水。
并通入冷凝水。ii.加热管式炉的反应管至
 。
。iii.关闭
 (
( 为打开状态),加热
为打开状态),加热 ,温度保持在
,温度保持在 之间。
之间。iv.加热反应管继续升温至
 ,反应所生成的
,反应所生成的 将升华并凝聚在反应管的右端,直到装置
将升华并凝聚在反应管的右端,直到装置 中反应完全,切断管式炉的电源。
中反应完全,切断管式炉的电源。v.停止加热装置
 ,打开
,打开 ,关闭
,关闭 ,继续通入
,继续通入 直至装置
直至装置 中无液滴滴下,停止通入冷凝水。
中无液滴滴下,停止通入冷凝水。vi.装置冷却后,结束制备实验。
①步骤i中,通
 的作用为
的作用为 通常采用的加热方式是
通常采用的加热方式是②步骤iv中装置
 中反应完全的标志是
中反应完全的标志是(2)装置
 中发生反应的化学方程式为
中发生反应的化学方程式为(3)装置
 、
、 的作用是
的作用是(4)准确称取
 无水三氯化铬样品置于
无水三氯化铬样品置于 烧杯中,加水定容于
烧杯中,加水定容于 容量瓶中。移取
容量瓶中。移取 于
于 碘量瓶中,加热至沸,慢慢加入
碘量瓶中,加热至沸,慢慢加入 (足量),待溶液变成黄色后,再加水至
(足量),待溶液变成黄色后,再加水至 ,充分加热煮沸,冷却后用
,充分加热煮沸,冷却后用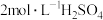 溶液中和至呈橙红色,再加入足量
溶液中和至呈橙红色,再加入足量 溶液,加塞摇匀充分反应后,铬元素只以
溶液,加塞摇匀充分反应后,铬元素只以 存在,暗处静置
存在,暗处静置 后,加入指示剂,用
后,加入指示剂,用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 (已知杂质不参加反应,且
(已知杂质不参加反应,且 )。
)。①向碘量瓶中加入
 后,发生反应的离子方程式为
后,发生反应的离子方程式为②该样品中无水三氯化铬的质量分数为
 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
解题方法
4 . 根据下列实验操作和现象所得到的结论错误 的是
| 实验操作和现象 | 实验结论 | |
| A | 向2mL 溶液中滴加3滴 溶液中滴加3滴 NaOH溶液,再滴加4滴 NaOH溶液,再滴加4滴 溶液,白色沉淀转化为红褐色 溶液,白色沉淀转化为红褐色 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| B | 向盛有某溶液的试管中加入NaOH溶液并加热,将湿润的红色石蕊试纸放在试管口,试纸变蓝 | 某溶液中含有 |
| C | 向1-溴丙烷中加入KOH溶液,加热并充分振荡,然后取少量液体滴入 溶液,出现棕黑色沉淀 溶液,出现棕黑色沉淀 | 1-溴丙烷中混有杂质 |
| D | 铜与浓硫酸在加热条件下反应一段时间,冷却后,将试管里的物质慢慢倒入盛有少量水的另一支试管里,溶液颜色为蓝色 | 铜与浓硫酸生成了硫酸铜 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-15更新
|
298次组卷
|
3卷引用:山西运城盐湖五中2023-2024学年高三上学期期末考试化学试题
解题方法
5 . 某学习小组以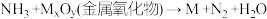 反应为原理设计实验测定金属M的相对原子质量,实验装置如图。
反应为原理设计实验测定金属M的相对原子质量,实验装置如图。
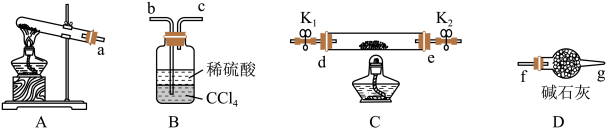
已知,MxOy可为CuO、Fe2O3、MgO;氨气不溶于有机溶剂CCl4.
(1)实验步骤:
①连接实验装置,上述仪器接口顺序为a→_____ (按气流方向从左到右,仪器不重复使用,填标号),检验装置的气密性;
②将m1g纯净的金属氧化物MxOy装入玻璃管C中;
③打开K1和K2,点燃装置A中酒精灯,当装置中充满NH3后再点燃装置C中酒精灯,加热至MxOy反应完全;
④熄灭C中酒精灯,冷却至室温;熄灭A中酒精灯;
⑤冷却至室温后,称量得C中玻璃管剩余固体的质量为m2g。
(2)利用装置A制取氨气的化学方程式为_____ ,列举出一种检验氨气的试剂:_____ 。
(3)仪器D的名称为_____ ;装置B中加入的CCl4的作用是_____ 。
(4)若金属氧化物为CuO,则装置C中发生反应的化学方程式为_____ ,该反应中NH3表现出_____ 性,根据实验记录,算得铜的相对原子质量为_____ (用含m1、m2的式子表示)。
(5)若MxOy未完全反应,则会导致测得的金属M的相对原子质量_____ (填“偏大”、“偏小”或“无影响”)。
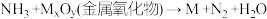 反应为原理设计实验测定金属M的相对原子质量,实验装置如图。
反应为原理设计实验测定金属M的相对原子质量,实验装置如图。
已知,MxOy可为CuO、Fe2O3、MgO;氨气不溶于有机溶剂CCl4.
(1)实验步骤:
①连接实验装置,上述仪器接口顺序为a→
②将m1g纯净的金属氧化物MxOy装入玻璃管C中;
③打开K1和K2,点燃装置A中酒精灯,当装置中充满NH3后再点燃装置C中酒精灯,加热至MxOy反应完全;
④熄灭C中酒精灯,冷却至室温;熄灭A中酒精灯;
⑤冷却至室温后,称量得C中玻璃管剩余固体的质量为m2g。
(2)利用装置A制取氨气的化学方程式为
(3)仪器D的名称为
(4)若金属氧化物为CuO,则装置C中发生反应的化学方程式为
(5)若MxOy未完全反应,则会导致测得的金属M的相对原子质量
您最近一年使用:0次
2023-07-09更新
|
93次组卷
|
2卷引用:山西省忻州市2022-2023学年高一下学期7月期末考试化学试题
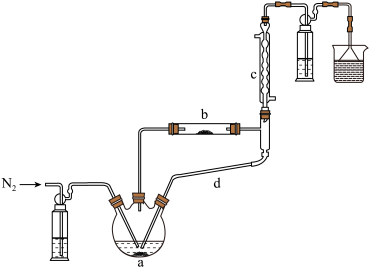
6 . 实验室利用 和亚硫酰氯(
和亚硫酰氯( )制备无水
)制备无水 的装置如图所示(加热及夹持装置略)。已知
的装置如图所示(加热及夹持装置略)。已知 的沸点为
的沸点为 ,遇水极易反应生成两种酸性气体。实验步骤为实验开始时先通
,遇水极易反应生成两种酸性气体。实验步骤为实验开始时先通 ,一段时间后,先加热装置a,再加热装置b,反应一段时间。
,一段时间后,先加热装置a,再加热装置b,反应一段时间。
(1)基态Fe原子的价层电子轨道表示式为______ ,其最外层电子所占据原子轨道的电子云轮廓图为______ 形。
(2)实验开始先通 的目的是
的目的是______ 。c中的冷凝水应从______ (填“上”或“下”)口通入。
(3)写出 遇水反应生成两种酸性气体的化学方程式:
遇水反应生成两种酸性气体的化学方程式:______ 。
(4) 纯度的测定。
纯度的测定。
称取5.0g样品,用足量稀硫酸溶解后,配制成250mL溶液,用滴定管量取25.00mL于锥形瓶中、用 酸性
酸性 标准溶液滴定,平行滴定3次,测得消耗酸性
标准溶液滴定,平行滴定3次,测得消耗酸性 标准溶液的平均体积为12.50mL(滴定过程中
标准溶液的平均体积为12.50mL(滴定过程中 转化为
转化为 ,
, 不反应)。
不反应)。
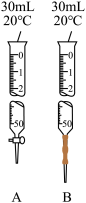
①量取酸性 标准溶液应选用
标准溶液应选用______ (填“A”或“B”)。
②写出酸性 溶液与
溶液与 反应的离子方程式:
反应的离子方程式:______ 。
③ 样品的纯度为
样品的纯度为______ %。
 和亚硫酰氯(
和亚硫酰氯( )制备无水
)制备无水 的装置如图所示(加热及夹持装置略)。已知
的装置如图所示(加热及夹持装置略)。已知 的沸点为
的沸点为 ,遇水极易反应生成两种酸性气体。实验步骤为实验开始时先通
,遇水极易反应生成两种酸性气体。实验步骤为实验开始时先通 ,一段时间后,先加热装置a,再加热装置b,反应一段时间。
,一段时间后,先加热装置a,再加热装置b,反应一段时间。
(1)基态Fe原子的价层电子轨道表示式为
(2)实验开始先通
 的目的是
的目的是(3)写出
 遇水反应生成两种酸性气体的化学方程式:
遇水反应生成两种酸性气体的化学方程式:(4)
 纯度的测定。
纯度的测定。称取5.0g样品,用足量稀硫酸溶解后,配制成250mL溶液,用滴定管量取25.00mL于锥形瓶中、用
 酸性
酸性 标准溶液滴定,平行滴定3次,测得消耗酸性
标准溶液滴定,平行滴定3次,测得消耗酸性 标准溶液的平均体积为12.50mL(滴定过程中
标准溶液的平均体积为12.50mL(滴定过程中 转化为
转化为 ,
, 不反应)。
不反应)。
①量取酸性
 标准溶液应选用
标准溶液应选用②写出酸性
 溶液与
溶液与 反应的离子方程式:
反应的离子方程式:③
 样品的纯度为
样品的纯度为
您最近一年使用:0次
7 . 下列关于物质的分离、提纯实验中的一些操作或做法,正确的是
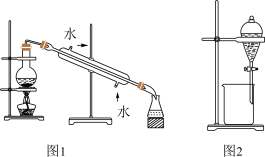

| A.用95.6%的工业酒精制取无水乙醇、可采用的方法是加生石灰,再蒸馏 |
| B.在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后要冷却到常温再过滤 |
| C.用图1所示装置可以分离二氯甲烷、三氯甲烷和四氯化碳的混合物 |
| D.用图2所示装置可以用乙醇提取溴水中的溴 |
您最近一年使用:0次
名校
8 . 用下列实验装置进行相应实验,能达到实验目的的是
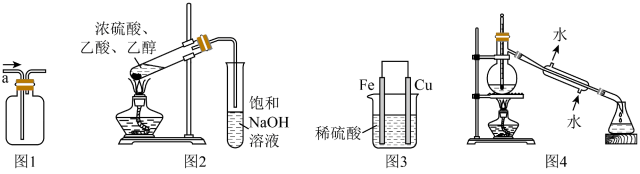

| A.用图1所示装置从a口进气收集纯净的CH4 |
| B.用图2所示装置制取并收集乙酸乙酯 |
| C.用图3所示装置比较Fe、Cu的金属活动性 |
| D.用图4所示装置进行石油的蒸馏实验 |
您最近一年使用:0次
2023-05-05更新
|
1052次组卷
|
8卷引用:山西省朔州市怀仁市2022-2023学年高一下学期7月期末化学试题
9 . 某化学小组采用类似制乙酸乙酯的装置,用环己醇制备环己烯:
已知: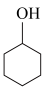
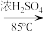
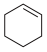 +H2O
+H2O
(1)制备粗品:采用如图所示装置,用环己醇制备环己烯。
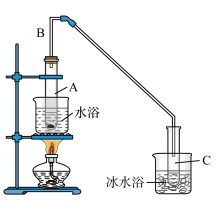
将10.0g环己醇加入试管A中,再加入1mL浓硫酸,摇匀放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是______ 。
②试管C置子冰水浴中的目的是_____ 。
(2)制备精品:
①环己烯粗品中含有环己醇和少量有机酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在______ 层(填“上”或“下),分液后用______ 洗涤(填字母)。
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液
②再将环己烯按如图装置蒸馏。冷凝水从_____ 口进入(填“g”或“f”)。
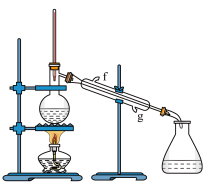
③收集产品时,应收集______ ℃的馏分,若最终收集到环己烯5.74g,则产率为______ 。
已知:

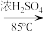
 +H2O
+H2O| 密度(g•cm-3) | 熔点(℃) | 沸点(℃) | 溶解性 | 摩尔质量(g/mol) | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 | 100 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 | 82 |

将10.0g环己醇加入试管A中,再加入1mL浓硫酸,摇匀放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是
②试管C置子冰水浴中的目的是
(2)制备精品:
①环己烯粗品中含有环己醇和少量有机酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液
②再将环己烯按如图装置蒸馏。冷凝水从

③收集产品时,应收集
您最近一年使用:0次
2023-04-28更新
|
290次组卷
|
2卷引用:山西省大同市阳高县第四中学校2022-2023学年高二下学期7月期末考试化学试题
10 . 某小组设计如图实验探究铁与水蒸气的反应。
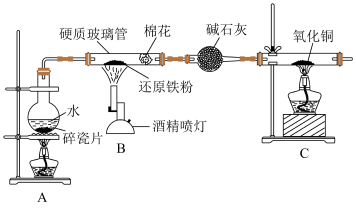
(1)写出铁和水蒸气反应的化学方程式,并用双线桥表示电子转移的方向和数目:______ 。
(2)圆底烧瓶中碎瓷片的作用是防止暴沸,若加热一段时间后发现忘记加碎瓷片,需要补加碎瓷片的操作是______ 。
(3)检验反应后的固体是否存在Fe3O4,引起小组成员争论:
①甲同学认为可以使用化学方法,先用足量硫酸溶解,再分别检验Fe2+和Fe3+。
先检测Fe2+是否存在:请从下列试剂中选择一种:NaOH溶液、新制氯水、KSCN溶液、酸性KMnO4溶液,写出发生反应的离子方程式:______ ;然后再检测Fe3+是否存在。多数同学认为该方法检验是否存在Fe3O4不合理,请写出一条理由:______ 。
②乙同学认为可以利用Fe3O4的物理性质进行快速检验。用铁片接触样品后再移开,若观察到_____ 现象,证明了反应后的固体中含有Fe3O4。

(1)写出铁和水蒸气反应的化学方程式,并用双线桥表示电子转移的方向和数目:
(2)圆底烧瓶中碎瓷片的作用是防止暴沸,若加热一段时间后发现忘记加碎瓷片,需要补加碎瓷片的操作是
(3)检验反应后的固体是否存在Fe3O4,引起小组成员争论:
①甲同学认为可以使用化学方法,先用足量硫酸溶解,再分别检验Fe2+和Fe3+。
先检测Fe2+是否存在:请从下列试剂中选择一种:NaOH溶液、新制氯水、KSCN溶液、酸性KMnO4溶液,写出发生反应的离子方程式:
②乙同学认为可以利用Fe3O4的物理性质进行快速检验。用铁片接触样品后再移开,若观察到
您最近一年使用:0次



