解题方法
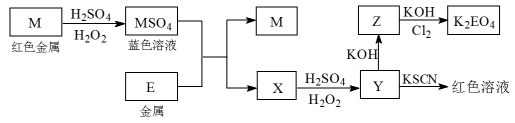
1 . 随着电子工业的发展,电子垃圾的数量逐渐增多,对环境构成了极大的污染。某化学兴趣探究小组将一批废弃的线路板简单处理后,得到红色金属M和金属E并进行如下框图所示转化,获得高效净水剂K2EO4.(答题时,化学式及化学方程式中的M、E均用所对应的元素符号表示):_______ 。
(2)检验X中阳离子的方法和现象是_______ 。
(3)如果各步转化无损失,M转化为MSO4消耗的H2O2与X转化为Y消耗的H2O2的用量之比为:_______ 。
(4)由MSO4的蓝色溶液经一系列操作可以获得蓝色晶体,这些操作中用到的实验仪器除了酒精灯、蒸发皿、铁架台外,还需要用到的玻璃仪器有_____ 、______ 、______ (填写仪器名称)。
(5)某同学利用H2还原MO来测定M的相对原子质量,下图是测定装置示意图,A中试剂是盐酸。_______ (填写偏高、偏低、正常),装置D的作用_______ ;
②连接好装置并检验装置的气密性,检验气密性的方法是:________ 。然后应首先“加热反应管E”还是“从A瓶中逐滴加入液体”?_______ 在这两步之间还应进行的操作是_______ 。
(2)检验X中阳离子的方法和现象是
(3)如果各步转化无损失,M转化为MSO4消耗的H2O2与X转化为Y消耗的H2O2的用量之比为:
(4)由MSO4的蓝色溶液经一系列操作可以获得蓝色晶体,这些操作中用到的实验仪器除了酒精灯、蒸发皿、铁架台外,还需要用到的玻璃仪器有
(5)某同学利用H2还原MO来测定M的相对原子质量,下图是测定装置示意图,A中试剂是盐酸。
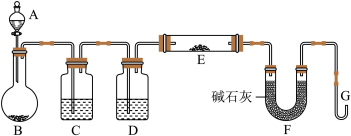
②连接好装置并检验装置的气密性,检验气密性的方法是:
您最近一年使用:0次
名校
解题方法
2 . 利用硫铁矿(主要成分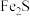 )生产硫酸和绿矾(
)生产硫酸和绿矾( )的工业流程示意图如下:
)的工业流程示意图如下:_______ 。
(2)吸收塔中,发生的主要反应的化学方程式是_______ 。
(3)反应釜中,烧渣经过反应转化为溶液I和固体。溶液I中所含溶质的化学式_______ 。
(4)操作a的主要步骤是:加热浓缩、_______ 、过滤、洗涤、_______ 。
(5)流程中,固体X可以选择硫铁矿(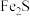 )或
)或_______ ;当固体X为硫铁矿(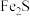 )时,将溶液I与固体发生反应的离子方程式补充完整:
)时,将溶液I与固体发生反应的离子方程式补充完整:_______ 。

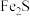 )生产硫酸和绿矾(
)生产硫酸和绿矾( )的工业流程示意图如下:
)的工业流程示意图如下: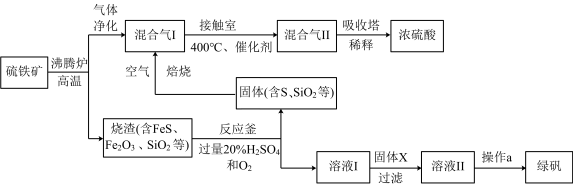
(2)吸收塔中,发生的主要反应的化学方程式是
(3)反应釜中,烧渣经过反应转化为溶液I和固体。溶液I中所含溶质的化学式
(4)操作a的主要步骤是:加热浓缩、
(5)流程中,固体X可以选择硫铁矿(
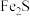 )或
)或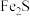 )时,将溶液I与固体发生反应的离子方程式补充完整:
)时,将溶液I与固体发生反应的离子方程式补充完整:
您最近一年使用:0次
2024-04-29更新
|
139次组卷
|
2卷引用:安徽省安庆二中2023-2024学年高一下学期期中考试化学试题
名校
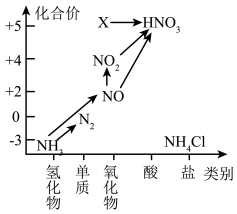
3 . 依据下图中氨元素及其化合物的转化关系,回答问题: 与
与 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为_______ 。
(2)若要收集一瓶氨气,请将下列装置补充完整,在虚框内画出连接图_________ 。 的是
的是_______ 。
A.浓硫酸 B.碱石灰 C.
(4)工业上以 、空气、水为原料生产硝酸分为三步:
、空气、水为原料生产硝酸分为三步:
① 化学方程式为
化学方程式为_______ 。
② 实验现象是
实验现象是_______ 。
③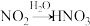 氧化剂与还原剂物质的量之比为
氧化剂与还原剂物质的量之比为_______ 。
 与
与 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为(2)若要收集一瓶氨气,请将下列装置补充完整,在虚框内画出连接图

 的是
的是A.浓硫酸 B.碱石灰 C.

(4)工业上以
 、空气、水为原料生产硝酸分为三步:
、空气、水为原料生产硝酸分为三步:①
 化学方程式为
化学方程式为②
 实验现象是
实验现象是③
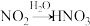 氧化剂与还原剂物质的量之比为
氧化剂与还原剂物质的量之比为
您最近一年使用:0次
4 . 现有NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去杂质,从而得到纯净的NaNO3晶体,相应的实验流程如图所示。
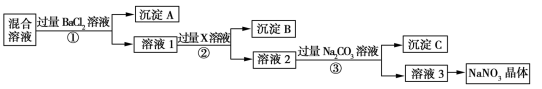
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X_____ 沉淀B_____ 。
(2)上述实验流程中①②③步均要进行的实验操作是_____ (填操作名称)。
(3)上述实验流程中加入过量Na2CO3溶液后发生反应的离子方程式:_____ 、_____ 。
(4)(本小题两空均填化学式)按此实验方案得到的溶液3中肯定含有_____ 杂质。为了解决这个问题,可以向溶液3中加入适量的_____ 。
(5)在①步操作中如何证明加的BaCl2溶液已过量?_____ 。

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X
(2)上述实验流程中①②③步均要进行的实验操作是
(3)上述实验流程中加入过量Na2CO3溶液后发生反应的离子方程式:
(4)(本小题两空均填化学式)按此实验方案得到的溶液3中肯定含有
(5)在①步操作中如何证明加的BaCl2溶液已过量?
您最近一年使用:0次
名校
5 . 海水中富含大量的氯化钠,将海水蒸发可得粗盐,精制后得到精制食盐,不仅可食用,还可用作工业生产的原料。
Ⅰ.粗盐中除了含有泥沙之外,还含有少量Ca2+、Mg2+、SO 等杂质离子,某同学设计如图实验方案提纯粗盐,请根据下图回答下列问题。
等杂质离子,某同学设计如图实验方案提纯粗盐,请根据下图回答下列问题。
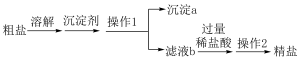
(1)粗盐溶解后加入沉淀剂:①过量的Na2CO3溶液 ②过量的BaCl2溶液 ③过量的NaOH溶液,加入沉淀剂的顺序正确的是___________ (填序号)。
a.①②③ b.②①③ c.③①②
(2)操作1中用到的玻璃仪器有玻璃棒、烧杯、___________ (填仪器名称);玻璃棒作用是___________ 。沉淀a的主要成分是碳酸钙、碳酸钡、___________ (填化学式)。
(3)操作2后可得到精盐,操作名称是___________ 。
(4)检验滤液b中是否含有SO 的实验操作:
的实验操作:___________ 。
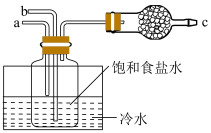
Ⅱ. 我国近代化学工业的奠基人侯德榜先生,设计出“侯氏制碱法”,提高了食盐的转化率,缩短了生产流程,减少了对环境的污染。工艺流程如图所示:

(5)氨化和碳酸化过程在如图所示装置中进行,对应的总化学方程式为___________ ,a导管应通入的气体是___________ (填化学式),仪器c中盛放的药品___________ 。
Ⅰ.粗盐中除了含有泥沙之外,还含有少量Ca2+、Mg2+、SO
 等杂质离子,某同学设计如图实验方案提纯粗盐,请根据下图回答下列问题。
等杂质离子,某同学设计如图实验方案提纯粗盐,请根据下图回答下列问题。
(1)粗盐溶解后加入沉淀剂:①过量的Na2CO3溶液 ②过量的BaCl2溶液 ③过量的NaOH溶液,加入沉淀剂的顺序正确的是
a.①②③ b.②①③ c.③①②
(2)操作1中用到的玻璃仪器有玻璃棒、烧杯、
(3)操作2后可得到精盐,操作名称是
(4)检验滤液b中是否含有SO
 的实验操作:
的实验操作:Ⅱ. 我国近代化学工业的奠基人侯德榜先生,设计出“侯氏制碱法”,提高了食盐的转化率,缩短了生产流程,减少了对环境的污染。工艺流程如图所示:

(5)氨化和碳酸化过程在如图所示装置中进行,对应的总化学方程式为

您最近一年使用:0次
名校
解题方法
6 . 某同学为了测定某生铁(仅含C、 )中铁的质量分数,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究.
)中铁的质量分数,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究.

回答下列问题:
(1)仪器a的名称为________ ,仪器e的名称为________ ;
(2)B装置的作用为________ ,D装置的作用为________ ;
(3)点燃酒精灯,A装置中发生的反应化学方程式为_______________ 、_________________
(4)待 生铁完全溶解后,停止加热,拆下装置E并称重.若装置E增重
生铁完全溶解后,停止加热,拆下装置E并称重.若装置E增重 ,则生铁中铁的质量分数为
,则生铁中铁的质量分数为________ (用含m、b的表达式表示);
(5)利用该装置测得实验结果不够准确,改良的方法为____________________ 。
 )中铁的质量分数,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究.
)中铁的质量分数,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究.
回答下列问题:
(1)仪器a的名称为
(2)B装置的作用为
(3)点燃酒精灯,A装置中发生的反应化学方程式为
(4)待
 生铁完全溶解后,停止加热,拆下装置E并称重.若装置E增重
生铁完全溶解后,停止加热,拆下装置E并称重.若装置E增重 ,则生铁中铁的质量分数为
,则生铁中铁的质量分数为(5)利用该装置测得实验结果不够准确,改良的方法为
您最近一年使用:0次
7 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
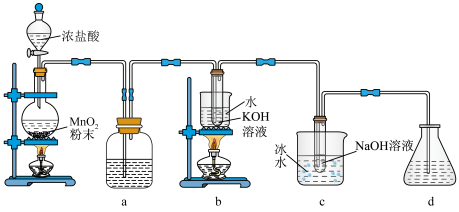
回答下列问题:
(1)盛放 粉末的仪器名称是
粉末的仪器名称是_______ ,a中的试剂为_______ 。
(2)b中采用的加热方式是_______ ,c中化学反应的离子方程式是_______ 。
(3)d的作用是_______ ,可选用试剂_______ (填标号)。
A.NaCl B.NaOH C. D.
D.
 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
回答下列问题:
(1)盛放
 粉末的仪器名称是
粉末的仪器名称是(2)b中采用的加热方式是
(3)d的作用是
A.NaCl B.NaOH C.
 D.
D.
您最近一年使用:0次
名校
8 . 回答下列问题:
(1)实验室常见的几种气体发生装置如图A、B、C所示:

①实验室可以用B或C装置制取氨气,如果用C装置,通常使用的药品是_______ ;检查C装置气密性的方法是_______ 。
②若用A装置与D装置相连制取并收集X气体,则X可能是下列气体中的_______ (填序号)。
a. b.NO c.
b.NO c. d.
d.
(2)取化学式为MZ的粉末状化合物进行如下实验。将MZ和足量碳粉充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成,同时b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却,此时管中的熔融物凝固成银白色金属。根据以上叙述回答:

①元素Z是_______ ;(填名称)
②停止加热是否需要先断开a和b的连接处?为什么?_______ 。
③本实验的尾气是否需处理?_______ (填“需要”或“不需要”),请说明理由_______ 。
(1)实验室常见的几种气体发生装置如图A、B、C所示:

①实验室可以用B或C装置制取氨气,如果用C装置,通常使用的药品是
②若用A装置与D装置相连制取并收集X气体,则X可能是下列气体中的
a.
 b.NO c.
b.NO c. d.
d.
(2)取化学式为MZ的粉末状化合物进行如下实验。将MZ和足量碳粉充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成,同时b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却,此时管中的熔融物凝固成银白色金属。根据以上叙述回答:

①元素Z是
②停止加热是否需要先断开a和b的连接处?为什么?
③本实验的尾气是否需处理?
您最近一年使用:0次
名校
9 . 某兴趣小组用铬铁矿(FeCr2O4,含SiO2等杂质)为主要原料制备重铬酸钾(K2Cr2O7)晶体,流程如图:

已知:FeCr2O4中Cr元素为+3价;SiO2与Na2CO3高温生成可溶于水的Na2SiO3;CrO 酸性条件下能转化为Cr2O
酸性条件下能转化为Cr2O 。
。
回答下列问题:
(1)“焙烧”时,除生成Na2CrO4和Fe2O3外,还生成一种无色无味的气体,该反应的化学方程式为_______ 。焙烧时气体与矿料逆流而行,目的是________ 。
(2)实验室进行“操作1”用到的玻璃仪器有:烧杯、_______ 。
(3)“晶体X”的化学式为______ 。
(4)交警查酒驾所用检测仪器的工作原理为:2Cr2O (橙红色)+3C2H5OH+16H+=3CH3COOH+11H2O+4Cr3+。该反应中,还原剂为
(橙红色)+3C2H5OH+16H+=3CH3COOH+11H2O+4Cr3+。该反应中,还原剂为_______ ;反应消耗1molK2Cr2O7时,转移电子的数目为________ 。
(5)“结晶”时,为得到杂质较少的K2Cr2O7粗产品,请结合如图从下列选项中选出合理的操作并排序_______ (填字母)。

a.40℃蒸发溶剂 b.90℃蒸发溶剂 c.过滤 d.冷却至室温 e.蒸发至溶液出现晶膜,停止加热
(6)该小组用m1kg铬铁矿(FeCr2O450%)制备K2Cr2O7,最终得到m2kg,产率为______ 。

已知:FeCr2O4中Cr元素为+3价;SiO2与Na2CO3高温生成可溶于水的Na2SiO3;CrO
 酸性条件下能转化为Cr2O
酸性条件下能转化为Cr2O 。
。回答下列问题:
(1)“焙烧”时,除生成Na2CrO4和Fe2O3外,还生成一种无色无味的气体,该反应的化学方程式为
(2)实验室进行“操作1”用到的玻璃仪器有:烧杯、
(3)“晶体X”的化学式为
(4)交警查酒驾所用检测仪器的工作原理为:2Cr2O
 (橙红色)+3C2H5OH+16H+=3CH3COOH+11H2O+4Cr3+。该反应中,还原剂为
(橙红色)+3C2H5OH+16H+=3CH3COOH+11H2O+4Cr3+。该反应中,还原剂为(5)“结晶”时,为得到杂质较少的K2Cr2O7粗产品,请结合如图从下列选项中选出合理的操作并排序

a.40℃蒸发溶剂 b.90℃蒸发溶剂 c.过滤 d.冷却至室温 e.蒸发至溶液出现晶膜,停止加热
(6)该小组用m1kg铬铁矿(FeCr2O450%)制备K2Cr2O7,最终得到m2kg,产率为
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
10 . 硫脲[CS(NH2)2](M=76)在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备Ca(HS)2,再与CaCN2溶液反应合成CS(NH2)2,实验装置如图所示(夹持及加热装置略)。

已知:CS(NH2)2易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
回答下列问题:
(1)盛装盐酸的仪器名称是_______ 。
(2)实验前先检查装置气密性,操作:
①在E中加水至浸没导管末端,……;
②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;
③一段时间后,E处导管末端形成一段水柱,且高度不变。
将操作①补充完整_______ 。
(3)检查装置气密性后加入药品,打开K2,装置B中盛装的试剂为_______ 。
(4)关闭K2,撤走搅拌器,打开K3,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度不高于80℃的原因是_______ ,D处合成硫脲的化学方程式为_______ 。

已知:CS(NH2)2易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
回答下列问题:
(1)盛装盐酸的仪器名称是
(2)实验前先检查装置气密性,操作:
①在E中加水至浸没导管末端,……;
②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;
③一段时间后,E处导管末端形成一段水柱,且高度不变。
将操作①补充完整
(3)检查装置气密性后加入药品,打开K2,装置B中盛装的试剂为
(4)关闭K2,撤走搅拌器,打开K3,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度不高于80℃的原因是
您最近一年使用:0次



