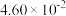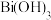名校
解题方法
1 . 工业上以富钒炉渣(主要含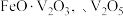 和少量的
和少量的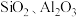 等)为原料制备
等)为原料制备 的工艺流程如下:
的工艺流程如下: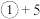 价钒元素在溶液中的存在形式与溶液
价钒元素在溶液中的存在形式与溶液 的关系:
的关系:
②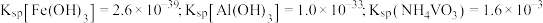
回答下列问题:
(1)“高温氧化”前将富钒炉渣研磨粉碎的目的是___________________ ;“高温氧化”过程中发生主要反应的化学方程式为_____________________ ;
(2)“酸浸”后滤渣1的主要成分为___________ ;
(3)“调 ”时,需将
”时,需将 完全除尽(浓度
完全除尽(浓度 时,可认为已除尽)且保证钒元素以
时,可认为已除尽)且保证钒元素以 存在,则需调节
存在,则需调节 的范围为
的范围为________ ;
(4)若“沉钒”前溶液中 ,忽略溶液体积变化,为使钒元素的沉降率达到
,忽略溶液体积变化,为使钒元素的沉降率达到 ,至少应调节
,至少应调节 为
为__________  。过滤、洗涤、干燥得到
。过滤、洗涤、干燥得到 沉淀,检验
沉淀,检验 沉淀是否洗净的操作是
沉淀是否洗净的操作是_____________________ ;
(5)“焙烧”时,写出 受热分解的化学方程式
受热分解的化学方程式______________ 。
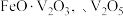 和少量的
和少量的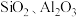 等)为原料制备
等)为原料制备 的工艺流程如下:
的工艺流程如下: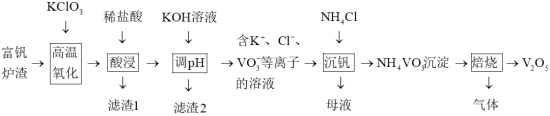
 价钒元素在溶液中的存在形式与溶液
价钒元素在溶液中的存在形式与溶液 的关系:
的关系:溶液 |
|
|
|
|
|
|
钒元素存在形式 |
|
| 多矾酸根 |
| 多矾酸根 |
|
备注 | 多矾酸盐在水中溶解度较小, | |||||
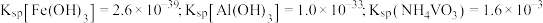
回答下列问题:
(1)“高温氧化”前将富钒炉渣研磨粉碎的目的是
(2)“酸浸”后滤渣1的主要成分为
(3)“调
 ”时,需将
”时,需将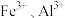 完全除尽(浓度
完全除尽(浓度 时,可认为已除尽)且保证钒元素以
时,可认为已除尽)且保证钒元素以 存在,则需调节
存在,则需调节 的范围为
的范围为(4)若“沉钒”前溶液中
 ,忽略溶液体积变化,为使钒元素的沉降率达到
,忽略溶液体积变化,为使钒元素的沉降率达到 ,至少应调节
,至少应调节 为
为 。过滤、洗涤、干燥得到
。过滤、洗涤、干燥得到 沉淀,检验
沉淀,检验 沉淀是否洗净的操作是
沉淀是否洗净的操作是(5)“焙烧”时,写出
 受热分解的化学方程式
受热分解的化学方程式
您最近一年使用:0次
2024-03-24更新
|
171次组卷
|
2卷引用:重庆市西南大学附属中学校2023-2024学年高二下学期3月联合考试化学试题
名校
2 . 通过海水晾晒可以得到粗盐,粗盐除含有 外,还含有
外,还含有 以及泥沙等杂质.以下是某兴趣小组制备精盐的实验方案,各步操作流程如图.下列说法正确的是
以及泥沙等杂质.以下是某兴趣小组制备精盐的实验方案,各步操作流程如图.下列说法正确的是
 外,还含有
外,还含有 以及泥沙等杂质.以下是某兴趣小组制备精盐的实验方案,各步操作流程如图.下列说法正确的是
以及泥沙等杂质.以下是某兴趣小组制备精盐的实验方案,各步操作流程如图.下列说法正确的是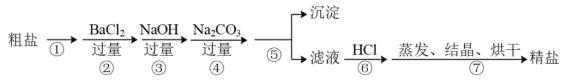
| A.实验过程中②、④步骤互换,对实验结果不影响 |
| B.实验过程中①、⑤步骤的操作分别是溶解、过滤 |
| C.实验过程中步骤⑦中的蒸发所用到的仪器是酒精灯、玻璃棒、烧杯、表面皿、铁架台(带铁圈) |
D.实验过程中步骤④的目的是仅除去溶液中的 |
您最近一年使用:0次
2024-03-21更新
|
310次组卷
|
6卷引用:重庆市实验中学2021-2022学年高一下学期第一次月考化学试题
名校
3 . 钛被誉为“21世纪的金属”,以颜钛铁矿(主要含 ,钛元素化合价为
,钛元素化合价为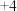 价;含
价;含 等杂质)为原料制备颜料铵铁蓝
等杂质)为原料制备颜料铵铁蓝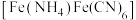 和
和 的流程示意图如下:
的流程示意图如下: 难溶于水,遇酸后钛元素以
难溶于水,遇酸后钛元素以 的形式存在于溶液中,
的形式存在于溶液中, 易水解为
易水解为 [
[ 也可写作
也可写作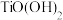 ].
].
(1)基态 原子的价电子轨道表示式为
原子的价电子轨道表示式为____________________ ,提高“酸浸”浸出率的方法有____________________ (任写一种即可)
(2)固体物质A是__________ (填化学式)。试剂B为____________________ (填下列选项标号)
A. B.
B. C.
C. D.
D.
(3)由 制备
制备 时需在稀有气体氛围中进行,其目的是
时需在稀有气体氛围中进行,其目的是______________________________ 。
(4)粗 转化为
转化为 时,高温下充分反应后,混合气体中生成物各组分的分压如下表:
时,高温下充分反应后,混合气体中生成物各组分的分压如下表:
该温度下, 与
与 反应的总化学方程式为
反应的总化学方程式为__________________ 。
(5)在“沉铁”步骤产生的白色沉淀为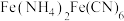 ,
,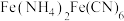 转化为铵铁蓝的离子方程式为
转化为铵铁蓝的离子方程式为___________________ 。
(6)已知:常温下,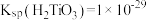 ,若要让
,若要让 水解完全(离子浓度小于
水解完全(离子浓度小于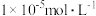 ),应控制
),应控制 不低
不低__________ 。
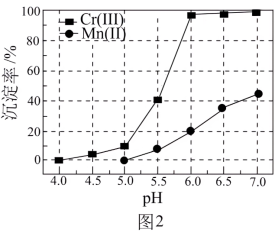
(7)在物质制备的过程中需不断调整外界因素,以得到最佳制备条件,某小组为探究流程中“还原”工序的最佳条件进行了相关实验,在其他条件不变的情况下,体系中 (Ⅲ)含量随
(Ⅲ)含量随 变化如图,试分析在
变化如图,试分析在 介于
介于 之间时,
之间时, (Ⅲ)含量基本保持不变的原因:
(Ⅲ)含量基本保持不变的原因:______________________________ 。
 ,钛元素化合价为
,钛元素化合价为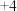 价;含
价;含 等杂质)为原料制备颜料铵铁蓝
等杂质)为原料制备颜料铵铁蓝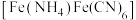 和
和 的流程示意图如下:
的流程示意图如下: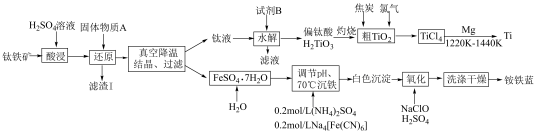
 难溶于水,遇酸后钛元素以
难溶于水,遇酸后钛元素以 的形式存在于溶液中,
的形式存在于溶液中, 易水解为
易水解为 [
[ 也可写作
也可写作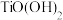 ].
].(1)基态
 原子的价电子轨道表示式为
原子的价电子轨道表示式为(2)固体物质A是
A.
 B.
B. C.
C. D.
D.
(3)由
 制备
制备 时需在稀有气体氛围中进行,其目的是
时需在稀有气体氛围中进行,其目的是(4)粗
 转化为
转化为 时,高温下充分反应后,混合气体中生成物各组分的分压如下表:
时,高温下充分反应后,混合气体中生成物各组分的分压如下表:物质 |
|
|
|
分压 |
|
|
|
 与
与 反应的总化学方程式为
反应的总化学方程式为(5)在“沉铁”步骤产生的白色沉淀为
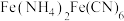 ,
,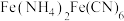 转化为铵铁蓝的离子方程式为
转化为铵铁蓝的离子方程式为(6)已知:常温下,
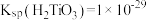 ,若要让
,若要让 水解完全(离子浓度小于
水解完全(离子浓度小于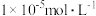 ),应控制
),应控制 不低
不低(7)在物质制备的过程中需不断调整外界因素,以得到最佳制备条件,某小组为探究流程中“还原”工序的最佳条件进行了相关实验,在其他条件不变的情况下,体系中
 (Ⅲ)含量随
(Ⅲ)含量随 变化如图,试分析在
变化如图,试分析在 介于
介于 之间时,
之间时, (Ⅲ)含量基本保持不变的原因:
(Ⅲ)含量基本保持不变的原因: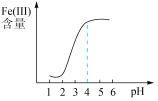
您最近一年使用:0次
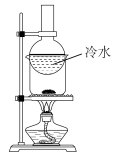
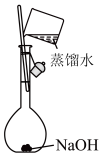
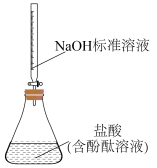
4 . 下列实验装置及试剂的使用正确,且能达到实验目的的是
|
|
|
|
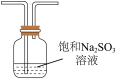
| A.除去SO2中的HCl | B.制备氢氧化铁胶体 | C.分离乙酸乙酯和乙醇 | D.分离NH4Cl(s)和NaCl(s) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 近日,科学家利用光催化剂 实现高选择性制备氢气。某小组以辉铋矿(主要成分是
实现高选择性制备氢气。某小组以辉铋矿(主要成分是 ,含少量
,含少量 和
和 等杂质)为原料制备钒酸铋(
等杂质)为原料制备钒酸铋( )的流程如下:
)的流程如下: 和
和 。
。
②几种氢氧化物沉淀的 如表所示。
如表所示。
回答下列问题:
(1)基态 原子的价层电子排布式为
原子的价层电子排布式为_________ 。浸渣1中,除了 外还有一种单质为
外还有一种单质为_________ 。
(2)调 的最低值为
的最低值为_________ 。滤液3可以循环用于“_________ ”工序(填名称)。
(3)“氯化”的化学方程式为___________________________ 。
(4)已知辉铋矿中所含 元素的质量分数为
元素的质量分数为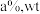 这种矿石经上述转化最终制得
这种矿石经上述转化最终制得 ,则铋的收率为
,则铋的收率为_________ ( )。
)。
(5) 的立方晶胞结构如图所示。已知晶体密度为
的立方晶胞结构如图所示。已知晶体密度为 ,设
,设 为阿伏加德罗常数的值,则该晶体中与
为阿伏加德罗常数的值,则该晶体中与 距离最近且相等的
距离最近且相等的 有
有_________ 个,相邻2个 的核间距为
的核间距为_________  。
。
 实现高选择性制备氢气。某小组以辉铋矿(主要成分是
实现高选择性制备氢气。某小组以辉铋矿(主要成分是 ,含少量
,含少量 和
和 等杂质)为原料制备钒酸铋(
等杂质)为原料制备钒酸铋( )的流程如下:
)的流程如下:
 和
和 。
。②几种氢氧化物沉淀的
 如表所示。
如表所示。氢氧化物 |
|
|
|
开始沉淀 | 7.5 | 1.6 | 4.0 |
沉淀完全 | 9.7 | 3.1 | 5.5 |
(1)基态
 原子的价层电子排布式为
原子的价层电子排布式为 外还有一种单质为
外还有一种单质为(2)调
 的最低值为
的最低值为(3)“氯化”的化学方程式为
(4)已知辉铋矿中所含
 元素的质量分数为
元素的质量分数为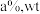 这种矿石经上述转化最终制得
这种矿石经上述转化最终制得 ,则铋的收率为
,则铋的收率为 )。
)。(5)
 的立方晶胞结构如图所示。已知晶体密度为
的立方晶胞结构如图所示。已知晶体密度为 ,设
,设 为阿伏加德罗常数的值,则该晶体中与
为阿伏加德罗常数的值,则该晶体中与 距离最近且相等的
距离最近且相等的 有
有 的核间距为
的核间距为 。
。
您最近一年使用:0次
2024-03-17更新
|
187次组卷
|
2卷引用:重庆市七校联盟2023-2024学年高三下学期第一次月考化学试题
6 . 下列实验操作(如图)正确且能达到实验目的的是


A.图甲模拟侯氏制碱法获得 |
| B.图乙用NaOH溶液滴定未知浓度的醋酸溶液 |
| C.图丙装置用于干燥高锰酸钾 |
D.图丁用于除去 中的 中的 |
您最近一年使用:0次
名校
解题方法
7 . 用下列仪器或装置进行相应实验,能达到实验目的的是
|
|
| 配置一定物质的量浓度的NaOH溶液 | 可用于灼烧碎海带 |
| A | B |
|
|
| 可用于除去SO2中的HCl | 可用于测定盐酸浓度 |
| C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 从钒铬锰矿渣(主要成分为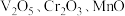 )中提铬的一种工艺流程如下:
)中提铬的一种工艺流程如下: 较大时,二价锰
较大时,二价锰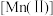 在空气中易被氧化。回答下列问题:
在空气中易被氧化。回答下列问题:
(1) 元素在周期表中的位置是
元素在周期表中的位置是___________ 。
(2)常温下,各种形态五价钒粒子总浓度的对数 与
与 关系如图1,已知钒铬锰矿渣硫酸浸液中
关系如图1,已知钒铬锰矿渣硫酸浸液中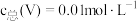 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为___________ (填化学式)。_____ (填标号);
在该条件下滤液B中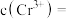
______  [
[ 近似为
近似为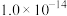 ,
, 的
的 近似为
近似为 ]。
]。
(4)“转化”过程中生成 的离子方程式为
的离子方程式为_________ 。
(5)“提纯”过程中 的作用为
的作用为________ 。
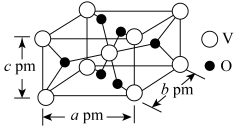
(6)一种含钒的氧化物晶胞结构如图所示,已知NA表示阿伏加德罗常数的值,则该晶体密度为_______ g•cm-3 (列出计算式即可)。
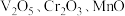 )中提铬的一种工艺流程如下:
)中提铬的一种工艺流程如下: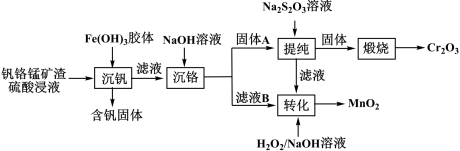
 较大时,二价锰
较大时,二价锰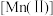 在空气中易被氧化。回答下列问题:
在空气中易被氧化。回答下列问题:(1)
 元素在周期表中的位置是
元素在周期表中的位置是(2)常温下,各种形态五价钒粒子总浓度的对数
 与
与 关系如图1,已知钒铬锰矿渣硫酸浸液中
关系如图1,已知钒铬锰矿渣硫酸浸液中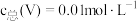 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为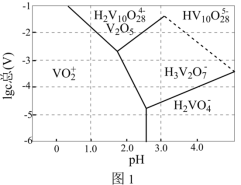
在该条件下滤液B中
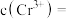
 [
[ 近似为
近似为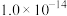 ,
, 的
的 近似为
近似为 ]。
]。(4)“转化”过程中生成
 的离子方程式为
的离子方程式为(5)“提纯”过程中
 的作用为
的作用为(6)一种含钒的氧化物晶胞结构如图所示,已知NA表示阿伏加德罗常数的值,则该晶体密度为
您最近一年使用:0次
名校
解题方法
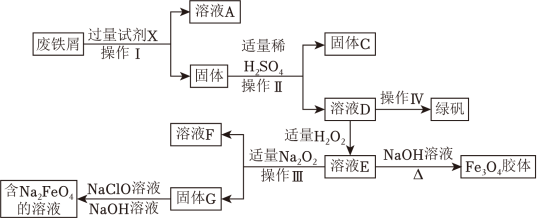
9 . 绿矾(FeSO4⋅7H2O)是治疗缺铁性贫血药品的重要成分,某化学兴趣小组利用工厂的废铁屑(主要成分为Fe,此外还含有少量Cu、Al,Al2O3和Fe2O3)制备磁性Fe3O4胶体粒子、绿矾和净水剂Na2FeO4的实验流程如图:
(1)试剂X化学式为_____ 。写出加入过量试剂X时所有发生反应的离子方程式_____ 。
(2)铁元素位于元素周期表_____ 。
(3)固体C化学名称为_____ 。溶液D中加入KSCN溶液,无血红色产生,原因是_____ (用化学方程式表示)。
(4)为得到绿矾晶体需要将溶液D进行_____ (“蒸发结晶”或“降温结晶”)。
(5)D中加入适量H2O2生成E的离子方程式_____ 。若D中含amolFe2+,则理论上加入_____ molH2O2可使溶液E中铁元素恰好转化为Fe3O4胶体。
(6)由固体G生成Na2FeO4的离子方程式为_____ 。
(1)试剂X化学式为
(2)铁元素位于元素周期表
(3)固体C化学名称为
(4)为得到绿矾晶体需要将溶液D进行
(5)D中加入适量H2O2生成E的离子方程式
(6)由固体G生成Na2FeO4的离子方程式为
您最近一年使用:0次
2024-02-01更新
|
63次组卷
|
2卷引用:重庆市乌江新高考协作体2023-2024学年高一下学期4月月考化学试题
名校
10 . 通过海水晾晒可以得到粗盐,粗盐除还有 NaCl 外,还含有 MgCl2 、 CaCl2 、 Na2 SO4以及泥沙等杂质。以下是某兴趣小组制备精盐的实验方案,各步操作流程如图。下列说法不正确的是
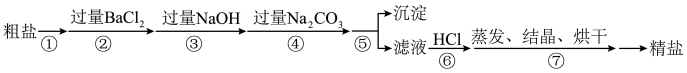
A.步骤②的目的是除去溶液中的 SO |
| B.步骤③的目的是除去溶液中的 Mg2+ |
| C.步骤④仅除去溶液中的 Ca2+ |
| D.步骤⑥可同时除去溶液中过量的 NaOH 和 Na2CO3 |
您最近一年使用:0次
2024-02-01更新
|
69次组卷
|
3卷引用:重庆市黔江中学校2021-2022年度高一上11月考试化学试题
重庆市黔江中学校2021-2022年度高一上11月考试化学试题江西省景德镇市乐平市第三中学2023-2024学年高一下学期3月月考化学试题(已下线)实验05 用化学沉淀法去除粗盐中的杂质离子-【同步实验课】2023-2024学年高一化学教材实验大盘点(人教版2019必修第二册)

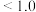
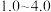
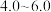

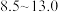
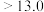


 在
在 时开始溶解
时开始溶解