名校
1 . 某废旧金属材料中主要含 、
、 、
、 、
、 、
、 、
、 、
、 和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物:
和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物: 。
。
回答下列问题:
(1)“焙烧”的目的是将金属单质转化为氧化物,并除去_______ 。
(2) 的电子式为
的电子式为_________ ,“碱浸”时发生反应的离子方程式为______ 。
(3)“操作Ⅰ”的名称为________ 。
(4)试剂a为_______ (填化学式),加入试剂a后可能发生的反应为______ (写出其中1个反应的离子方程式即可)。
(5)滤液Ⅱ中可能含有因氧气的作用而产生的少量______ (填离子符号),检验该离子的操作是______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物:
和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物: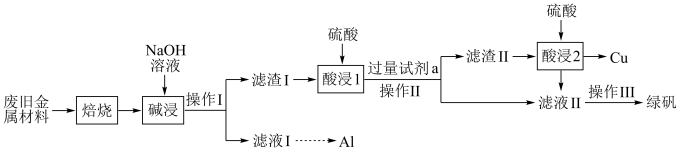
 。
。回答下列问题:
(1)“焙烧”的目的是将金属单质转化为氧化物,并除去
(2)
 的电子式为
的电子式为(3)“操作Ⅰ”的名称为
(4)试剂a为
(5)滤液Ⅱ中可能含有因氧气的作用而产生的少量
您最近一年使用:0次
名校
2 . 海水是巨大的资源宝库,工业上从海水中获取某些重要化工原料的流程如下图示。 、
、 和
和 等。回答下列问题:
等。回答下列问题:
(1)请列举除蒸馏法外海水淡化的一种方法:____________________ 。
(2)试剂1最好选用__________ (填编号)。
a. b.
b. c.
c. d.NaOH
d.NaOH
(3)提取溴单质时,往苦卤中通入氯气和酸,其酸化的目的是____________________ 。
(4)将吹出后的含 的空气按一定速率通入吸收塔,用
的空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。
和水进行吸收,吸收后的空气进行循环利用。
①流程中可用热空气吹出溴的原因为_____________________ 。
②“吸收塔”内发生反应的离子方程式:_____________________ 。
③流程中不是将酸和氯气氧化后的苦卤直接蒸馏,而是经过“空气吹出”、“二氧化硫吸收”、“氢气氧化”再蒸馏得到液溴,目的是_____________________ 。
(5)检验吸收塔里的溶液是否含 的方法是
的方法是_______________________ 。
(6)海带灰中富含以 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如图所示:
的途径如图所示:__________ (填一种仪器名称)中加热灼烧。
②向酸化的滤液中加入过氧化氢溶液,可将 氧化为
氧化为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:__________________ 。

 、
、 和
和 等。回答下列问题:
等。回答下列问题:(1)请列举除蒸馏法外海水淡化的一种方法:
(2)试剂1最好选用
a.
 b.
b. c.
c. d.NaOH
d.NaOH(3)提取溴单质时,往苦卤中通入氯气和酸,其酸化的目的是
(4)将吹出后的含
 的空气按一定速率通入吸收塔,用
的空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。
和水进行吸收,吸收后的空气进行循环利用。①流程中可用热空气吹出溴的原因为
②“吸收塔”内发生反应的离子方程式:
③流程中不是将酸和氯气氧化后的苦卤直接蒸馏,而是经过“空气吹出”、“二氧化硫吸收”、“氢气氧化”再蒸馏得到液溴,目的是
(5)检验吸收塔里的溶液是否含
 的方法是
的方法是(6)海带灰中富含以
 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如图所示:
的途径如图所示: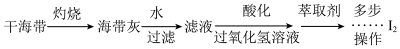
②向酸化的滤液中加入过氧化氢溶液,可将
 氧化为
氧化为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:
您最近一年使用:0次
名校
3 . 某硫酸厂用硫铁矿焙烧后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制备绿矾粗产品(FeSO4·7H2O),设计了如下流程:
回答下列问题:
(1)“试剂a”的化学式为___________ ,“操作”的名称是___________ 。
(2)“酸浸”后溶液呈黄色,“还原”操作是向溶液逐步加入试剂b,溶液变为浅绿色,写出溶液变为浅绿色的离子方程式___________ 。
(3)在“调pH至5-6”步骤中,写出生成Al(OH)3的离子方程式___________ 。
(4)鉴别“滤液1”中金属阳离子的实验方案:取少量滤液1进行___________ (填实验名称),若观察到火焰呈黄色,则证明含有Na+;另外取少量滤液1于试管中,依次滴入___________ 和氯水,若实验现象依次为溶液先无红色,后变红色,则证明含有Fe2+,写出该过程中属于氧化还原反应的离子方程式___________ 。

回答下列问题:
(1)“试剂a”的化学式为
(2)“酸浸”后溶液呈黄色,“还原”操作是向溶液逐步加入试剂b,溶液变为浅绿色,写出溶液变为浅绿色的离子方程式
(3)在“调pH至5-6”步骤中,写出生成Al(OH)3的离子方程式
(4)鉴别“滤液1”中金属阳离子的实验方案:取少量滤液1进行
您最近一年使用:0次
解题方法
4 . I.通过海水晾晒可得粗盐,粗盐中除NaCl外,还含有 、
、 、
、 以及泥沙等杂质,为了将粗盐有效提纯,实验的各步操作流程如下:
以及泥沙等杂质,为了将粗盐有效提纯,实验的各步操作流程如下:______ (填名称)。
(2)操作溶解、过滤、蒸发都用到一种玻璃仪器是______ (填仪器名称),
(3)试剂a由三种试剂构成,除杂步骤中试剂可行的添加顺序有______(填标号)。
Ⅱ.某研究小组利用提纯后精盐配制饱和NaCl溶液,模拟侯德榜制碱法制取碱,流程如图:
(4)装置Ⅰ中,往饱和食盐水中优先通入的气体为______ (填化学式),装置Ⅰ中反应的化学方程式为____________ ;
(5)该流程中可循环利用的物质是______ (填化学式)
 、
、 、
、 以及泥沙等杂质,为了将粗盐有效提纯,实验的各步操作流程如下:
以及泥沙等杂质,为了将粗盐有效提纯,实验的各步操作流程如下:
(2)操作溶解、过滤、蒸发都用到一种玻璃仪器是
(3)试剂a由三种试剂构成,除杂步骤中试剂可行的添加顺序有______(填标号)。
A.① ② ② ③NaOH ③NaOH | B.① ②NaOH③ ②NaOH③ |
C.①NaOH② ③ ③ | D.① ② ② ③NaOH ③NaOH |
Ⅱ.某研究小组利用提纯后精盐配制饱和NaCl溶液,模拟侯德榜制碱法制取碱,流程如图:

| 物质 | NaCl |  |  |  |
| 溶解度 | 36.0 | 21.7 | 9.6 | 37.2 |
(4)装置Ⅰ中,往饱和食盐水中优先通入的气体为
(5)该流程中可循环利用的物质是
您最近一年使用:0次
名校
5 . 食盐不但是人类生活中不可缺少的物质,而且是重要的化工原料。用化学沉淀法去除粗盐中的杂质离子 所需的实验操作如下:
所需的实验操作如下:
①加入稍过量的 溶液 ②加入稍过量的
溶液 ②加入稍过量的 溶液 ③加入稍过量的
溶液 ③加入稍过量的 溶液
溶液
④加入稀盐酸直至无气泡产生 ⑤过滤
下列有关说法正确的是
 所需的实验操作如下:
所需的实验操作如下:①加入稍过量的
 溶液 ②加入稍过量的
溶液 ②加入稍过量的 溶液 ③加入稍过量的
溶液 ③加入稍过量的 溶液
溶液④加入稀盐酸直至无气泡产生 ⑤过滤
下列有关说法正确的是
| A.操作顺序可为③①④②⑤ |
B.加入 溶液后,只发生一个离子反应 溶液后,只发生一个离子反应 |
C.将除杂后的滤液倒入表面血中加热得到 固体 固体 |
D.除杂过程中,稀盐酸的作用是除去多余的 并调节滤液至呈中性或微酸性 并调节滤液至呈中性或微酸性 |
您最近一年使用:0次
名校
6 . 氮化硅( )是一种高温结构陶瓷材料,它硬度大、熔点高、化学性质稳定。合成氮化硅的一种工艺流程如图所示。下列说法正确的是
)是一种高温结构陶瓷材料,它硬度大、熔点高、化学性质稳定。合成氮化硅的一种工艺流程如图所示。下列说法正确的是 在潮湿的空气中易水解,产生白雾
在潮湿的空气中易水解,产生白雾
 )是一种高温结构陶瓷材料,它硬度大、熔点高、化学性质稳定。合成氮化硅的一种工艺流程如图所示。下列说法正确的是
)是一种高温结构陶瓷材料,它硬度大、熔点高、化学性质稳定。合成氮化硅的一种工艺流程如图所示。下列说法正确的是
 在潮湿的空气中易水解,产生白雾
在潮湿的空气中易水解,产生白雾A.该流程中可循环使用的物质是 |
| B.第③步反应是氧化还原反应 |
C. 因为硬度大不属于无机非金属材料 因为硬度大不属于无机非金属材料 |
D.第③步反应可用氨水代替 |
您最近一年使用:0次
名校
7 . 以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O3既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
以下是一种废钒催化剂回收工艺路线:
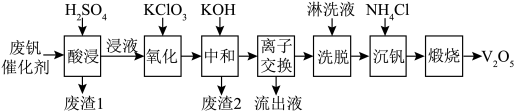
回答下列问题:
(1)“酸浸”时V2O5转化为 , 反应的离子方程式为
, 反应的离子方程式为___________ ,同时V2O4转化为 。“废渣1”的主要成分是
。“废渣1”的主要成分是______ 。
(2)“氧化”中使 变为
变为 , 则“氧化”环节中还原剂与氧化剂的物质的量之比为
, 则“氧化”环节中还原剂与氧化剂的物质的量之比为______ 。
(3)“中和”后的溶液中,钒主要以 形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
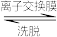
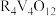 +
+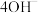 (以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈
(以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈_____ 性(填“敢”或“碱”)。
(4)检验“流出液”中含量最多的阳离子,其实验操作称为___ 。
(5)“煅烧”中发生反应的化学方程式 ,写出“沉钒”过程的离子方程式
,写出“沉钒”过程的离子方程式_________ 。
| 物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
| 质量分数/% | 2.20~2.90 | 2.8~3.32 | 22~28 | 60~65 | 1~2 | <1 |

回答下列问题:
(1)“酸浸”时V2O5转化为
 , 反应的离子方程式为
, 反应的离子方程式为 。“废渣1”的主要成分是
。“废渣1”的主要成分是(2)“氧化”中使
 变为
变为 , 则“氧化”环节中还原剂与氧化剂的物质的量之比为
, 则“氧化”环节中还原剂与氧化剂的物质的量之比为(3)“中和”后的溶液中,钒主要以
 形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
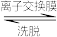
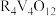 +
+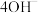 (以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈
(以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈(4)检验“流出液”中含量最多的阳离子,其实验操作称为
(5)“煅烧”中发生反应的化学方程式
 ,写出“沉钒”过程的离子方程式
,写出“沉钒”过程的离子方程式
您最近一年使用:0次
解题方法
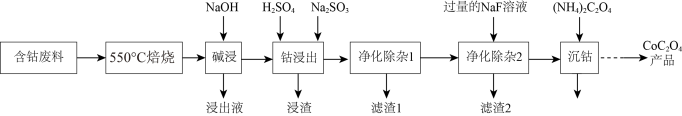
8 . 草酸钴是制作氧化钴和金属钴的原料,一种利用含钴废料(主要成分为Co2O3,含少量Fe2O3、ZnO、Al2O3、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如下:
②ZnO与Al2O3化学性质相似,既能溶于强酸又能溶于强碱
(1)“550℃焙烧”的目的是_______ 。
(2)“浸出液”的主要成分是_______ 。
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为_______ 。
(4)“净化除杂1”过程中,先在40 ~ 50℃加入H2O2,控制温度不能太高的原因是_______ ,H2O2的作用是_______ (用离子方程式表示)。
(5)在空气中焙烧CoC2O4生成Co3O4和一种气体,请写出该反应的化学方程式:_______ 。
②ZnO与Al2O3化学性质相似,既能溶于强酸又能溶于强碱
(1)“550℃焙烧”的目的是
(2)“浸出液”的主要成分是
(3)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为
(4)“净化除杂1”过程中,先在40 ~ 50℃加入H2O2,控制温度不能太高的原因是
(5)在空气中焙烧CoC2O4生成Co3O4和一种气体,请写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
9 . 碱式氧化镍是镍电池的正极活性材料。利用镍渣(主要含NiO,及少量 、CuO、CaO、
、CuO、CaO、 等杂质)制备碱式氧化镍的流程如下:
等杂质)制备碱式氧化镍的流程如下:
(2)浸渣的主要成分是_______ 。
(3)“沉铜”过程中生成单质S的离子方程式为______ 。
(4)“氧化”中的目的是将 氧化为
氧化为 ,试剂R可选用
,试剂R可选用_____ (填标号)。写出“氧化”时反应的离子方程式:_____ 。
A.氯水 B. 酸性溶液 C.
酸性溶液 C.
(5)碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,电池的总反应为
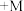 ,其工作时的正极电极反应式为
,其工作时的正极电极反应式为_______ 。
(6)若用2.0t废料(含NiO75%)制得NiOOH 0.92 t,则NiOOH的产率为_____ %。
 、CuO、CaO、
、CuO、CaO、 等杂质)制备碱式氧化镍的流程如下:
等杂质)制备碱式氧化镍的流程如下: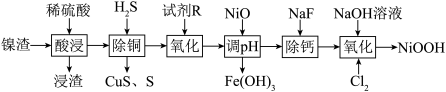
| A.研磨废料 | B.加入大量水 | C.搅拌 | D.适当升高温度 |
(2)浸渣的主要成分是
(3)“沉铜”过程中生成单质S的离子方程式为
(4)“氧化”中的目的是将
 氧化为
氧化为 ,试剂R可选用
,试剂R可选用A.氯水 B.
 酸性溶液 C.
酸性溶液 C.
(5)碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,电池的总反应为

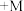 ,其工作时的正极电极反应式为
,其工作时的正极电极反应式为(6)若用2.0t废料(含NiO75%)制得NiOOH 0.92 t,则NiOOH的产率为
您最近一年使用:0次
2024-05-03更新
|
278次组卷
|
2卷引用:广东省深圳市翠园中学、龙城高级中学2023-2024学年高一下学期第一次月考化学试题
名校
解题方法
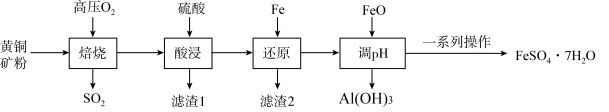
10 . 绿矾(FeSO4⋅7H2O))是一种重要的药物,也是一种工业原料。一种以黄铜矿(主要成分是CuFeS2,含SiO2、Al2O3等杂质)为原料制备绿矾的流程如图:
(1)“焙烧”时,需将黄铜矿粉碎,其目的是_______ ;高温“焙烧”过程中生成了三种氧化物,其化学方程式是_______ 。
(2)滤渣1的主要成分为_______ (填化学式,下同);滤渣2的主要成分为_______ 。
(3)“一系列操作”为:_______ 、_______ 、过滤、洗涤、干燥。
(4)硫代硫酸钠(Na2S2O3)俗称“海波”或“大苏打”,也是一种重要的含硫盐。在酸性条件下不稳定,易生成一种固体和一种气体,其离子方程式为_______ 。
(5)绿矾在空气中容易被部分氧化。现取被部分氧化的绿矾晶体溶于稀盐酸后,加入足量的BaCl2溶液,过滤得沉淀9.32g;再通入112mL(标准状况)氯气恰好将其中的Fe2+完全氧化。推测所取晶体中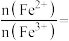
_______ 。
(1)“焙烧”时,需将黄铜矿粉碎,其目的是
(2)滤渣1的主要成分为
(3)“一系列操作”为:
(4)硫代硫酸钠(Na2S2O3)俗称“海波”或“大苏打”,也是一种重要的含硫盐。在酸性条件下不稳定,易生成一种固体和一种气体,其离子方程式为
(5)绿矾在空气中容易被部分氧化。现取被部分氧化的绿矾晶体溶于稀盐酸后,加入足量的BaCl2溶液,过滤得沉淀9.32g;再通入112mL(标准状况)氯气恰好将其中的Fe2+完全氧化。推测所取晶体中
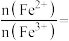
您最近一年使用:0次



