名校
解题方法
1 . 铈(Ce)的氧化物在半导体材料、高级颜料及汽车尾气的净化器方面有广泛应用。以氟碳铈矿(含 、
、 、
、 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图:
(1) 中氟元素对应的氟原子激发态的电子排布式有
中氟元素对应的氟原子激发态的电子排布式有_______ (填序号)。
a. b.
b. c.
c. d.
d.
(2) 中非金属元素的第一电离能从小到大依次为
中非金属元素的第一电离能从小到大依次为_______ 。
(3)“氧化焙烧”后, 元素转化为
元素转化为 和
和 。写出“氧化焙烧”时
。写出“氧化焙烧”时 发生的化学反应方程式:
发生的化学反应方程式:_______ 。
(4)实验室进行操作①所需的玻璃仪器有_______ 。
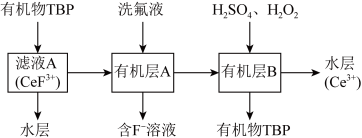
(5)“系列操作”包含下图几个过程: 不能溶于有机物
不能溶于有机物 ;
; 能溶于有机物
能溶于有机物 ,且存在反应
,且存在反应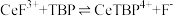 。“滤液A”中加入有机物
。“滤液A”中加入有机物 后的分离方法是
后的分离方法是_______ 。
(6)已知25℃时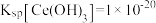 ,“调pH”时,要使
,“调pH”时,要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制
为沉淀完全),应控制 大于
大于_______ 。
(7) 立方晶胞结构如图所示。
立方晶胞结构如图所示。_______ 。
 、
、 、
、 等)为原料制备
等)为原料制备 的工艺流程如图:
的工艺流程如图: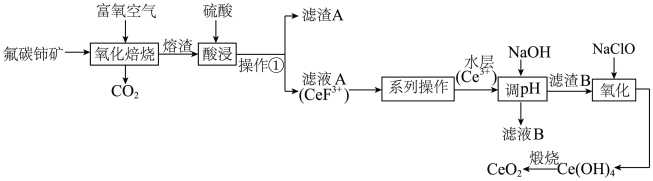
(1)
 中氟元素对应的氟原子激发态的电子排布式有
中氟元素对应的氟原子激发态的电子排布式有a.
 b.
b. c.
c. d.
d.
(2)
 中非金属元素的第一电离能从小到大依次为
中非金属元素的第一电离能从小到大依次为(3)“氧化焙烧”后,
 元素转化为
元素转化为 和
和 。写出“氧化焙烧”时
。写出“氧化焙烧”时 发生的化学反应方程式:
发生的化学反应方程式:(4)实验室进行操作①所需的玻璃仪器有
(5)“系列操作”包含下图几个过程:
 不能溶于有机物
不能溶于有机物 ;
; 能溶于有机物
能溶于有机物 ,且存在反应
,且存在反应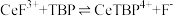 。“滤液A”中加入有机物
。“滤液A”中加入有机物 后的分离方法是
后的分离方法是(6)已知25℃时
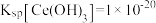 ,“调pH”时,要使
,“调pH”时,要使 沉淀完全(通常认为溶液中离子浓度小于
沉淀完全(通常认为溶液中离子浓度小于 为沉淀完全),应控制
为沉淀完全),应控制 大于
大于(7)
 立方晶胞结构如图所示。
立方晶胞结构如图所示。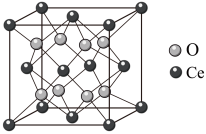
您最近一年使用:0次
名校
2 . 某废旧金属材料中主要含 、
、 、
、 、
、 、
、 、
、 、
、 和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物:
和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物: 。
。
回答下列问题:
(1)“焙烧”的目的是将金属单质转化为氧化物,并除去_______ 。
(2) 的电子式为
的电子式为_________ ,“碱浸”时发生反应的离子方程式为______ 。
(3)“操作Ⅰ”的名称为________ 。
(4)试剂a为_______ (填化学式),加入试剂a后可能发生的反应为______ (写出其中1个反应的离子方程式即可)。
(5)滤液Ⅱ中可能含有因氧气的作用而产生的少量______ (填离子符号),检验该离子的操作是______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物:
和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物: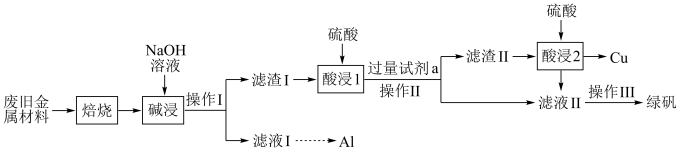
 。
。回答下列问题:
(1)“焙烧”的目的是将金属单质转化为氧化物,并除去
(2)
 的电子式为
的电子式为(3)“操作Ⅰ”的名称为
(4)试剂a为
(5)滤液Ⅱ中可能含有因氧气的作用而产生的少量
您最近一年使用:0次
3 . 碘、水吸收 ,具体流程如图所示。(已知:HI易挥发)
,具体流程如图所示。(已知:HI易挥发) 和HI的方法为___________。
和HI的方法为___________。
(2)该流程总反应的化学方程式为___________ 。
(3)请评价该流程的优点___________ (任写两点)。
 ,具体流程如图所示。(已知:HI易挥发)
,具体流程如图所示。(已知:HI易挥发)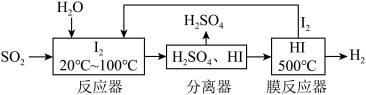
 和HI的方法为___________。
和HI的方法为___________。| A.过滤 | B.蒸馏 | C.结晶 | D.渗析 |
(2)该流程总反应的化学方程式为
(3)请评价该流程的优点
您最近一年使用:0次
名校
4 . 食盐不但是人类生活中不可缺少的物质,而且是重要的化工原料。用化学沉淀法去除粗盐中的杂质离子 所需的实验操作如下:
所需的实验操作如下:
①加入稍过量的 溶液 ②加入稍过量的
溶液 ②加入稍过量的 溶液 ③加入稍过量的
溶液 ③加入稍过量的 溶液
溶液
④加入稀盐酸直至无气泡产生 ⑤过滤
下列有关说法正确的是
 所需的实验操作如下:
所需的实验操作如下:①加入稍过量的
 溶液 ②加入稍过量的
溶液 ②加入稍过量的 溶液 ③加入稍过量的
溶液 ③加入稍过量的 溶液
溶液④加入稀盐酸直至无气泡产生 ⑤过滤
下列有关说法正确的是
| A.操作顺序可为③①④②⑤ |
B.加入 溶液后,只发生一个离子反应 溶液后,只发生一个离子反应 |
C.将除杂后的滤液倒入表面血中加热得到 固体 固体 |
D.除杂过程中,稀盐酸的作用是除去多余的 并调节滤液至呈中性或微酸性 并调节滤液至呈中性或微酸性 |
您最近一年使用:0次
名校
5 . 海水提溴的主要工业生产流程如下图所示。 ,利用了
,利用了 的
的___________ ,吸收塔中吸收 ,利用了
,利用了 的
的___________ 。
2.吸收塔中反应的离子方程式是___________ 。

 ,利用了
,利用了 的
的 ,利用了
,利用了 的
的2.吸收塔中反应的离子方程式是
您最近一年使用:0次
解题方法
6 . 某工厂的固体废渣中主要含 和
和 ,还含有少量
,还含有少量 和
和 。
。
利用该固体废渣制取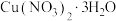 的部分工艺流程如图所示:
的部分工艺流程如图所示: 属于碱性氧化物;
属于碱性氧化物; 在酸性溶液中不稳定,会转变为
在酸性溶液中不稳定,会转变为 和
和 。
。
② 是酸性氧化物,难于水和酸。
是酸性氧化物,难于水和酸。
(1)若中和时加入的 恰好完全反应,则过滤后所得废渣的成分为
恰好完全反应,则过滤后所得废渣的成分为________ 。
(2) 与稀硝酸反应时,硝酸体现出的性质:
与稀硝酸反应时,硝酸体现出的性质:________ 。
(3)酸溶时,反应温度不宜超过 ,其主要原因是
,其主要原因是________ 。
(4)写出 与稀硝酸反应的离子方程式:
与稀硝酸反应的离子方程式:________ 。
(5)已知: 的溶解度曲线如图所示
的溶解度曲线如图所示 )为原料,制取
)为原料,制取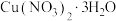 晶体的操作流程如下:
晶体的操作流程如下:
先向工业废水中加入 溶液,充分反应后,过滤,洗涤;向滤渣中加入稀硝酸至固体完全溶解,
溶液,充分反应后,过滤,洗涤;向滤渣中加入稀硝酸至固体完全溶解,_________ ,_________ ,(填操作名称)过滤,洗涤,干燥,即制得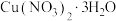 晶体。
晶体。
 和
和 ,还含有少量
,还含有少量 和
和 。
。利用该固体废渣制取
 的部分工艺流程如图所示:
的部分工艺流程如图所示:
 属于碱性氧化物;
属于碱性氧化物; 在酸性溶液中不稳定,会转变为
在酸性溶液中不稳定,会转变为 和
和 。
。②
 是酸性氧化物,难于水和酸。
是酸性氧化物,难于水和酸。(1)若中和时加入的
 恰好完全反应,则过滤后所得废渣的成分为
恰好完全反应,则过滤后所得废渣的成分为(2)
 与稀硝酸反应时,硝酸体现出的性质:
与稀硝酸反应时,硝酸体现出的性质:(3)酸溶时,反应温度不宜超过
 ,其主要原因是
,其主要原因是(4)写出
 与稀硝酸反应的离子方程式:
与稀硝酸反应的离子方程式:(5)已知:
 的溶解度曲线如图所示
的溶解度曲线如图所示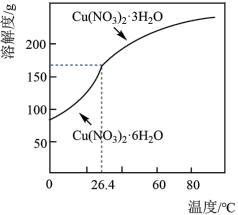
 )为原料,制取
)为原料,制取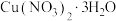 晶体的操作流程如下:
晶体的操作流程如下:先向工业废水中加入
 溶液,充分反应后,过滤,洗涤;向滤渣中加入稀硝酸至固体完全溶解,
溶液,充分反应后,过滤,洗涤;向滤渣中加入稀硝酸至固体完全溶解,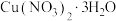 晶体。
晶体。
您最近一年使用:0次
解题方法
7 . 下列分离或除杂所用试剂和方法正确的是
| A.分离溶于水中的碘(乙醇、萃取) |
| B.除去苯中混有苯酚(NaOH溶液、过滤) |
| C.制无水乙醇(CaO、蒸馏) |
| D.除去乙酸乙酯中的乙酸(NaOH、蒸馏) |
您最近一年使用:0次
名校
解题方法
8 . 工业上用硫化镍矿(主要成分为NiS,含有ZnS、CuS、FeS等杂质)制备 的工艺流程如下:
的工艺流程如下:___________ ,煅烧NiS生成NiO和 的化学方程式为
的化学方程式为___________ 。
(2)向滤液Ⅰ中加入FeS是为了生成难溶于水的硫化物沉淀而除去 、
、 等杂质,则除去
等杂质,则除去 的离子方程式为
的离子方程式为 ,该反应的化学平衡常数为
,该反应的化学平衡常数为___________ (已知 ,
, ,
, )。
)。
(3)向滤液Ⅱ中加入H2O2的目的是___________ 。
(4)滤液Ⅲ中溶质的主要成分是 ,加
,加 过滤后得到
过滤后得到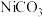 沉淀,再加适量稀硫酸溶解又生成
沉淀,再加适量稀硫酸溶解又生成 ,这两步操作的目的是
,这两步操作的目的是___________ 。
(5)用惰性电极电解 溶液时,在
溶液时,在___________ 极得到单质镍,另一电极的电极反应式为:___________ 。
 的工艺流程如下:
的工艺流程如下: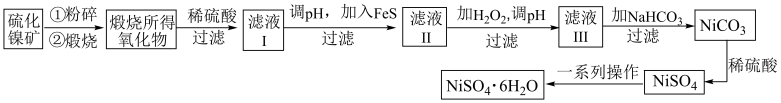
 的化学方程式为
的化学方程式为(2)向滤液Ⅰ中加入FeS是为了生成难溶于水的硫化物沉淀而除去
 、
、 等杂质,则除去
等杂质,则除去 的离子方程式为
的离子方程式为 ,该反应的化学平衡常数为
,该反应的化学平衡常数为 ,
, ,
, )。
)。(3)向滤液Ⅱ中加入H2O2的目的是
(4)滤液Ⅲ中溶质的主要成分是
 ,加
,加 过滤后得到
过滤后得到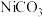 沉淀,再加适量稀硫酸溶解又生成
沉淀,再加适量稀硫酸溶解又生成 ,这两步操作的目的是
,这两步操作的目的是(5)用惰性电极电解
 溶液时,在
溶液时,在
您最近一年使用:0次
名校
解题方法
9 . 电路板广泛用于计算机、手机等电子产品中。某兴趣小组拟制作带有“化学”标志的电路板并对废液进行回收利用。
I.制作电路板
小组同学取一小块覆铜板,用油性笔在铜板上写出“化学”标志,然后浸入 溶液中,一段时间后,取出覆铜板并用水洗净,获得带有图案的印刷电路板和废液(如图所示)。
溶液中,一段时间后,取出覆铜板并用水洗净,获得带有图案的印刷电路板和废液(如图所示)。_______ 。
(2)取少量废液于试管中,_______ (填操作和现象),则废液中含有 。
。
Ⅱ.回收废液
该组同学查阅资料:一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如图。
(3)废液100mL,加入铁粉,其固体质量的变化如图所示,假设溶液体积不变,_______ 。
②原混合溶液中 的物质的量
的物质的量_______ 。
③ 点溶液中
点溶液中 的物质的量浓度
的物质的量浓度_______ 。
(4)操作方法 中是过滤的是
中是过滤的是_______ (填序号)。
(5)若取2mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,_______ (补全实验现象),此过程涉及氧化还原反应的化学方程式是:_______ 。
(6)试剂⑥是 时,发生反应的化学方程式是
时,发生反应的化学方程式是_______ 。
I.制作电路板
小组同学取一小块覆铜板,用油性笔在铜板上写出“化学”标志,然后浸入
 溶液中,一段时间后,取出覆铜板并用水洗净,获得带有图案的印刷电路板和废液(如图所示)。
溶液中,一段时间后,取出覆铜板并用水洗净,获得带有图案的印刷电路板和废液(如图所示)。
(2)取少量废液于试管中,
 。
。Ⅱ.回收废液
该组同学查阅资料:一种从腐蚀废液回收金属铜并获得氯化铁晶体的工艺流程如图。
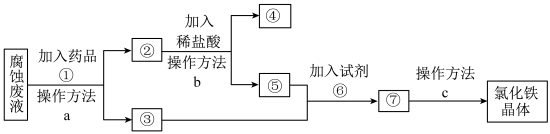
(3)废液100mL,加入铁粉,其固体质量的变化如图所示,假设溶液体积不变,
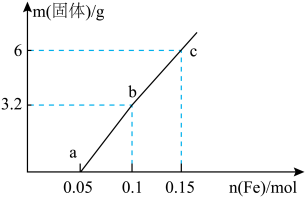
②原混合溶液中
 的物质的量
的物质的量③
 点溶液中
点溶液中 的物质的量浓度
的物质的量浓度(4)操作方法
 中是过滤的是
中是过滤的是(5)若取2mL溶液⑤加入试管中,然后滴加氢氧化钠溶液,产生白色沉淀,
(6)试剂⑥是
 时,发生反应的化学方程式是
时,发生反应的化学方程式是
您最近一年使用:0次
解题方法
10 . 已知溶液A中含有Cu2+、Fe2+、Fe3+三种金属离子,且三种离子沉淀时的pH如下表:
___________ 。
(2)加入CuO作用是调节pH,则pH的范围:___________ 。还可以用哪些物质来代替CuO?___________ 。
(3)操作1为___________ ,操作2为___________ 。
| 金属离子 | Fe3+ | Fe2+ | Cu2+ | |
| pH | 开始沉淀 | 1.9 | 7.0 | 4.7 |
| 完全沉淀 | 3.2 | 9.0 | 6.7 | |
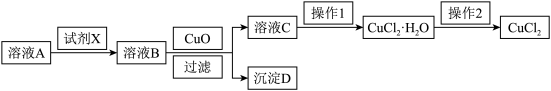
(2)加入CuO作用是调节pH,则pH的范围:
(3)操作1为
您最近一年使用:0次



