名校
解题方法
1 . 以硫酸工业的尾气 为主要原料制备
为主要原料制备 、
、 的工艺流程如下图所示:
的工艺流程如下图所示:
(1)反应I的化学方程式为___________ 。
(2)生产过程中,得到滤液时,操作所需的玻璃仪器除烧杯外还有___________ 。
(3)反应Ⅲ所得的 可在反应
可在反应___________ (填“I”、“Ⅱ”或“Ⅳ”)中重复使用,检验滤液中阳离子的操作方法是___________ 。
(4)已知 能将氮氧化物转化为无污染性气体(
能将氮氧化物转化为无污染性气体( 不参与氧化还原反应),则
不参与氧化还原反应),则 与
与 反应(忽略
反应(忽略 和
和 的转化),还原剂和氧化剂的比值为
的转化),还原剂和氧化剂的比值为___________ ,当生成的无污染性气体体积为 (标准状况),该反应转移的电子数目为
(标准状况),该反应转移的电子数目为___________ 。
(5)将一定比例的氢气和二氧化硫以一定流速通过装有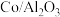 催化剂的反应容器,反应原理如图所示。结合图中信息写出第2步反应的化学方程式:
催化剂的反应容器,反应原理如图所示。结合图中信息写出第2步反应的化学方程式:___________ 。
 为主要原料制备
为主要原料制备 、
、 的工艺流程如下图所示:
的工艺流程如下图所示: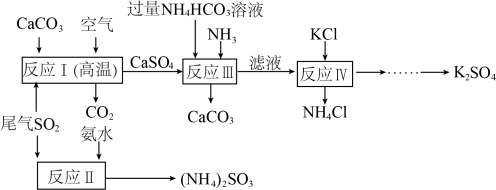
(1)反应I的化学方程式为
(2)生产过程中,得到滤液时,操作所需的玻璃仪器除烧杯外还有
(3)反应Ⅲ所得的
 可在反应
可在反应(4)已知
 能将氮氧化物转化为无污染性气体(
能将氮氧化物转化为无污染性气体( 不参与氧化还原反应),则
不参与氧化还原反应),则 与
与 反应(忽略
反应(忽略 和
和 的转化),还原剂和氧化剂的比值为
的转化),还原剂和氧化剂的比值为 (标准状况),该反应转移的电子数目为
(标准状况),该反应转移的电子数目为(5)将一定比例的氢气和二氧化硫以一定流速通过装有
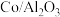 催化剂的反应容器,反应原理如图所示。结合图中信息写出第2步反应的化学方程式:
催化剂的反应容器,反应原理如图所示。结合图中信息写出第2步反应的化学方程式: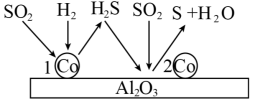
您最近一年使用:0次
名校
解题方法
2 . 海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素。_____________ 操作。
(2)过程c的化学反应方程式_____________________________________ 。
(3)过程b用于海水提溴.主要工业生产流程如下图所示。 ,利用了
,利用了 的氧化性,写出对应反应的离子方程式
的氧化性,写出对应反应的离子方程式_____________________________________________ 。
②吹出塔中通入热空气吹出 ,利用了
,利用了 的
的_____________ (填字母)。
A.氧化性 B.还原性 C.挥发性,沸点比水低 D.易溶于水
(4)实验室可以利用蒸馏的方法进行海水淡化,可选用如图装置完成。
①仪器B的名称是_____________ 。
②该装置中有一处明显的错误是________________________ 。
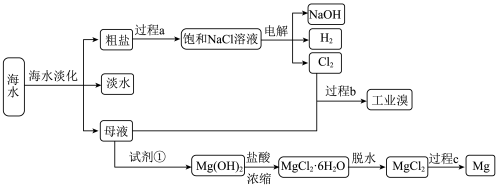
(2)过程c的化学反应方程式
(3)过程b用于海水提溴.主要工业生产流程如下图所示。

 ,利用了
,利用了 的氧化性,写出对应反应的离子方程式
的氧化性,写出对应反应的离子方程式②吹出塔中通入热空气吹出
 ,利用了
,利用了 的
的A.氧化性 B.还原性 C.挥发性,沸点比水低 D.易溶于水
(4)实验室可以利用蒸馏的方法进行海水淡化,可选用如图装置完成。
①仪器B的名称是
②该装置中有一处明显的错误是

您最近一年使用:0次
名校
3 .  是一种常见的化肥,某工厂用石膏、
是一种常见的化肥,某工厂用石膏、 、
、 和
和 制备
制备 的工艺流程如下:
的工艺流程如下:
(1)通入 和
和 的顺序
的顺序__________ (填“能”或“否”)互换,原因为____________ 。
(2)工序②中反应的离子方程式为______________ 。
(3)工序②中 气体要适量,判断其未过量的简单实验方法是取少量滤液于试管中,滴加少量
气体要适量,判断其未过量的简单实验方法是取少量滤液于试管中,滴加少量______ 溶液,若无浑浊出现则 未过量。
未过量。
(4)下列仪器在工序③中不需要的是___________ (填序号)。
①分液漏斗 ②蒸发皿 ③玻璃棒 ④坩埚 ⑤烧杯
(5)工序④的操作步骤为_____________ 、____________ 、过滤、洗涤、干燥。
(6)工厂后面还可以如何操作,提高制备 的经济效益
的经济效益_______________ 。
 是一种常见的化肥,某工厂用石膏、
是一种常见的化肥,某工厂用石膏、 、
、 和
和 制备
制备 的工艺流程如下:
的工艺流程如下:
(1)通入
 和
和 的顺序
的顺序(2)工序②中反应的离子方程式为
(3)工序②中
 气体要适量,判断其未过量的简单实验方法是取少量滤液于试管中,滴加少量
气体要适量,判断其未过量的简单实验方法是取少量滤液于试管中,滴加少量 未过量。
未过量。(4)下列仪器在工序③中不需要的是
①分液漏斗 ②蒸发皿 ③玻璃棒 ④坩埚 ⑤烧杯
(5)工序④的操作步骤为
(6)工厂后面还可以如何操作,提高制备
 的经济效益
的经济效益
您最近一年使用:0次
名校
4 . 下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是
| 物质(括号内为杂质) | 除杂试剂 | |
| A | 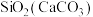 | 稀盐酸 |
| B | 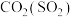 |  溶液 溶液 |
| C | 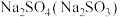 | 稀 |
| D | 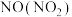 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 由重晶石矿(主要成分是 ,含
,含 等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
 ,含
,含 等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是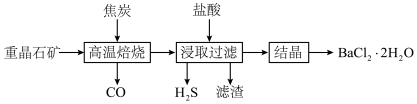
| A.“高温焙烧”前将原料研磨处理,能加快“高温焙烧”的反应速率 |
B.“高温焙烧”时只有 被C还原 被C还原 |
| C.“浸取过滤”发生的主要反应是氧化还原反应 |
| D.“高温焙烧”和“结晶”两处操作均需用到蒸发皿 |
您最近一年使用:0次
名校
6 . 某硫酸厂用硫铁矿焙烧后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制备绿矾粗产品(FeSO4·7H2O),设计了如下流程:
回答下列问题:
(1)“试剂a”的化学式为___________ ,“操作”的名称是___________ 。
(2)“酸浸”后溶液呈黄色,“还原”操作是向溶液逐步加入试剂b,溶液变为浅绿色,写出溶液变为浅绿色的离子方程式___________ 。
(3)在“调pH至5-6”步骤中,写出生成Al(OH)3的离子方程式___________ 。
(4)鉴别“滤液1”中金属阳离子的实验方案:取少量滤液1进行___________ (填实验名称),若观察到火焰呈黄色,则证明含有Na+;另外取少量滤液1于试管中,依次滴入___________ 和氯水,若实验现象依次为溶液先无红色,后变红色,则证明含有Fe2+,写出该过程中属于氧化还原反应的离子方程式___________ 。

回答下列问题:
(1)“试剂a”的化学式为
(2)“酸浸”后溶液呈黄色,“还原”操作是向溶液逐步加入试剂b,溶液变为浅绿色,写出溶液变为浅绿色的离子方程式
(3)在“调pH至5-6”步骤中,写出生成Al(OH)3的离子方程式
(4)鉴别“滤液1”中金属阳离子的实验方案:取少量滤液1进行
您最近一年使用:0次
名校
解题方法
7 . 某工业废水中存在大量的 和
和 ,欲除去废水中的Cu2+和
,欲除去废水中的Cu2+和 ,设计工艺流程如图所示:
,设计工艺流程如图所示:___________ 。
a.烧杯 b.托盘天平 c.漏斗 d.玻璃棒 e.量筒
(2)a溶液和b溶液分别是___________ ,___________ (填溶质化学式)。
(3)溶液A→混合物B过程中可观察到有白色沉淀___________ 生成(填化学式),如何证明溶液中含有硫酸根离子:_______________ 。
(4)混合物B→溶液C过程中所涉及的离子方程式是___________ 。
(5)加入适量盐酸的作用是___________ 。
 和
和 ,欲除去废水中的Cu2+和
,欲除去废水中的Cu2+和 ,设计工艺流程如图所示:
,设计工艺流程如图所示:
a.烧杯 b.托盘天平 c.漏斗 d.玻璃棒 e.量筒
(2)a溶液和b溶液分别是
(3)溶液A→混合物B过程中可观察到有白色沉淀
(4)混合物B→溶液C过程中所涉及的离子方程式是
(5)加入适量盐酸的作用是
您最近一年使用:0次
名校
8 . 从海水中提取澳的工业流程如图,下列说法正确的是

| A.海水晒盐利用的是蒸发结晶法 |
| B.获取Cl2的同时可以得到金属钠,通常采用热分解法 |
| C.步骤Ⅱ中溴与碳酸钠反应中氧化剂与还原剂物质的量之比为1:1 |
| D.实验室分离溴还可以用溶剂萃取法,乙醇可以用作溴的萃取剂 |
您最近一年使用:0次
名校
解题方法
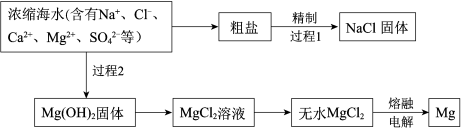
9 . 浩瀚的海洋中蕴藏着丰富的资源。
过程1除去粗盐中的Ca2+、Mg2+、SO 杂质时,粗盐溶解后加入沉淀剂:a.过量的Na2CO3溶液b.过量的BaCl2溶液c.过量的NaOH溶液过滤除去沉淀,再加入适量的盐酸。
杂质时,粗盐溶解后加入沉淀剂:a.过量的Na2CO3溶液b.过量的BaCl2溶液c.过量的NaOH溶液过滤除去沉淀,再加入适量的盐酸。
①加入沉淀剂的顺序正确的是___________ (填序号)。
A.abc B.bac C.cba
②加入适量盐酸,反应的离子方程式有2H++CO =H2O+CO2↑和
=H2O+CO2↑和___________ 。
(2)海水提镁。
过程2中加入的试剂是___________ 。由无水MgCl2获得Mg的化学方程式是___________ 。
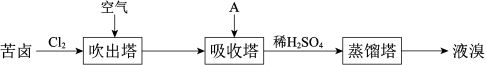
(3)海水提溴。
主要工业生产流程如下图所示:___________ 。
②吸收塔中,A吸收了Br2后的溶液中含有Br‒和BrO ,则A是
,则A是___________ (填序号)。
a.NaCl溶液 b.Na2CO3溶液 c.SO2气体
③从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是___________ 。
过程1除去粗盐中的Ca2+、Mg2+、SO
 杂质时,粗盐溶解后加入沉淀剂:a.过量的Na2CO3溶液b.过量的BaCl2溶液c.过量的NaOH溶液过滤除去沉淀,再加入适量的盐酸。
杂质时,粗盐溶解后加入沉淀剂:a.过量的Na2CO3溶液b.过量的BaCl2溶液c.过量的NaOH溶液过滤除去沉淀,再加入适量的盐酸。①加入沉淀剂的顺序正确的是
A.abc B.bac C.cba
②加入适量盐酸,反应的离子方程式有2H++CO
 =H2O+CO2↑和
=H2O+CO2↑和(2)海水提镁。
过程2中加入的试剂是
(3)海水提溴。
主要工业生产流程如下图所示:
②吸收塔中,A吸收了Br2后的溶液中含有Br‒和BrO
 ,则A是
,则A是a.NaCl溶液 b.Na2CO3溶液 c.SO2气体
③从吸收塔出来的溶液中加入稀H2SO4得到Br2的离子方程式是
您最近一年使用:0次
2024-05-27更新
|
389次组卷
|
2卷引用:北师大附属实验中学2023-2024学年度第二学期期中试卷
名校
10 . 氮化硅( )是一种高温结构陶瓷材料,它硬度大、熔点高、化学性质稳定。合成氮化硅的一种工艺流程如图所示。下列说法正确的是
)是一种高温结构陶瓷材料,它硬度大、熔点高、化学性质稳定。合成氮化硅的一种工艺流程如图所示。下列说法正确的是 在潮湿的空气中易水解,产生白雾
在潮湿的空气中易水解,产生白雾
 )是一种高温结构陶瓷材料,它硬度大、熔点高、化学性质稳定。合成氮化硅的一种工艺流程如图所示。下列说法正确的是
)是一种高温结构陶瓷材料,它硬度大、熔点高、化学性质稳定。合成氮化硅的一种工艺流程如图所示。下列说法正确的是
 在潮湿的空气中易水解,产生白雾
在潮湿的空气中易水解,产生白雾A.该流程中可循环使用的物质是 |
| B.第③步反应是氧化还原反应 |
C. 因为硬度大不属于无机非金属材料 因为硬度大不属于无机非金属材料 |
D.第③步反应可用氨水代替 |
您最近一年使用:0次



