名校
解题方法
1 . 实验室用 和浓盐酸制取
和浓盐酸制取 并回收
并回收 ,下列装置不能达到实验目的的是
,下列装置不能达到实验目的的是
 和浓盐酸制取
和浓盐酸制取 并回收
并回收 ,下列装置不能达到实验目的的是
,下列装置不能达到实验目的的是A.制备氯气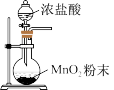 | B.收集氯气 |
C.过滤除MnO2 | D.浓缩滤液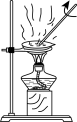 |
您最近一年使用:0次
2023-08-21更新
|
148次组卷
|
5卷引用:广西河池市八校2021-2022学年高二下学期第二次联考化学试题
2 . MnSO4是一种重要的化工产品。以菱锰矿(主要成分为MnCO3,还含有Fe3O4、FeO、CoO等)为原料制备MnSO4的工艺流程如图所示。

金属离子成的pH:
(1)写出酸浸池中MnCO3溶解的离子方程式:____ 。
(2)沉淀池1中,先加MnO2充分反应后再加氨水。写出加氨水时发生反应的离子方程式:____ 。
(3)沉淀池2中,____ (填“能”或“不能”)用NaOH代替含硫沉淀剂,原因是____ 。
(4)用酸性高锰酸钾溶液可以检验Mn2+,产生黑色沉淀,该反应的离子方程式为____ 。
(5)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下:
i.称取ωg废渣,加酸将锰元素全部溶出成Mn2+,过滤,将滤液定容于250mL容量瓶中;
ii.取25.00mL溶液于锥形瓶中,加入少量催化剂和过量(NH4)2S2O8溶液,加热、充分反应后,煮沸溶液使过量的(NH4)2S2O8分解。
iii.加入指示剂,用xmol·L-1(NH4)2Fe(SO4)2溶液滴定。滴定至终点时消耗(NH4)2Fe(SO4)2溶液的体积为ymL,MnO 重新转化成Mn2+。
重新转化成Mn2+。
①步骤iii中反应的离子方程式为____ 。
②废渣中锰元素的质量分数为___ 。
(6)电解MnSO4溶液可获得二氧化锰,电解后的废水中还含有Mn2+,可用碱性溶液进行沉降得到Mn(OH)2沉淀。欲使溶液中c(Mn2+)≤1.0×10-5mol·L-1,则应使溶液中c(OH-)≥____ mol·L-1。

金属离子成的pH:
| 金属离子 | Fe3+ | Fe2+ | Co2+ | Mn2+ |
| 开始沉淀时的pH | 1.5 | 6.3 | 7.4 | 7.6 |
| 完全沉淀时的pH | 2.8 | 8.3 | 94 | 10.2 |
(2)沉淀池1中,先加MnO2充分反应后再加氨水。写出加氨水时发生反应的离子方程式:
(3)沉淀池2中,
(4)用酸性高锰酸钾溶液可以检验Mn2+,产生黑色沉淀,该反应的离子方程式为
(5)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下:
i.称取ωg废渣,加酸将锰元素全部溶出成Mn2+,过滤,将滤液定容于250mL容量瓶中;
ii.取25.00mL溶液于锥形瓶中,加入少量催化剂和过量(NH4)2S2O8溶液,加热、充分反应后,煮沸溶液使过量的(NH4)2S2O8分解。
iii.加入指示剂,用xmol·L-1(NH4)2Fe(SO4)2溶液滴定。滴定至终点时消耗(NH4)2Fe(SO4)2溶液的体积为ymL,MnO
 重新转化成Mn2+。
重新转化成Mn2+。①步骤iii中反应的离子方程式为
②废渣中锰元素的质量分数为
(6)电解MnSO4溶液可获得二氧化锰,电解后的废水中还含有Mn2+,可用碱性溶液进行沉降得到Mn(OH)2沉淀。欲使溶液中c(Mn2+)≤1.0×10-5mol·L-1,则应使溶液中c(OH-)≥
您最近一年使用:0次
解题方法
3 . 开发利用海水化学资源的部分过程如图所示,下列说法不正确的是
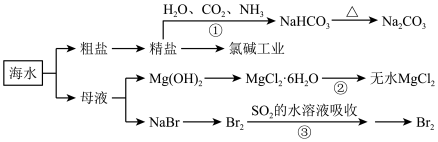

| A.①的操作是先通入足量的NH3,再通入CO2 |
| B.不可以用澄清石灰水鉴别NaHCO3和Na2CO3溶液 |
C.③的离子方程式为Br2+ SO2 +2H2O=2H+ +SO +2HBr +2HBr |
D.除去粗盐溶液中的Ca2+、Mg2+、SO ,可依次加入NaOH、BaCl2、Na2CO3溶液,过滤后再加盐酸 ,可依次加入NaOH、BaCl2、Na2CO3溶液,过滤后再加盐酸 |
您最近一年使用:0次
名校
解题方法
4 . 钴(Co)及其化合物在工业上广泛应用于磁性材料、电池材料及超硬材料等领域。某学习小组欲从某工业废料中回收钴,设计工艺流程如下:(废料中含有Al、Co2O3和Fe2O3等物质)。
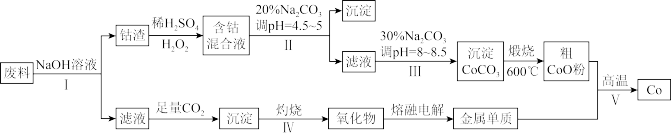
请回答:
(1)废料用NaOH溶液处理前通常先将废料粉碎,其目的是____________ 。
(2)过程Ⅱ用稀H2SO4和H2O2溶液与Co2O3反应而达到浸出钴的目的,请写出该反应的离子方程式___________ 。在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请分析不用盐酸浸出钴的主要原因______________ 。
(3)碳酸钠溶液在过程Ⅱ和Ⅲ中所起作用有所不同,请写出碳酸钠在过程Ⅱ中发生反应生成沉淀的离子方程式__________________________________ 。
(4) 若在实验室中完成过程Ⅳ,则沉淀物需在__________________ (填仪器名称)中灼烧;写出在过程Ⅴ中发生反应的化学方程式__________________________________ 。
(5)将1.0×10-3 mol/LCoSO4与1.2×10-3mol/L的Na2CO3等体积混合,此时溶液中的Co2+的浓度为__________ mol/L。(已知:CoCO3的溶度积为:Ksp=1.0×10-13)
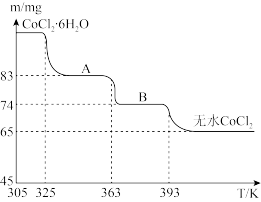
(6)CoO与盐酸反应可得粉红色的CoCl2溶液。CoCl2晶体因结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。如图是粉红色的CoCl2·6H2O晶体在烘箱中受热分解时,剩余固体质量随温度变化的曲线,物质A的化学式是____________________ 。

请回答:
(1)废料用NaOH溶液处理前通常先将废料粉碎,其目的是
(2)过程Ⅱ用稀H2SO4和H2O2溶液与Co2O3反应而达到浸出钴的目的,请写出该反应的离子方程式
(3)碳酸钠溶液在过程Ⅱ和Ⅲ中所起作用有所不同,请写出碳酸钠在过程Ⅱ中发生反应生成沉淀的离子方程式
(4) 若在实验室中完成过程Ⅳ,则沉淀物需在
(5)将1.0×10-3 mol/LCoSO4与1.2×10-3mol/L的Na2CO3等体积混合,此时溶液中的Co2+的浓度为
(6)CoO与盐酸反应可得粉红色的CoCl2溶液。CoCl2晶体因结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。如图是粉红色的CoCl2·6H2O晶体在烘箱中受热分解时,剩余固体质量随温度变化的曲线,物质A的化学式是

您最近一年使用:0次
2019-12-05更新
|
342次组卷
|
4卷引用:广西河池高级中学2022届高三下学期4月考试理科综合化学试题
广西河池高级中学2022届高三下学期4月考试理科综合化学试题陕西省西安市长安区第一中学2022-2023学年高三上学期第二次质量检测化学试题湖北省示范高中2019~2020学年高三11月月考理综化学试题(已下线)考点17 化工生产诸要素及流程图分析-2020年高考化学命题预测与模拟试题分类精编



