解题方法
1 . 下列有关实验说法正确的是
| A.碱液不慎溅到手上,先用大量水冲洗,再用饱和小苏打溶液洗,最后用水冲洗 |
| B.用容量瓶配制溶液时,容量瓶洗涤后必须干燥后再使用 |
| C.KCl和MnO2的混合物经溶解、过滤、洗涤、干燥,可分离出MnO2 |
| D.火柴头的浸泡液中滴加AgNO3溶液、稀HNO3,可检验火柴头是否含有氯元素 |
您最近一年使用:0次
2 . 下列说法不正确 的是
| A.往浸过火柴头的溶液中加入硝酸酸化的硝酸银溶液,可检验火柴头中含氯元素 |
| B.减压过滤不适用于过滤胶状类沉淀,是因沉淀容易透过滤纸,无法实现固液分离 |
C.实验中常用摩尔盐代替硫酸亚铁,是因为摩尔盐中 比硫酸亚铁中 比硫酸亚铁中 要稳定,不易被氧化 要稳定,不易被氧化 |
D.探究 与稀硫酸反应速率的影响因素时,可以通过观察产生浑浊的速率来判断反应的快慢 与稀硫酸反应速率的影响因素时,可以通过观察产生浑浊的速率来判断反应的快慢 |
您最近一年使用:0次
名校
解题方法
3 . 草木灰主要成分是 K2CO3、KCl、K2SO4和不溶于水的杂质。化学实验组为了制取 KCl晶体,设计了如图流程。以下说法错误的是
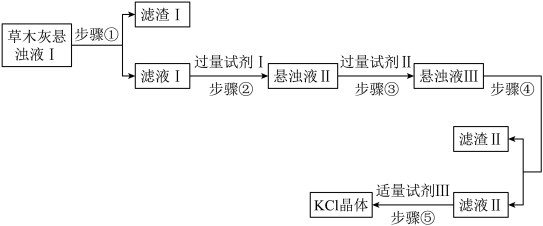

| A.步骤①中用到的玻璃仪器为:烧杯、漏斗、玻璃棒 |
| B.试剂Ⅰ是过量 Ba(NO3)2溶液除去 K2CO3、K2SO4 |
| C.过量试剂Ⅱ是 K2CO3,除去过量 BaCl2 |
| D.步骤⑤操作的名称是蒸发、结晶 |
您最近一年使用:0次
2021-10-13更新
|
755次组卷
|
10卷引用:浙江省诸暨市海亮高级中学2021-2022学年高一上学期期中考试化学试题
浙江省诸暨市海亮高级中学2021-2022学年高一上学期期中考试化学试题北京市中关村中学2020-2021学年高一上学期期中考试化学试题甘肃省甘谷县第四中学2021-2022学年高一上学期第二阶段考(期中)化学试题重庆市缙云教育联盟2021-2022学年高二11月质量检测化学试题天津市第三中学2021-2022学年高一上学期期中考试化学试题江苏省盐城市伍佑中学2021-2022学年高一上学期期中考试化学试题福建师范大学附属中学2021-2022学年高一上学期期末考试化学试题新疆沙湾县第一中学2021-2022学年高一上学期期中考试化学试题天津市西青区杨柳青第一中学2021-2022学年高一下学期期末适应性测试化学试题期中学业水平测试
4 . 下列说法正确的是
| A.抽滤时,用倾析法转移沉淀,再转移溶液,然后开大水龙头进行抽滤 |
| B.一些有机溶剂苯、四氯化碳、乙醚等极易被引燃,使用时必须远离明火和热源 |
| C.抽滤得阿司匹林粗产品后,先用冷水洗涤晶体,再用酒精洗涤,加快干燥 |
| D.MnO2催化双氧水分解时,其用量和颗粒直径大小均会影响双氧水分解的速率 |
您最近一年使用:0次
5 . 在中学化学实验中学过的可用于分离或提纯物质的方法很多,如重结晶、过滤、盐析……。请将分离或提纯下列各混合物最适宜方法的名称填到横线上。
(1)除去氯化钠溶液中的石灰石:____ 。
(2)除去碘中混有的碘化钠固体:____ 。
(3)除去乙醇中溶解的少量食盐:____ 。
(4)除去Fe(OH)3胶体中混有的Cl-:____ 。
(1)除去氯化钠溶液中的石灰石:
(2)除去碘中混有的碘化钠固体:
(3)除去乙醇中溶解的少量食盐:
(4)除去Fe(OH)3胶体中混有的Cl-:
您最近一年使用:0次
2021高三·浙江·专题练习
解题方法
6 . 亚铁盐在空气中易被氧化,但形成复盐可稳定存在。硫酸亚铁铵[(NH4)2SO4•FeSO4•6H2O]是一种重要化学试剂,实验室可用纯铁片来制取硫酸亚铁铵,流程如图:

请回答下列问题:
(1)操作Ⅰ的名称是___ ,所用主要仪器和用品有___ (铁架台、铁圈除外)。
(2)若A物质为CuSO4,其加入的目的是___ ,则固体B的成分为___ 。
(3)加少量硫酸可以调节pH为1~2,其作用是___ 。
(4)假设在水溶液中硫酸氢钠如此电离:NaHSO4=Na++H++SO 。物质的量浓度相同的①氨水;②氯化铵;③碳酸氢铵;④硫酸氢铵;⑤硫酸铵;⑥硫酸亚铁铵(NH4)2Fe(SO4)2)溶液6种溶液中c(
。物质的量浓度相同的①氨水;②氯化铵;③碳酸氢铵;④硫酸氢铵;⑤硫酸铵;⑥硫酸亚铁铵(NH4)2Fe(SO4)2)溶液6种溶液中c( )由大到小的顺序是
)由大到小的顺序是___ ,溶液pH由大到小的顺序是___ 。

请回答下列问题:
(1)操作Ⅰ的名称是
(2)若A物质为CuSO4,其加入的目的是
(3)加少量硫酸可以调节pH为1~2,其作用是
(4)假设在水溶液中硫酸氢钠如此电离:NaHSO4=Na++H++SO
 。物质的量浓度相同的①氨水;②氯化铵;③碳酸氢铵;④硫酸氢铵;⑤硫酸铵;⑥硫酸亚铁铵(NH4)2Fe(SO4)2)溶液6种溶液中c(
。物质的量浓度相同的①氨水;②氯化铵;③碳酸氢铵;④硫酸氢铵;⑤硫酸铵;⑥硫酸亚铁铵(NH4)2Fe(SO4)2)溶液6种溶液中c( )由大到小的顺序是
)由大到小的顺序是
您最近一年使用:0次
7 . 下列说法不正确 的是
| A.重结晶时,溶液冷却速度越慢得到的晶体颗粒越大 |
| B.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
| C.抽滤装置由布氏漏斗、吸滤瓶、安全瓶、抽气泵等仪器组成,工作的主要原理是抽气泵给吸滤瓶减压,导致装置内部的压强降低,使过滤的速度加快 |
| D.硝酸钾饱和溶液冷却未出现结晶时,可以用玻璃棒充分磨擦器皿壁,促使晶体析出 |
您最近一年使用:0次
8 . 减压过滤装置和普通过滤装置相比,除可加快过滤速度外,还具有的优点是
| A.可得到较干燥的沉淀 | B.可减少沉淀中的杂质 |
| C.可过滤胶状的沉淀 | D.可过滤颗粒更小的沉淀 |
您最近一年使用:0次
9 . 下列说法不正确的是
| A.用抽滤法快速分离氢氧化铁胶状沉淀和氯化钠溶液 |
| B.纸上层析属于色谱分析法,其原理跟“毛细现象”相关 |
| C.在提纯鸡蛋清中的蛋白质时,可向鸡蛋清溶液中加入浓(NH4)2SO4溶液,然后将所得沉淀滤出,即得较纯的蛋白质 |
| D.洗涤沉淀时,不能用玻璃棒轻轻搅拌沉淀,会把滤纸捅破 |
您最近一年使用:0次
10 . 硫酸铜晶体在工农业生产中具有重要作用。某学习小组对硫酸铜晶体的制备和纯度的测定进行如下探究。
(1)粗硫酸铜晶体的制备
在盛有铜屑的蒸发皿中加入20 mL 3 mol·L-1的硫酸,水浴加热,分多次缓慢加入浓硝酸,待反应缓和后,盖上表面皿。将所得溶液加热浓缩、趁热过滤,冷却,得到粗硫酸铜晶体。反应原理为浓硝酸将铜氧化成Cu2+,Cu2+与SO 结合得到硫酸铜,该反应的化学方程式为
结合得到硫酸铜,该反应的化学方程式为___________ 。
(2)硫酸铜晶体的提纯
实验室提纯硫酸铜晶体的一种方法如下:

①提纯过程中需要加入氧化剂,检验其氧化完全的方法是___________ 。
②溶液中金属离子开始沉淀和沉淀完全的pH如下表所示。提纯过程中需要调节pH=4.0,其原因是___________ 。
③操作I、II、III都要用到的玻璃仪器有___________ 。
(3)硫酸铜晶体纯度的测定
称取样品0.3125 g于250 mL锥形瓶中,加入适量稀硫酸和水使之完全溶解。加入过量的KI溶液(杂质不参与反应),再加入几滴淀粉溶液,用0.1000 mol·L-1 Na2S2O3溶液滴定至终点时消耗Na2S2O3溶液10.00 mL。(已知:2Cu2++4I-=2CuI↓+I2,I2+2S2O =S4O
=S4O +2I-),则所测试样中硫酸铜晶体的纯度为
+2I-),则所测试样中硫酸铜晶体的纯度为___________ 。
(1)粗硫酸铜晶体的制备
在盛有铜屑的蒸发皿中加入20 mL 3 mol·L-1的硫酸,水浴加热,分多次缓慢加入浓硝酸,待反应缓和后,盖上表面皿。将所得溶液加热浓缩、趁热过滤,冷却,得到粗硫酸铜晶体。反应原理为浓硝酸将铜氧化成Cu2+,Cu2+与SO
 结合得到硫酸铜,该反应的化学方程式为
结合得到硫酸铜,该反应的化学方程式为(2)硫酸铜晶体的提纯
实验室提纯硫酸铜晶体的一种方法如下:

①提纯过程中需要加入氧化剂,检验其氧化完全的方法是
②溶液中金属离子开始沉淀和沉淀完全的pH如下表所示。提纯过程中需要调节pH=4.0,其原因是
| 金属离子 | Fe3+ | Cu2+ |
| 开始沉淀时的pH | 1.9 | 4.7 |
| 沉淀完全时的pH | 3.2 | 6.7 |
(3)硫酸铜晶体纯度的测定
称取样品0.3125 g于250 mL锥形瓶中,加入适量稀硫酸和水使之完全溶解。加入过量的KI溶液(杂质不参与反应),再加入几滴淀粉溶液,用0.1000 mol·L-1 Na2S2O3溶液滴定至终点时消耗Na2S2O3溶液10.00 mL。(已知:2Cu2++4I-=2CuI↓+I2,I2+2S2O
 =S4O
=S4O +2I-),则所测试样中硫酸铜晶体的纯度为
+2I-),则所测试样中硫酸铜晶体的纯度为
您最近一年使用:0次



