1 . 某研究小组拟在实验室以废铁屑(含有少量炭和 杂质)为原料制备无水
杂质)为原料制备无水 ,设计如下流程(已知
,设计如下流程(已知 易水解):
易水解):不正确 的是
 杂质)为原料制备无水
杂质)为原料制备无水 ,设计如下流程(已知
,设计如下流程(已知 易水解):
易水解):
| A.试剂X可选用硫酸 |
B.“氧化”时: |
| C.操作①②均需用到漏斗、烧杯、玻璃棒 |
| D.“脱水”时可能会产生亚铁盐 |
您最近一年使用:0次
2 . 为除去粗盐中的CaCl2、MgCl2、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):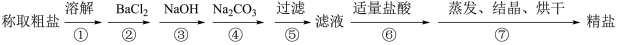
(1)判断BaCl2已过量的方法是___________ 。
(2)第④步中,相关的化学方程式是___________ 。
(3)过滤操作中,需要用到的玻璃仪器有___________ 。
(1)判断BaCl2已过量的方法是
(2)第④步中,相关的化学方程式是
(3)过滤操作中,需要用到的玻璃仪器有
您最近一年使用:0次
3 . 下列关于过滤操作的表述,错误的是
| A.漏斗下口尖端紧靠烧杯壁 | B.玻璃棒有引流的作用 |
| C.将滤纸湿润,使其紧贴漏斗壁 | D.用玻璃棒在漏斗中轻轻搅动以加快过滤速度 |
您最近一年使用:0次
4 . 下列实验装置及操作都正确的是
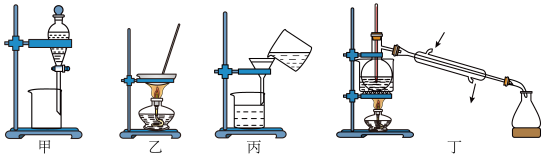

| A.图甲:萃取中的分液过程 | B.图乙:蒸干溶液制碳酸氢钠固体 |
C.图丙:过滤 悬浊液 悬浊液 | D.图丁:蒸馏自来水获取蒸馏水 |
您最近一年使用:0次
2024-01-10更新
|
116次组卷
|
2卷引用:福建省福州延安中学2023-2024学年高一上学期11月期中考试化学试题
名校
5 . 无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。
。

下列说法不正确的是
 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。
。
下列说法不正确的是
A.试剂 可以选用 可以选用 溶液,其目的是氧化 溶液,其目的是氧化 |
| B.操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和漏斗 |
C.操作②中,加热的同时通入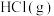 的目的是防止水解 的目的是防止水解 |
D.反应 的化学方程式为 的化学方程式为 |
您最近一年使用:0次
6 . SO2是有毒气体,任意排放会造成环境污染。若加以利用,可以变废为宝。下图为SO2的无害化处理流程图,回答下列问题:
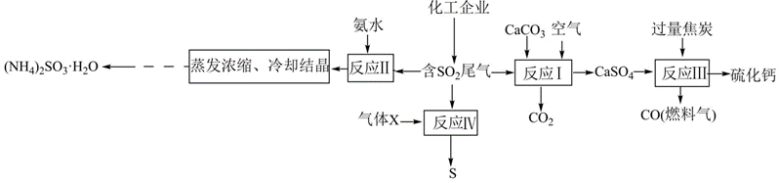
(1)“反应I”在高温条件下进行,写出该反应的化学方程式:___________ 。
(2)X可能为___________ (填化学式),电子式为___________ ,该反应说明SO2具有___________ (填“氧化性”或“还原性”)。
(3)“蒸发浓缩、冷却结晶”后获得 固体的操作是
固体的操作是___________ 。
(4) 暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:
暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:________ 。
A.稀硝酸,BaCl2 B.稀盐酸,BaCl2 C.稀盐酸,硝酸钡

(1)“反应I”在高温条件下进行,写出该反应的化学方程式:
(2)X可能为
(3)“蒸发浓缩、冷却结晶”后获得
 固体的操作是
固体的操作是(4)
 暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:
暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:A.稀硝酸,BaCl2 B.稀盐酸,BaCl2 C.稀盐酸,硝酸钡
您最近一年使用:0次
7 . FeF3是制备硫化物全固态锂电池高能正极材料的原料。一种制备FeF3材料的微型流程如下。下列说法正确的是:
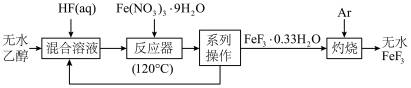

| A.混合溶液时需要用到的实验仪器有:烧杯、玻璃棒 |
| B.系列操作为涉及到蒸发浓缩、冷却结晶、过滤、洗涤、蒸馏 |
| C.该实验反应器中的温度越高,越有利于得到产品 |
| D.灼烧时通入Ar的作用是除去可能混入的HF、HNO3蒸汽等 |
您最近一年使用:0次
名校
解题方法
8 . 青蒿素是高效的抗疟疾药,为无色针状晶体,易溶于有机溶剂,在水中几乎不溶,熔点为 ,热稳定性差。提取青蒿素的主要工艺如下。(已知:乙醚的沸点为
,热稳定性差。提取青蒿素的主要工艺如下。(已知:乙醚的沸点为 )下列说法不正确的是
)下列说法不正确的是
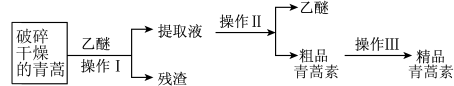
 ,热稳定性差。提取青蒿素的主要工艺如下。(已知:乙醚的沸点为
,热稳定性差。提取青蒿素的主要工艺如下。(已知:乙醚的沸点为 )下列说法不正确的是
)下列说法不正确的是
| A.破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素浸取率 |
| B.操作Ⅰ需要用到的玻璃仪器有分液漏斗、玻璃棒、烧杯 |
| C.操作Ⅱ利用了乙醚与青蒿素的沸点相差较大 |
| D.操作Ⅲ为重结晶 |
您最近一年使用:0次
名校
9 . 物质的分离、提纯和定量测定是研究物质的方法。
(1)选择下列实验方法分离物质,将分离方法的序号填在横线上。
a.萃取分液b.升华c.结晶d.过滤e.蒸馏f.分液
①从碘水中提取碘单质_____ ;
②分离水和汽油的混合物_____ ;
③从硝酸钾和氯化钠的混合液中获得硝酸钾_____ ;
现有 、
、 和
和 的混合物,选择适当的试剂除去杂质,从而得到纯净的
的混合物,选择适当的试剂除去杂质,从而得到纯净的 晶体,相应的实验流程如图所示。
晶体,相应的实验流程如图所示。
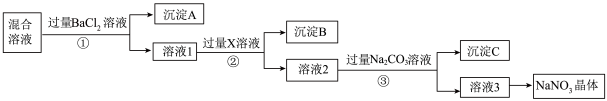
(2)写出实验流程中下列物质的化学式:沉淀A_____ ,试剂X_____ 。
(3)上述实验流程中①②③步均要进行的实验操作是_____ (填操作名称)。
(4)上述实验流程中加入过量 溶液的目的是
溶液的目的是_____ 。
(5)按此实验方案得到的溶液3中肯定含有_____ (填化学式)杂质。为了解决这个问题,可以向溶液3中加入适量的_____ (填化学式)
(1)选择下列实验方法分离物质,将分离方法的序号填在横线上。
a.萃取分液b.升华c.结晶d.过滤e.蒸馏f.分液
①从碘水中提取碘单质
②分离水和汽油的混合物
③从硝酸钾和氯化钠的混合液中获得硝酸钾
现有
 、
、 和
和 的混合物,选择适当的试剂除去杂质,从而得到纯净的
的混合物,选择适当的试剂除去杂质,从而得到纯净的 晶体,相应的实验流程如图所示。
晶体,相应的实验流程如图所示。
(2)写出实验流程中下列物质的化学式:沉淀A
(3)上述实验流程中①②③步均要进行的实验操作是
(4)上述实验流程中加入过量
 溶液的目的是
溶液的目的是(5)按此实验方案得到的溶液3中肯定含有
您最近一年使用:0次
解题方法
10 . 某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物。试回答下列问题:
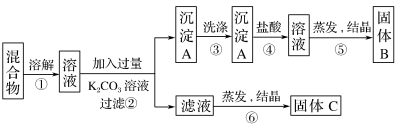
(1)操作①用玻璃棒搅拌的目的是___________ ;操作②所需的玻璃仪器有烧杯、玻璃棒、__________ 。
(2)B的化学式为___________ 。
(3)该方案的明显失误是因某一步设计不当而使分离的产物KCl不纯,该步骤是___________ (填序号),改进措施是往滤液中滴加过量___________ 以除去多余的杂质离子再结晶。
(4)写出④对应的化学反应方程式___________ 。

(1)操作①用玻璃棒搅拌的目的是
(2)B的化学式为
(3)该方案的明显失误是因某一步设计不当而使分离的产物KCl不纯,该步骤是
(4)写出④对应的化学反应方程式
您最近一年使用:0次



