名校
1 . Li2CO3是制备锂离子电极材料LiFePO4的重要原料。以盐湖卤水(主要含有NaCl、MgCl2、LiCl和Na2B4O7等)为原料提取Li2CO3并制备LiFePO4的工艺流程如图所示:

已知:“日晒蒸发喷雾干燥”后固体含NaCl、LiCl、MgCl2•6H2O等。
(1)硼酸在水中的溶解度随温度的变化关系如图所示:
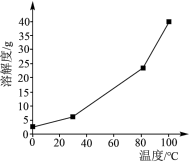
已知:H3BO3+H2O⇌[B(OH)4]-+H+。6.2gH3BO3最多与______ mL2.5mol/LNaOH溶液完全反应。“酸化脱硼”中采用______ (填“加热”或“冷却”),其目的是______ 。
(2)“水浸”后的溶液中溶质的主要成分是______ 。
(3)“蒸发分解”生成Li2CO3的化学方程式为______ 。
(4)已知不同温度下蒸发分解得到Li2CO3的产率及其溶解度随温度的变化关系如图所示。则“蒸发分解”的最佳温度是______ ,制得的Li2CO3沉淀需要进行洗涤,具体操作为______ 。
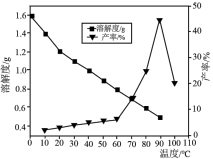
(5)制备LiFePO4时同时生成CO2,其中FePO4与C6H12O6物质的量之比为24:1,该化学反应方程式为______ 。

已知:“日晒蒸发喷雾干燥”后固体含NaCl、LiCl、MgCl2•6H2O等。
(1)硼酸在水中的溶解度随温度的变化关系如图所示:

已知:H3BO3+H2O⇌[B(OH)4]-+H+。6.2gH3BO3最多与
(2)“水浸”后的溶液中溶质的主要成分是
(3)“蒸发分解”生成Li2CO3的化学方程式为
(4)已知不同温度下蒸发分解得到Li2CO3的产率及其溶解度随温度的变化关系如图所示。则“蒸发分解”的最佳温度是

(5)制备LiFePO4时同时生成CO2,其中FePO4与C6H12O6物质的量之比为24:1,该化学反应方程式为
您最近一年使用:0次
解题方法
2 . 玻璃棒是化学实验中的常用仪器。下列有关玻璃棒的使用不合理的是
A. | B. |
C.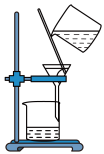 | D.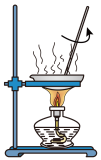 |
您最近一年使用:0次
名校
3 . 下列事实中,可以用胶体性质解释的是
| A.利用醋酸除去水垢 |
B.向 溶液中滴加 溶液中滴加 溶液产生白色沉淀 溶液产生白色沉淀 |
| C.可以用过滤的方法除去粗食盐水中的难溶杂质 |
| D.黑暗的电影院中,放映口发出的光会在影院中形成光柱 |
您最近一年使用:0次
2024-03-12更新
|
114次组卷
|
2卷引用:黑龙江省大庆市大庆中学2023-2024学年高一下学期开学化学试题
名校
解题方法
4 . 从干海带中提取碘的实验流程如下:
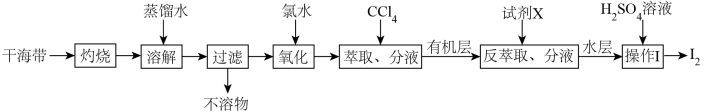
| A.氧化步骤中氯水可用过氧化氢代替 |
B.试剂X可以为 ,反萃取的离子方程式为: ,反萃取的离子方程式为: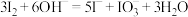 |
C. 可循环利用以有效提高干海带提碘的产率 可循环利用以有效提高干海带提碘的产率 |
| D.操作Ⅰ要用到普通漏斗、烧杯和玻璃棒 |
您最近一年使用:0次
2024-01-28更新
|
573次组卷
|
6卷引用:山东省烟台市莱州市第一中学2023-2024学年高一下学期开学化学试题
5 . 从酸性含铬废水(主要阴离子为 )中回收铬元素(
)中回收铬元素( )的部分工艺流程如图所示。
)的部分工艺流程如图所示。
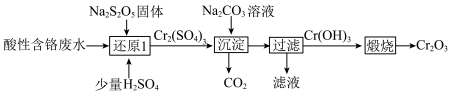
下列有关说法正确的是
 )中回收铬元素(
)中回收铬元素( )的部分工艺流程如图所示。
)的部分工艺流程如图所示。
下列有关说法正确的是
| A.“过滤”时需用玻璃棒搅拌 |
| B.“煅烧”过程中发生了氧化还原反应 |
C.若分别用 、 、 还原等量的 还原等量的 ,消耗 ,消耗 与 与 的物质的量之比为1∶3 的物质的量之比为1∶3 |
D.“还原1”时反应的离子方程式为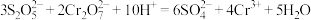 |
您最近一年使用:0次
2024-01-08更新
|
262次组卷
|
6卷引用:内蒙古自治区乌兰浩特第一中学2023-2024学年高一下学期开学考试化学试题
解题方法
6 . 早在战国时期,《周礼·考工记》就记载了我国劳动人民制取氢氧化钾以漂洗丝帛的工艺。大意是:先将干燥的木头烧成灰(含 ),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。
),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。

(1)操作a要用到的玻璃仪器有烧杯、玻璃棒和________ 。
(2)反应过程中未涉及的基本反应类型是________ 。
(3)反应过程中能够循环利用的物质是________ (填化学式)。
(4)氢氧化钙与灰汁(含 )反应的化学方程式为
)反应的化学方程式为________ 。
(5)古人不提前制备大量氢氧化钾的原因是________ (用化学方程式表达)。
 ),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。
),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。
(1)操作a要用到的玻璃仪器有烧杯、玻璃棒和
(2)反应过程中未涉及的基本反应类型是
(3)反应过程中能够循环利用的物质是
(4)氢氧化钙与灰汁(含
 )反应的化学方程式为
)反应的化学方程式为(5)古人不提前制备大量氢氧化钾的原因是
您最近一年使用:0次
名校
解题方法
7 . 生物浸出技术在金属冶炼中应用广泛。嗜热细菌在65-80℃酸性水溶液及氧气存在下,能氧化黄铜矿(主要成分CuFeS2)产生硫酸盐,进而生产铜和绿矾,主要流程如图:
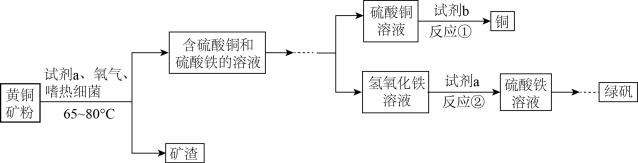
(1)分离出矿渣的操作是_______ 。该操作需要的玻璃仪器有烧杯、玻璃棒、_______ 。
(2)若试剂b为Fe粉,反应①的化学方程式为_______ 。
(3)氢氧化铁与试剂a发生中和反应,试剂a为_______ (填化学式),反应②的化学方程式为_______ 。
(4)最后由硫酸铁溶液获得绿矾晶体(FeSO4∙7H2O)的操作步骤依次为:加适量铁粉、过滤、蒸发浓缩、_______ 、过滤、洗涤、干燥。写出加适量铁粉时发生反应的离子反应方程式_______ 。

(1)分离出矿渣的操作是
(2)若试剂b为Fe粉,反应①的化学方程式为
(3)氢氧化铁与试剂a发生中和反应,试剂a为
(4)最后由硫酸铁溶液获得绿矾晶体(FeSO4∙7H2O)的操作步骤依次为:加适量铁粉、过滤、蒸发浓缩、
您最近一年使用:0次
8 . 工业上利用废渣[ 、
、 及少量CaO和MgO]制备高档颜料铁红(主要成分为
及少量CaO和MgO]制备高档颜料铁红(主要成分为 )和回收
)和回收 。具体生产流程如下:
。具体生产流程如下:
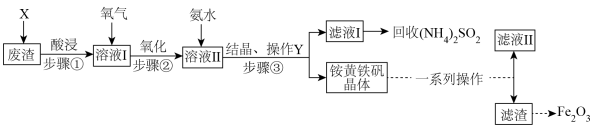
【背景信息】a.氧化步骤中会有元素化合价发生变化。
b.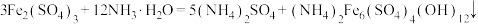 (铵黄铁矾晶体)。
(铵黄铁矾晶体)。
(1)步骤③中“操作Y”的名称是_______ ,必须用到的玻璃仪器有_______ 。
(2)加入物质X溶解废渣,X应选用_______(填标号)。
(3)步骤①“酸浸”时,生成盐的化学方程式为_______ (任写一个)。
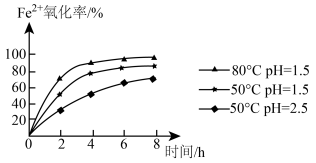
(4)用离子方程式表示步骤②通入氧气氧化的目的:_______ 。工业上该操作的时间一般控制在4小时左右为宜,根据如图有关数据分析 氧化率[
氧化率[ 氧化率=
氧化率=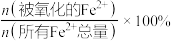 ]的变化规律:
]的变化规律:_______ 。
(5)“滤液Ⅱ”中溶质的主要成分是_______ (填化学式)。
 、
、 及少量CaO和MgO]制备高档颜料铁红(主要成分为
及少量CaO和MgO]制备高档颜料铁红(主要成分为 )和回收
)和回收 。具体生产流程如下:
。具体生产流程如下:
【背景信息】a.氧化步骤中会有元素化合价发生变化。
b.
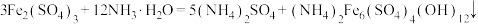 (铵黄铁矾晶体)。
(铵黄铁矾晶体)。(1)步骤③中“操作Y”的名称是
(2)加入物质X溶解废渣,X应选用_______(填标号)。
| A.盐酸 | B.硫酸 | C.氨水 | D.氢氧化钠 |
(4)用离子方程式表示步骤②通入氧气氧化的目的:
 氧化率[
氧化率[ 氧化率=
氧化率=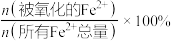 ]的变化规律:
]的变化规律:
(5)“滤液Ⅱ”中溶质的主要成分是
您最近一年使用:0次
9 . 化学实验是化学学习的重要途径。下列实验操作不能达到实验目的的是
| A.鉴别羊毛纤维和合成纤维:取样,分别点燃 |
| B.检验硫酸铝溶液的酸碱性:用玻璃棒蘸取溶液滴到pH试纸上 |
| C.实验室用过氧化氢制取氧气后,回收二氧化锰:过滤、洗涤、干燥 |
| D.除去氧化钙中混有的少量氢氧化钙:加入适量稀盐酸,蒸发 |
您最近一年使用:0次
10 . 水是宝贵的自然资源。下列关于水的说法错误的是
| A.水的天然循环过程中,水分子本身不发生变化 |
| B.利用蒸馏法可以实现海水淡化 |
| C.用滤纸过滤不能除去天然水中溶解的矿物质 |
| D.利用电解水制取氢气,是获得氢能源的理想途径 |
您最近一年使用:0次



