解题方法
1 . 碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。请回答下列问题:
(1)海带中含有丰富的碘,将海带灼烧、浸泡、过滤,所得的滤液中含有丰富的碘离子。在实验室中进行过滤操作时,需要用到的玻璃仪器为___________ 。
(2) 的化学性质与卤素单质类似,
的化学性质与卤素单质类似, 也具有强氧化性,
也具有强氧化性, 可与氢硫酸(
可与氢硫酸( 的水溶液)反应生成淡黄色沉淀和两种强酸,试写出
的水溶液)反应生成淡黄色沉淀和两种强酸,试写出 和氢硫酸反应的化学方程式:
和氢硫酸反应的化学方程式:___________ 。 和
和 溶液反应生成
溶液反应生成 和
和 ,该反应
,该反应___________ 氧化还原反应(填“是”或“不是”)。
(3)加碘食盐中加入的是 。请回答下列问题:
。请回答下列问题:
①在 溶液中滴加少量
溶液中滴加少量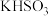 溶液,发生如下反应,请配平并写出该反应方程式
溶液,发生如下反应,请配平并写出该反应方程式___________ 。

②在 溶液中滴加过量
溶液中滴加过量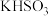 溶液,反应完全,推测反应后溶液中的还原产物为
溶液,反应完全,推测反应后溶液中的还原产物为___________ (填化学式)。(已知:还原性: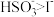 ;氧化性:
;氧化性: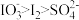 。)
。)
(1)海带中含有丰富的碘,将海带灼烧、浸泡、过滤,所得的滤液中含有丰富的碘离子。在实验室中进行过滤操作时,需要用到的玻璃仪器为
(2)
 的化学性质与卤素单质类似,
的化学性质与卤素单质类似, 也具有强氧化性,
也具有强氧化性, 可与氢硫酸(
可与氢硫酸( 的水溶液)反应生成淡黄色沉淀和两种强酸,试写出
的水溶液)反应生成淡黄色沉淀和两种强酸,试写出 和氢硫酸反应的化学方程式:
和氢硫酸反应的化学方程式: 和
和 溶液反应生成
溶液反应生成 和
和 ,该反应
,该反应(3)加碘食盐中加入的是
 。请回答下列问题:
。请回答下列问题:①在
 溶液中滴加少量
溶液中滴加少量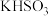 溶液,发生如下反应,请配平并写出该反应方程式
溶液,发生如下反应,请配平并写出该反应方程式
②在
 溶液中滴加过量
溶液中滴加过量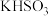 溶液,反应完全,推测反应后溶液中的还原产物为
溶液,反应完全,推测反应后溶液中的还原产物为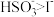 ;氧化性:
;氧化性: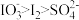 。)
。)
您最近半年使用:0次
2 . 氧化镁是优质的耐高温材料。某兴趣小组利用菱镁矿(主要成分为 ,含有少量
,含有少量 、
、 等杂质)设计制备氧化镁的流程如下:
等杂质)设计制备氧化镁的流程如下:
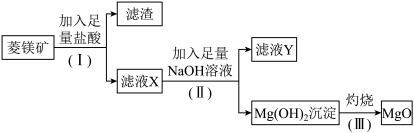
回答下列问题:
(1)步骤(Ⅰ)中分离操作的名称是_________ ,所使用的玻璃仪器有__________ 烧杯、玻璃棒。
(2)步骤(Ⅰ)中分离出的滤渣主要含有___________ ,它属于_________ (填“酸性”或“碱性”)氧化物。
(3)滤液Y中的阴离子除了含 、
、 外还有
外还有_________ (填离子符号);若步骤(Ⅱ)中加入的NaOH溶液不足量,则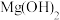 沉淀中混有的杂质是
沉淀中混有的杂质是_________ (填化学式)。
(4)写出步骤(Ⅲ)中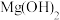 受热分解生成MgO和
受热分解生成MgO和 的化学方程式
的化学方程式_____________ 。
 ,含有少量
,含有少量 、
、 等杂质)设计制备氧化镁的流程如下:
等杂质)设计制备氧化镁的流程如下:
回答下列问题:
(1)步骤(Ⅰ)中分离操作的名称是
(2)步骤(Ⅰ)中分离出的滤渣主要含有
(3)滤液Y中的阴离子除了含
 、
、 外还有
外还有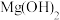 沉淀中混有的杂质是
沉淀中混有的杂质是(4)写出步骤(Ⅲ)中
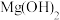 受热分解生成MgO和
受热分解生成MgO和 的化学方程式
的化学方程式
您最近半年使用:0次
2020-11-28更新
|
333次组卷
|
2卷引用:云南省梁河县第一中学2020-2021学年高一下学期期中考试化学试题
解题方法
3 . 用如图方法回收废旧CPU中的单质Au(金),Ag和Cu。

已知:①浓硝酸不能单独将Au溶解。②HAuCl4=H++AuCl 。
。
(1)酸溶后经__ 操作,将混合物分离。
(2)浓、稀HNO3均可作酸溶试剂。溶解等量的Cu消耗HNO3的物质的量不同,写出消耗HNO3物质的量少的反应的化学方程式:__ 。
(3)HNO3—NaCl与王水[V(浓硝酸):V(浓盐酸)=1:3]溶金原理相同,还原产物遇空气变红棕色。
①将溶金反应的化学方程式补充完整:__ 。
Au+______NaCl+______HNO3=HAuCl4+______+______+______NaNO3
②关于溶金的下列说法正确的是__ 。
A.用到了HNO3的氧化性
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO3也可使Au溶解
(4)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如图方法从酸溶后的溶液中回收Cu和Ag(图中标注的试剂和物质均不同)。

试剂1是__ ,试剂2是__ 。

已知:①浓硝酸不能单独将Au溶解。②HAuCl4=H++AuCl
 。
。(1)酸溶后经
(2)浓、稀HNO3均可作酸溶试剂。溶解等量的Cu消耗HNO3的物质的量不同,写出消耗HNO3物质的量少的反应的化学方程式:
(3)HNO3—NaCl与王水[V(浓硝酸):V(浓盐酸)=1:3]溶金原理相同,还原产物遇空气变红棕色。
①将溶金反应的化学方程式补充完整:
Au+______NaCl+______HNO3=HAuCl4+______+______+______NaNO3
②关于溶金的下列说法正确的是
A.用到了HNO3的氧化性
B.王水中浓盐酸的主要作用是增强溶液的酸性
C.用浓盐酸与NaNO3也可使Au溶解
(4)用适当浓度的盐酸、NaCl溶液、氨水与铁粉,可按照如图方法从酸溶后的溶液中回收Cu和Ag(图中标注的试剂和物质均不同)。

试剂1是
您最近半年使用:0次
2021高三·全国·专题练习
解题方法
4 . 高铁酸钾(K2FeO4)具有强氧化性,可作为水处理剂和高容量电池材料。工业上生产高铁酸钾的工艺流程如下:
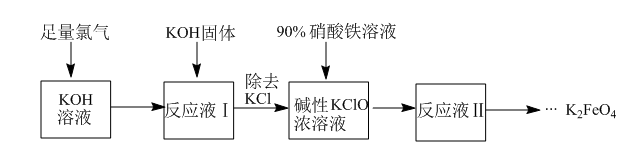
已知K2FeO4具有下列性质:①可溶于水,微溶于KOH溶液,难溶于异丙醇;②在0℃-5℃,强碱性溶液中比较稳定;③在Fe3+和Fe(OH)3催化作用下发生分解;④在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。请完成下列填空:
请补充完整由“反应液Ⅱ”得到K2FeO4晶体的实验步骤。(可选用的试剂:NaOH溶液、KOH溶液、蒸馏水和异丙醇)
① 向反应液Ⅱ中加入饱和___________ ,在冰水浴中静置结晶后过滤,得K2FeO4粗产品;
② 将K2FeO4粗产品溶解在___________ 中,再次在冰水浴中静置结晶后过滤,得到较纯净的K2FeO4;
③ 将K2FeO4晶体再用少量___________ 洗涤,低温真空干燥,得到高铁酸钾成品。

已知K2FeO4具有下列性质:①可溶于水,微溶于KOH溶液,难溶于异丙醇;②在0℃-5℃,强碱性溶液中比较稳定;③在Fe3+和Fe(OH)3催化作用下发生分解;④在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。请完成下列填空:
请补充完整由“反应液Ⅱ”得到K2FeO4晶体的实验步骤。(可选用的试剂:NaOH溶液、KOH溶液、蒸馏水和异丙醇)
① 向反应液Ⅱ中加入饱和
② 将K2FeO4粗产品溶解在
③ 将K2FeO4晶体再用少量
您最近半年使用:0次
5 . 硫代硫酸钠晶体( )不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分
)不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分 ,含少量
,含少量 )及纯碱等为原料制备
)及纯碱等为原料制备 的流程如下:
的流程如下:

下列说法正确的是
 )不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分
)不溶于乙醇,可用作纸浆漂白时的脱氯剂等。用工业硫化钠(主要成分 ,含少量
,含少量 )及纯碱等为原料制备
)及纯碱等为原料制备 的流程如下:
的流程如下:
下列说法正确的是
A. 作脱氯剂时主要利用其氧化性 作脱氯剂时主要利用其氧化性 |
B.“净化”时加入的试剂X可选用 溶液 溶液 |
| C.“反应”过程中体系pH大小对产品产率无影响 |
D.提纯 时,应先用水洗,再用乙醇洗涤 时,应先用水洗,再用乙醇洗涤 |
您最近半年使用:0次
2021-12-30更新
|
770次组卷
|
5卷引用:辽宁省名校2021-2022学年高三上学期第五次联合考试化学试题
辽宁省名校2021-2022学年高三上学期第五次联合考试化学试题(已下线)查补易混易错点08 化学实验基础-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)查补易混易错点08 化学实验基础-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)微专题22 新型含硫化合物的制备与性质探究(Na2S2O3 Na2S2O4 Na2S4O6 )-备战2023年高考化学一轮复习考点微专题(已下线)仿真卷05-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)
解题方法
6 . 过氧化钙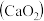 是一种用途广泛的优良供氧剂,常温下为白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备
是一种用途广泛的优良供氧剂,常温下为白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备 过程如下。
过程如下。
Ⅰ.制备
利用反应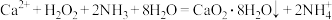 ,在碱性环境下制取
,在碱性环境下制取 的装置如图:
的装置如图:
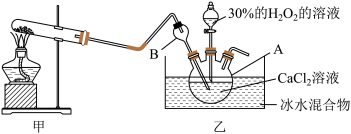
(1) 的电子式为
的电子式为_______ 。
(2)写出甲装置中反应的化学方程式_______ 。
(3)仪器A的名称为_______ ;仪器B的作用是_______ 。
(4)乙中反应温度需控制在0℃左右的原因是该反应是放热反应,温度低有利于提高 的产率和
的产率和_______ 。
(5)反应结束后,分离提纯 的过程中,洗涤的操作为
的过程中,洗涤的操作为_______ 。
Ⅱ.制得产品并定量检测
(6) 脱水干燥即得
脱水干燥即得 产品。经检测知某
产品。经检测知某 产品中含有
产品中含有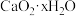 和
和 ,已知
,已知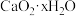 受热分解有
受热分解有 、
、 和
和 生成。①称取
生成。①称取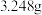 产品,加热,在标准状况下生成
产品,加热,在标准状况下生成 气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的
气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的 溶液得到沉淀
溶液得到沉淀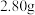 ,则该产品中
,则该产品中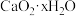 的x值为
的x值为_______ 。
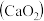 是一种用途广泛的优良供氧剂,常温下为白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备
是一种用途广泛的优良供氧剂,常温下为白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备 过程如下。
过程如下。Ⅰ.制备

利用反应
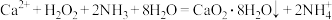 ,在碱性环境下制取
,在碱性环境下制取 的装置如图:
的装置如图:
(1)
 的电子式为
的电子式为(2)写出甲装置中反应的化学方程式
(3)仪器A的名称为
(4)乙中反应温度需控制在0℃左右的原因是该反应是放热反应,温度低有利于提高
 的产率和
的产率和(5)反应结束后,分离提纯
 的过程中,洗涤的操作为
的过程中,洗涤的操作为Ⅱ.制得产品并定量检测
(6)
 脱水干燥即得
脱水干燥即得 产品。经检测知某
产品。经检测知某 产品中含有
产品中含有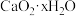 和
和 ,已知
,已知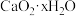 受热分解有
受热分解有 、
、 和
和 生成。①称取
生成。①称取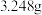 产品,加热,在标准状况下生成
产品,加热,在标准状况下生成 气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的
气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的 溶液得到沉淀
溶液得到沉淀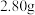 ,则该产品中
,则该产品中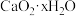 的x值为
的x值为
您最近半年使用:0次
名校
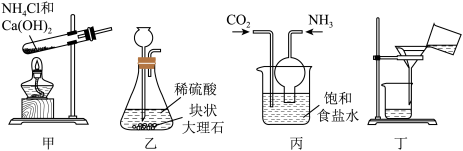
7 . 硝酸是一种具有强氧化性、腐蚀性的强酸。硝酸工业与合成氨工业紧密相关,氨氧化法是工业生产中制取硝酸的主要途径,其主要流程是将氨和空气的混合气通入灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮(NO)。生成的一氧化氮利用反应后残余的氧气继续氧化为二氧化氮,随后将二氧化氮通入水中制取硝酸。4NH3+5O2 4NO+6H2O、2NO+O2=2NO2、3NO2+H2O=2HNO3+NO。已知侯氏制碱的主要反应原理:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl,利用下列装置制取碳酸氢钠粗品,实验装置正确且能达到实验目的的是
4NO+6H2O、2NO+O2=2NO2、3NO2+H2O=2HNO3+NO。已知侯氏制碱的主要反应原理:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl,利用下列装置制取碳酸氢钠粗品,实验装置正确且能达到实验目的的是
 4NO+6H2O、2NO+O2=2NO2、3NO2+H2O=2HNO3+NO。已知侯氏制碱的主要反应原理:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl,利用下列装置制取碳酸氢钠粗品,实验装置正确且能达到实验目的的是
4NO+6H2O、2NO+O2=2NO2、3NO2+H2O=2HNO3+NO。已知侯氏制碱的主要反应原理:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl,利用下列装置制取碳酸氢钠粗品,实验装置正确且能达到实验目的的是
| A.用装置甲制取氨气 | B.用装置乙制取二氧化碳 |
| C.用装置丙制取碳酸氢钠 | D.用装置丁分离碳酸氢钠与母液 |
您最近半年使用:0次
20-21高二下·浙江·阶段练习
解题方法
8 . 下列说法不正确的是
| A.在K2Cr2O7酸性溶液中加入NaOH溶液,溶液由橙色变为黄色;若将NaOH溶液改成NaNO2溶液,则溶液变成绿色 |
| B.将火柴头直接浸入水中,加入硝酸银溶液和稀硝酸,通过观察是否产生白色沉淀来检验其中是否含有氯元素 |
| C.制备硫酸亚铁铵晶体时,可用少量酒精对晶体进行洗涤,除去附着在晶体表面的水 |
| D.为增强高锰酸钾的氧化性常对其进行酸化,酸化时常使用稀硫酸而不采用盐酸 |
您最近半年使用:0次
名校
9 . 废旧材料是巨大的资源宝库,回收利用前景广阔。从废黄铜合金(主要成分为Cu和Zn)中回收Cu并制备ZnO的部分实验流程如下图所示。下列叙述错误的是
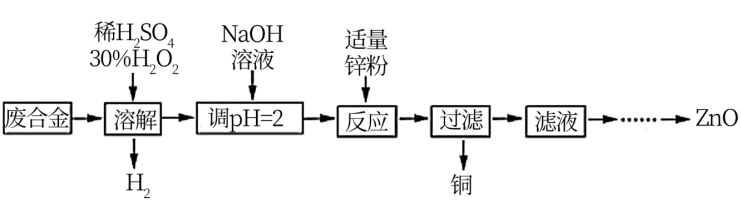

A.“溶解”过程中, 和稀硫酸都体现了氧化性 和稀硫酸都体现了氧化性 |
B.与锌粉反应的离子主要是 和 和 |
| C.过滤需要用到的玻璃仪器有烧杯、漏斗和玻璃棒 |
| D.为加快溶解速率可以选择高温、搅拌 |
您最近半年使用:0次
2021-04-23更新
|
417次组卷
|
6卷引用:江苏省百校联考2021届高三第三次考试化学试题
江苏省百校联考2021届高三第三次考试化学试题(已下线)押山东卷第08题 化学实验常用仪器和基本操作-备战2021年高考化学临考题号押题(山东卷)吉林省松原市前郭尔罗斯蒙古族自治县第五中学2021届高三下学期5月月考化学试题(已下线)考点31 化学实验与工艺流程-备战2022年高考化学一轮复习考点帮(浙江专用)湖南省岳阳市汨罗市第二中学2022届高三下学期期中考试化学试题上海市宝山区吴淞中学2021-2022学年高三下学期 3月第一次学科调研化学试题
10 . 用下列实验装置进行相应实验,设计正确且能达到实验目的的是


| A.用甲装置除去苯中的苯酚杂质 |
| B.用乙装置验证硫酸、碳酸、苯酚的酸性强弱 |
| C.用丙装置制备并检验乙炔的性质 |
| D.用丁装置分离乙醇和乙酸的混合物 |
您最近半年使用:0次
2021-07-22更新
|
240次组卷
|
3卷引用:辽宁省锦州市2020-2021学年高二下学期期末考试化学试题



