解题方法
1 . 某种常见补铁药物的主要成分为琥珀酸亚铁。该药品不溶于水但能溶于常见稀酸。某学习小组同学分别设计实验检验药片中Fe2+的存在并测定Fe2+的含量(假设杂质不参与反应)。回答下列问题:
(1)甲同学为了检验药品中的Fe2+ ,将药物碾碎、水溶后过滤。取少量所得滤液于两支试管中,分别加入K3[Fe(CN)6]溶液和KSCN溶液,观察并记录实验现象。
①甲同学过滤时的下列操作规范的是_______ (填编号)。
a.用玻璃棒引流
b.漏斗口未紧靠烧杯内壁
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高于漏斗边缘
e.用玻璃棒在漏斗中搅动以加快过滤速度
②滤液加入K3[Fe(CN)6]溶液或KSCN溶液均未出现明显现象,其主要原因为_______ 。
(2)乙同学设计如下实验测定药片中Fe2+的含量。
步骤一:取本品10片,碾碎后加入一定浓度试剂a,在适当的条件下配成100mL溶液。
步骤二:准确量取20.00mL步骤一所得溶液放入烧杯中。
步骤三:向烧杯中加入过量H2O2溶液,后加入过量NaOH溶液生成沉淀,将沉淀过滤、洗涤、干燥后灼烧至固体质量恒定,得0. 64g固体。
①步骤一中加入的试剂a为_______ 。
②步骤三中,加入H2O2溶液发生反应的离子方程式为_______ ,灼烧后 所得固体的颜色为 _______ ,灼烧时需要使用下列仪器中的 _______ (填编号)。
a.酒精灯 b.坩埚 c.蒸发皿 d.铁架台(带铁圈) e.三脚架
③若将步骤三中的H2O2 溶液换为Cl2也能达到目的,但使用H2O2溶液的好处是_______ 。
④由实验数据计算,每片药片中约含Fe2+_______ mg。
(3)医生建议该药品与维生素C同时服用以增强补铁效果,原因是利用了维生素C的_______ (选填“氧化性”、“ 还原性”或“碱性”。)
(1)甲同学为了检验药品中的Fe2+ ,将药物碾碎、水溶后过滤。取少量所得滤液于两支试管中,分别加入K3[Fe(CN)6]溶液和KSCN溶液,观察并记录实验现象。
①甲同学过滤时的下列操作规范的是
a.用玻璃棒引流
b.漏斗口未紧靠烧杯内壁
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高于漏斗边缘
e.用玻璃棒在漏斗中搅动以加快过滤速度
②滤液加入K3[Fe(CN)6]溶液或KSCN溶液均未出现明显现象,其主要原因为
(2)乙同学设计如下实验测定药片中Fe2+的含量。
步骤一:取本品10片,碾碎后加入一定浓度试剂a,在适当的条件下配成100mL溶液。
步骤二:准确量取20.00mL步骤一所得溶液放入烧杯中。
步骤三:向烧杯中加入过量H2O2溶液,后加入过量NaOH溶液生成沉淀,将沉淀过滤、洗涤、干燥后灼烧至固体质量恒定,得0. 64g固体。
①步骤一中加入的试剂a为
②步骤三中,加入H2O2溶液发生反应的离子方程式为
a.酒精灯 b.坩埚 c.蒸发皿 d.铁架台(带铁圈) e.三脚架
③若将步骤三中的H2O2 溶液换为Cl2也能达到目的,但使用H2O2溶液的好处是
④由实验数据计算,每片药片中约含Fe2+
(3)医生建议该药品与维生素C同时服用以增强补铁效果,原因是利用了维生素C的
您最近半年使用:0次
名校
2 . 硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]在工业上常用作分析试剂,它可用含SiO2、CeO2和Fe2O3的工业废料作原料来获得,同时可回收CeO2,工艺流程设计如下:
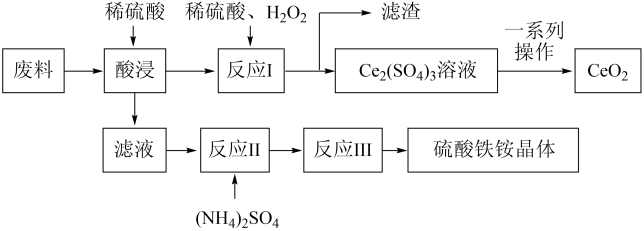
已知:①SiO2、CeO2不溶于稀硫酸;
②酸性条件下,CeO2可与H2O2反应;
③“反应I”所得溶液中含有Ce3+;
④碱性条件下, 与OH-结合生成NH3·H2O。
与OH-结合生成NH3·H2O。
请回答下列问题:
(1)“酸浸”时发生反应的离子方程式为______ 未发生反应的物质是_______ (填化学式)。
(2)“滤液”中含有的阳离子有______ (填离子符号)。
(3)写出“反应I”的化学方程式:____ ;“反应I”后进行固液分离时用到的玻璃仪器有______ 。
(4)在酸性条件下,H2O2、CeO2两种物质中,氧化性较弱的是_______ (填化学式)。
(5)若往硫酸铁铵溶液中加入过量的NaOH,写出该反应的离子方程式:______ 。

已知:①SiO2、CeO2不溶于稀硫酸;
②酸性条件下,CeO2可与H2O2反应;
③“反应I”所得溶液中含有Ce3+;
④碱性条件下,
 与OH-结合生成NH3·H2O。
与OH-结合生成NH3·H2O。请回答下列问题:
(1)“酸浸”时发生反应的离子方程式为
(2)“滤液”中含有的阳离子有
(3)写出“反应I”的化学方程式:
(4)在酸性条件下,H2O2、CeO2两种物质中,氧化性较弱的是
(5)若往硫酸铁铵溶液中加入过量的NaOH,写出该反应的离子方程式:
您最近半年使用:0次
名校
解题方法
3 . 高铁酸钾(K2FeO4)是一种新型净水剂,制备流程如下:
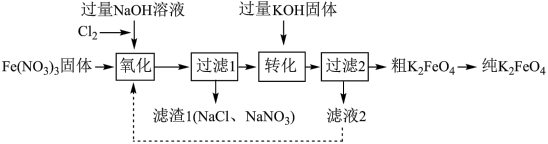
资料:Ⅰ.K2FeO4可溶于水,微溶于KOH溶液,难溶于乙醇。KOH易溶于乙醇。
Ⅱ. 在碱性溶液中稳定,中性和酸性溶液中不稳定。
在碱性溶液中稳定,中性和酸性溶液中不稳定。
(1)K2FeO4具有强氧化性,其中铁元素的化合价为___________ 价。
(2)Cl2与NaOH溶液反应的离子方程式是___________ 。
(3)补全“氧化”中反应的离子方程式:_________
ClO− + Fe3+ + ___________ =  + ___________ + ___________
+ ___________ + ___________
(4)下列说法正确的是___________ 。
a.“氧化”中NaOH溶液过量的目的是使 稳定存在
稳定存在
b.“转化”中生成K2FeO4固体
c.设计物质循环的目的是提高原料的利用率
(5)粗K2FeO4转化为纯K2FeO4的操作包含洗涤,去除固体表面的KOH,可以用___________ 洗涤。

资料:Ⅰ.K2FeO4可溶于水,微溶于KOH溶液,难溶于乙醇。KOH易溶于乙醇。
Ⅱ.
 在碱性溶液中稳定,中性和酸性溶液中不稳定。
在碱性溶液中稳定,中性和酸性溶液中不稳定。(1)K2FeO4具有强氧化性,其中铁元素的化合价为
(2)Cl2与NaOH溶液反应的离子方程式是
(3)补全“氧化”中反应的离子方程式:
ClO− + Fe3+ + ___________ =
 + ___________ + ___________
+ ___________ + ___________(4)下列说法正确的是
a.“氧化”中NaOH溶液过量的目的是使
 稳定存在
稳定存在b.“转化”中生成K2FeO4固体
c.设计物质循环的目的是提高原料的利用率
(5)粗K2FeO4转化为纯K2FeO4的操作包含洗涤,去除固体表面的KOH,可以用
您最近半年使用:0次
2023-09-30更新
|
46次组卷
|
2卷引用:北京市第七中学2022-2023学年高一上学期期中考试化学试题
4 . SO2是有毒气体,任意排放会造成环境污染。若加以利用,可以变废为宝。下图为SO2的无害化处理流程图,回答下列问题:
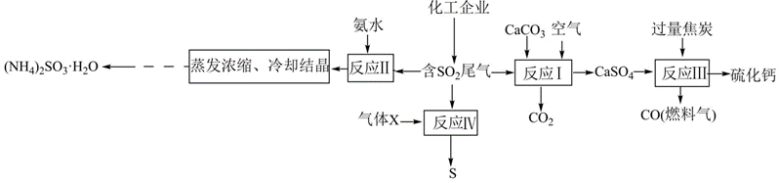
(1)“反应I”在高温条件下进行,写出该反应的化学方程式:___________ 。
(2)X可能为___________ (填化学式),电子式为___________ ,该反应说明SO2具有___________ (填“氧化性”或“还原性”)。
(3)“蒸发浓缩、冷却结晶”后获得 固体的操作是
固体的操作是___________ 。
(4) 暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:
暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:________ 。
A.稀硝酸,BaCl2 B.稀盐酸,BaCl2 C.稀盐酸,硝酸钡

(1)“反应I”在高温条件下进行,写出该反应的化学方程式:
(2)X可能为
(3)“蒸发浓缩、冷却结晶”后获得
 固体的操作是
固体的操作是(4)
 暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:
暴露在空气中易被氧化而变质,可以选用哪组试剂进行验证:A.稀硝酸,BaCl2 B.稀盐酸,BaCl2 C.稀盐酸,硝酸钡
您最近半年使用:0次
5 . 高纯 是广泛用于电子行业的强磁性材料.
是广泛用于电子行业的强磁性材料. 为白色粉末,不溶于水和乙醇,在潮湿环境下易被氧化,温度高于
为白色粉末,不溶于水和乙醇,在潮湿环境下易被氧化,温度高于 开始分解。
开始分解。
Ⅰ 实验室以
实验室以 为原料制备
为原料制备
 制备
制备 溶液:
溶液:
 主要反应装置如图1,缓缓通入经
主要反应装置如图1,缓缓通入经 稀释的
稀释的 气体,发生反应
气体,发生反应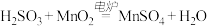 ,下列措施中,目的是加快化学反应速率的是
,下列措施中,目的是加快化学反应速率的是______  填标号
填标号 。
。
A. 加入前先研磨
加入前先研磨  搅拌
搅拌  提高混合气中
提高混合气中 比例
比例
 已知实验室制取
已知实验室制取 的原理是
的原理是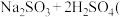 浓
浓

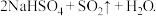 选择如图2所示部分装置与图装1置相连制备
选择如图2所示部分装置与图装1置相连制备 溶液,应选择的装置有
溶液,应选择的装置有______  填标号
填标号 .
.

 若用空气代替
若用空气代替 进行实验,缺点是
进行实验,缺点是______  酸性环境下
酸性环境下 不易被氧化
不易被氧化
 制备
制备 固体:
固体:
实验步骤: 向
向 溶液中边搅拌边加入饱和
溶液中边搅拌边加入饱和 溶液生成
溶液生成 沉淀,反应结束后过滤;
沉淀,反应结束后过滤; ;
; 在
在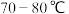 下烘干得到纯净干燥的
下烘干得到纯净干燥的 固体。
固体。
步骤 需要用到的试剂有
需要用到的试剂有______ 。
Ⅱ 设计实验方案
设计实验方案
 利用沉淀转化的方法证明
利用沉淀转化的方法证明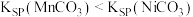 :
:______ 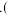 已知
已知 为难溶于水的浅绿色固体
为难溶于水的浅绿色固体
 证明
证明 的第二步电离不完全:
的第二步电离不完全:______ 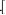 查阅资料表明
查阅资料表明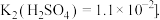
 是广泛用于电子行业的强磁性材料.
是广泛用于电子行业的强磁性材料. 为白色粉末,不溶于水和乙醇,在潮湿环境下易被氧化,温度高于
为白色粉末,不溶于水和乙醇,在潮湿环境下易被氧化,温度高于 开始分解。
开始分解。Ⅰ
 实验室以
实验室以 为原料制备
为原料制备
 制备
制备 溶液:
溶液: 主要反应装置如图1,缓缓通入经
主要反应装置如图1,缓缓通入经 稀释的
稀释的 气体,发生反应
气体,发生反应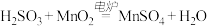 ,下列措施中,目的是加快化学反应速率的是
,下列措施中,目的是加快化学反应速率的是 填标号
填标号 。
。A.
 加入前先研磨
加入前先研磨  搅拌
搅拌  提高混合气中
提高混合气中 比例
比例 已知实验室制取
已知实验室制取 的原理是
的原理是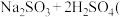 浓
浓

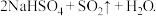 选择如图2所示部分装置与图装1置相连制备
选择如图2所示部分装置与图装1置相连制备 溶液,应选择的装置有
溶液,应选择的装置有 填标号
填标号 .
.

 若用空气代替
若用空气代替 进行实验,缺点是
进行实验,缺点是 酸性环境下
酸性环境下 不易被氧化
不易被氧化
 制备
制备 固体:
固体:实验步骤:
 向
向 溶液中边搅拌边加入饱和
溶液中边搅拌边加入饱和 溶液生成
溶液生成 沉淀,反应结束后过滤;
沉淀,反应结束后过滤; ;
; 在
在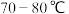 下烘干得到纯净干燥的
下烘干得到纯净干燥的 固体。
固体。步骤
 需要用到的试剂有
需要用到的试剂有Ⅱ
 设计实验方案
设计实验方案 利用沉淀转化的方法证明
利用沉淀转化的方法证明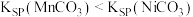 :
: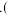 已知
已知 为难溶于水的浅绿色固体
为难溶于水的浅绿色固体
 证明
证明 的第二步电离不完全:
的第二步电离不完全: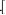 查阅资料表明
查阅资料表明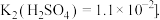
您最近半年使用:0次
6 . 化学源于生活,她与我们生活息息相关。
Ⅰ.我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已略去)。
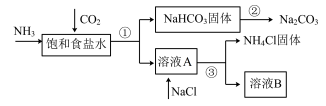
(1)①~③所涉及的操作方法中,包含过滤的是_______ (填序号)。
(2)根据上图,将化学方程式补充完整:
_______ 
_______ 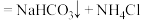
(3)煅烧 固体的化学方程式是
固体的化学方程式是_______ 。
(4)关于上述过程,下列说法中正确的是_______ (填字母)。
a. 不可循环使用
不可循环使用
b.副产物 可用作肥料
可用作肥料
c.反应过程中应先通入极易溶于水的 ,使溶液显碱性,然后再通入
,使溶液显碱性,然后再通入 气体
气体
Ⅱ.氧化还原反应是一类重要的化学反应,广泛应用于生产和生活中。
(5)氢化钠( )在野外被用作生氢剂,其原理是
)在野外被用作生氢剂,其原理是 ,该反应中氧化剂是
,该反应中氧化剂是_______ ,还原剂是_______ ;被氧化与被还原元素的物质的量之比为:_______ 。
(6)某离子反应中涉及 、
、 、
、 、
、 、
、 、
、 六种微粒。其中
六种微粒。其中 、
、 的物质的量随时间变化的曲线如图所示。下列判断不正确的是
的物质的量随时间变化的曲线如图所示。下列判断不正确的是_______ 。
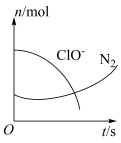
a.该反应的氧化剂是
b.消耗 还原剂,转移
还原剂,转移 电子
电子
c.氧化剂与还原剂的物质的量之比为
d.当生成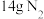 时,消耗的
时,消耗的 为
为
e.氧化性: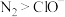
(7)高铁酸钠( ),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。高铁酸钠(
),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。高铁酸钠( )中铁元素的价态为
)中铁元素的价态为_______ ;写出制备高铁酸钠的离子方程式_______ 。
Ⅰ.我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已略去)。

(1)①~③所涉及的操作方法中,包含过滤的是
(2)根据上图,将化学方程式补充完整:


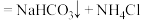
(3)煅烧
 固体的化学方程式是
固体的化学方程式是(4)关于上述过程,下列说法中正确的是
a.
 不可循环使用
不可循环使用b.副产物
 可用作肥料
可用作肥料c.反应过程中应先通入极易溶于水的
 ,使溶液显碱性,然后再通入
,使溶液显碱性,然后再通入 气体
气体Ⅱ.氧化还原反应是一类重要的化学反应,广泛应用于生产和生活中。
(5)氢化钠(
 )在野外被用作生氢剂,其原理是
)在野外被用作生氢剂,其原理是 ,该反应中氧化剂是
,该反应中氧化剂是(6)某离子反应中涉及
 、
、 、
、 、
、 、
、 、
、 六种微粒。其中
六种微粒。其中 、
、 的物质的量随时间变化的曲线如图所示。下列判断不正确的是
的物质的量随时间变化的曲线如图所示。下列判断不正确的是
a.该反应的氧化剂是

b.消耗
 还原剂,转移
还原剂,转移 电子
电子c.氧化剂与还原剂的物质的量之比为

d.当生成
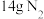 时,消耗的
时,消耗的 为
为
e.氧化性:
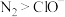
(7)高铁酸钠(
 ),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。高铁酸钠(
),易溶于水,是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。在次氯酸钠溶液中加入氢氧化钠和硫酸铁可制备高铁酸钠,此法被称为次氯酸盐氧化法。高铁酸钠( )中铁元素的价态为
)中铁元素的价态为
您最近半年使用:0次
7 . 从海水中提取食盐和溴的过程如下:

(1)海水日晒得到的盐因为含有较多杂质,称为粗盐。为了得到精制盐,可以用_______ 的办法除去其中的泥沙等不溶物。
(2)①步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为_______ 。
(3)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的_______。
(4)步骤Ⅱ用纯碱溶液吸收Br2,反应生成了NaBrO3、NaBr、CO2,则该反应的化学方程式为____
(5)下图是实验室传统蒸馏装置,回答下列问题。
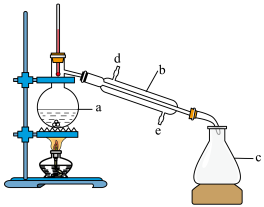
指出图中a、b、c三种仪器的名称:a_______ 、b_______ 、c_______ ;实验中在a仪器中应加入几片碎瓷片,其作用是_______ ;冷却水从_______ 端进入。

(1)海水日晒得到的盐因为含有较多杂质,称为粗盐。为了得到精制盐,可以用
(2)①步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为
(3)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的_______。
| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
(5)下图是实验室传统蒸馏装置,回答下列问题。

指出图中a、b、c三种仪器的名称:a
您最近半年使用:0次
解题方法
8 . 碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。请回答下列问题:
(1)海带中含有丰富的碘,将海带灼烧、浸泡、过滤,所得的滤液中含有丰富的碘离子。在实验室中进行过滤操作时,需要用到的玻璃仪器为___________ 。
(2) 的化学性质与卤素单质类似,
的化学性质与卤素单质类似, 也具有强氧化性,
也具有强氧化性, 可与氢硫酸(
可与氢硫酸( 的水溶液)反应生成淡黄色沉淀和两种强酸,试写出
的水溶液)反应生成淡黄色沉淀和两种强酸,试写出 和氢硫酸反应的化学方程式:
和氢硫酸反应的化学方程式:___________ 。 和
和 溶液反应生成
溶液反应生成 和
和 ,该反应
,该反应___________ 氧化还原反应(填“是”或“不是”)。
(3)加碘食盐中加入的是 。请回答下列问题:
。请回答下列问题:
①在 溶液中滴加少量
溶液中滴加少量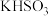 溶液,发生如下反应,请配平并写出该反应方程式
溶液,发生如下反应,请配平并写出该反应方程式___________ 。

②在 溶液中滴加过量
溶液中滴加过量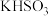 溶液,反应完全,推测反应后溶液中的还原产物为
溶液,反应完全,推测反应后溶液中的还原产物为___________ (填化学式)。(已知:还原性: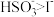 ;氧化性:
;氧化性: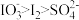 。)
。)
(1)海带中含有丰富的碘,将海带灼烧、浸泡、过滤,所得的滤液中含有丰富的碘离子。在实验室中进行过滤操作时,需要用到的玻璃仪器为
(2)
 的化学性质与卤素单质类似,
的化学性质与卤素单质类似, 也具有强氧化性,
也具有强氧化性, 可与氢硫酸(
可与氢硫酸( 的水溶液)反应生成淡黄色沉淀和两种强酸,试写出
的水溶液)反应生成淡黄色沉淀和两种强酸,试写出 和氢硫酸反应的化学方程式:
和氢硫酸反应的化学方程式: 和
和 溶液反应生成
溶液反应生成 和
和 ,该反应
,该反应(3)加碘食盐中加入的是
 。请回答下列问题:
。请回答下列问题:①在
 溶液中滴加少量
溶液中滴加少量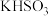 溶液,发生如下反应,请配平并写出该反应方程式
溶液,发生如下反应,请配平并写出该反应方程式
②在
 溶液中滴加过量
溶液中滴加过量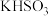 溶液,反应完全,推测反应后溶液中的还原产物为
溶液,反应完全,推测反应后溶液中的还原产物为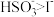 ;氧化性:
;氧化性: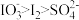 。)
。)
您最近半年使用:0次
9 . 氧化镁是优质的耐高温材料。某兴趣小组利用菱镁矿(主要成分为 ,含有少量
,含有少量 、
、 等杂质)设计制备氧化镁的流程如下:
等杂质)设计制备氧化镁的流程如下:
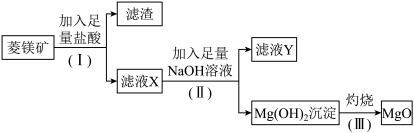
回答下列问题:
(1)步骤(Ⅰ)中分离操作的名称是_________ ,所使用的玻璃仪器有__________ 烧杯、玻璃棒。
(2)步骤(Ⅰ)中分离出的滤渣主要含有___________ ,它属于_________ (填“酸性”或“碱性”)氧化物。
(3)滤液Y中的阴离子除了含 、
、 外还有
外还有_________ (填离子符号);若步骤(Ⅱ)中加入的NaOH溶液不足量,则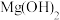 沉淀中混有的杂质是
沉淀中混有的杂质是_________ (填化学式)。
(4)写出步骤(Ⅲ)中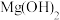 受热分解生成MgO和
受热分解生成MgO和 的化学方程式
的化学方程式_____________ 。
 ,含有少量
,含有少量 、
、 等杂质)设计制备氧化镁的流程如下:
等杂质)设计制备氧化镁的流程如下:
回答下列问题:
(1)步骤(Ⅰ)中分离操作的名称是
(2)步骤(Ⅰ)中分离出的滤渣主要含有
(3)滤液Y中的阴离子除了含
 、
、 外还有
外还有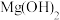 沉淀中混有的杂质是
沉淀中混有的杂质是(4)写出步骤(Ⅲ)中
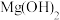 受热分解生成MgO和
受热分解生成MgO和 的化学方程式
的化学方程式
您最近半年使用:0次
2020-11-28更新
|
333次组卷
|
2卷引用:云南省2020年9月普通高中学业水平考试化学试卷
10 . 以银锰精矿(主要含Ag2S、MnS、FeS2)和氧化锰矿(主要含MnO2)为原料联合提取精银、Mn及MnO2的一种流程示意图如下。

已知:酸性条件下,MnO2的氧化性强于Fe3+。
(1)“浸锰”是在H2SO4溶液中使矿石中的锰元素浸出的过程,能同时去除FeS2,且有利于后续银的浸出,矿石中的银以Ag2S的形式残留于浸锰渣中。
①“浸锰”过程中,MnS发生反应的离子方程式是_______ 。
②在H2SO4溶液中,银锰精矿中的FeS2和氧化锰矿中的MnO2发生反应,则浸锰液中主要的金属阳离子有_______ 。
(2)“浸银”时,使用过量FeCl3、HCl、CaCl2的混合液作为浸出剂,将Ag2S中的银以 形式浸出。
形式浸出。
①将“浸银”反应的离子方程式补充完整:_______ 。
_______Fe3++Ag2S+_______⇌_______+_______[AgCl2]-+S
②浸出剂中H+的作用:_______ 。
(3)“电解精炼”时,将粗银粉进行“固态化”处理,制成“粗银电极”,下图为电解精炼银的示意图,回答下列问题:
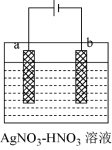
①_______ 极为“粗银电极”(填“a”或“b”)。
②若b极有少量红棕色气体产生,则生成该气体的电极反应式为_______ ;当电路中通过0.025NA电子时,b极质量增加2.16g,则b极产生的气体在标况下的体积为_______ mL(保留三位有效数字)。

已知:酸性条件下,MnO2的氧化性强于Fe3+。
(1)“浸锰”是在H2SO4溶液中使矿石中的锰元素浸出的过程,能同时去除FeS2,且有利于后续银的浸出,矿石中的银以Ag2S的形式残留于浸锰渣中。
①“浸锰”过程中,MnS发生反应的离子方程式是
②在H2SO4溶液中,银锰精矿中的FeS2和氧化锰矿中的MnO2发生反应,则浸锰液中主要的金属阳离子有
(2)“浸银”时,使用过量FeCl3、HCl、CaCl2的混合液作为浸出剂,将Ag2S中的银以
 形式浸出。
形式浸出。①将“浸银”反应的离子方程式补充完整:
_______Fe3++Ag2S+_______⇌_______+_______[AgCl2]-+S
②浸出剂中H+的作用:
(3)“电解精炼”时,将粗银粉进行“固态化”处理,制成“粗银电极”,下图为电解精炼银的示意图,回答下列问题:

①
②若b极有少量红棕色气体产生,则生成该气体的电极反应式为
您最近半年使用:0次



