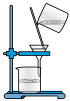
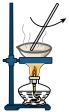
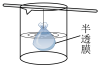
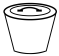
1 . 历经十年传承积淀,形成精湛的东阿阿胶传统工艺,包括洗皮、泡皮、晾皮、刮毛、铡皮、化皮、打沫、除渣、浓缩、挂旗、凝胶、切胶等工序。下列工序与化学实验中的原理不具有对应关系的是
| 选项 | A | B | C | D |
| 工序 |
|
|
|
|
| 化学实验 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 下列图示与操作名称对应关系错误的是
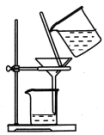 |  |  | 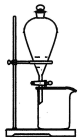 |
| A.过滤 | B.蒸馏 | C.分馏 | D.分液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-05-19更新
|
310次组卷
|
3卷引用:湖北省武汉市武昌区2022届高三5月质量检测化学试题
解题方法
3 . 下列图示与操作名称对应关系错误的是
A.过滤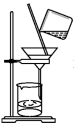 | B.蒸馏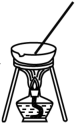 | C.分馏 | D.分液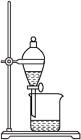 |
您最近半年使用:0次
4 . 为了实现中国人自己研制 的梦想,揭开索尔维法生产的秘密,打破洋人的封锁,侯德榜把全部身心都投入到研究和改进
的梦想,揭开索尔维法生产的秘密,打破洋人的封锁,侯德榜把全部身心都投入到研究和改进 生产工艺上,经过5年艰苦的摸索,终于在1926年生产出合格的
生产工艺上,经过5年艰苦的摸索,终于在1926年生产出合格的 产品。其生产工艺流程如图所示:
产品。其生产工艺流程如图所示:

已知制备中涉及化学方程式如下:
I.
II.
III.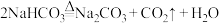
回答下列问题:
(1) 俗称
俗称___________ ,其水溶液的
___________ (填“ ”“
”“ ”或“
”或“ ”)7。
”)7。
(2)反应I需要通入 ,下列可用于实验室制备
,下列可用于实验室制备 的装置是
的装置是___________ (填字母,下同),收集 的装置是
的装置是___________ 。
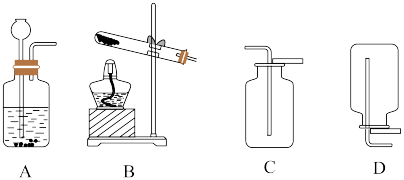
(3)反应III表现出 的化学性质是
的化学性质是___________ 。
(4)“操作”的名称是___________ ,该操作在实验室中必须用到的玻璃仪器有玻璃棒、___________ 。
(5)写出滤液中溶质的一种用途:___________ 。
(6)为了检验某含有 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将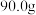 样品充分加热,固体质量变为
样品充分加热,固体质量变为 ,则该样品的纯度(质量分数)约为
,则该样品的纯度(质量分数)约为___________ (保留一位小数)。
 的梦想,揭开索尔维法生产的秘密,打破洋人的封锁,侯德榜把全部身心都投入到研究和改进
的梦想,揭开索尔维法生产的秘密,打破洋人的封锁,侯德榜把全部身心都投入到研究和改进 生产工艺上,经过5年艰苦的摸索,终于在1926年生产出合格的
生产工艺上,经过5年艰苦的摸索,终于在1926年生产出合格的 产品。其生产工艺流程如图所示:
产品。其生产工艺流程如图所示:
已知制备中涉及化学方程式如下:
I.

II.

III.
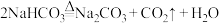
回答下列问题:
(1)
 俗称
俗称
 ”“
”“ ”或“
”或“ ”)7。
”)7。(2)反应I需要通入
 ,下列可用于实验室制备
,下列可用于实验室制备 的装置是
的装置是 的装置是
的装置是
(3)反应III表现出
 的化学性质是
的化学性质是(4)“操作”的名称是
(5)写出滤液中溶质的一种用途:
(6)为了检验某含有
 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将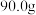 样品充分加热,固体质量变为
样品充分加热,固体质量变为 ,则该样品的纯度(质量分数)约为
,则该样品的纯度(质量分数)约为
您最近半年使用:0次
解题方法
5 . 钴及其化合物在化工生产中有重要的用途。三氯化六氨合钴(Ⅲ) 是制备其它三价钴配合物的重要试剂。实验室用活性炭作催化剂,
是制备其它三价钴配合物的重要试剂。实验室用活性炭作催化剂, 为主要原料合成
为主要原料合成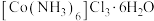 。反应原理为:
。反应原理为: 。该过程的流程如图:
。该过程的流程如图:
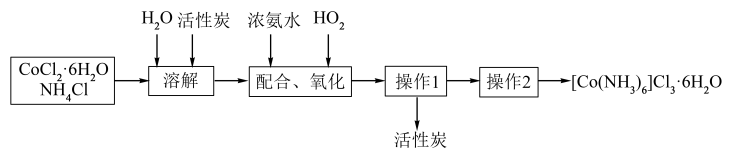
已知:① 不易被氧化,
不易被氧化, 具有较强还原性。
具有较强还原性。
②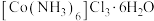 难溶于无水乙醇,在水中的溶解度随温度升高而增大。
难溶于无水乙醇,在水中的溶解度随温度升高而增大。
③加入浓盐酸有利于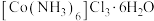 晶体析出。
晶体析出。
回答下列问题:
(1)溶解 时加入的
时加入的 有利于后续
有利于后续 与
与 的配合反应,还能抑制
的配合反应,还能抑制 的水解。写出
的水解。写出 水解的离子方程式
水解的离子方程式__________ 。
(2)发生“配合、氧化”的步骤在如下实验装置中进行。
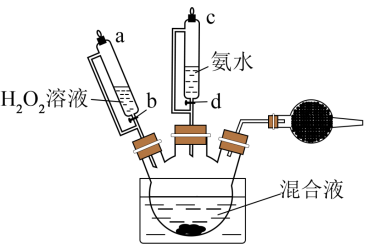
①盛放混合液仪器的名称_______ 。
②干燥管盛放的药品可以是_______ 。
a.浓硫酸 b.五氧化二磷 c.碱石灰
③向混合溶液中首先滴加_______ (填入“ 溶液”或“浓氨水”),完成该步骤的具体操作是
溶液”或“浓氨水”),完成该步骤的具体操作是_______ 。
④“配合、氧化”过程中,控制混合液温度不高于 的原因
的原因__________ 。
(3)“操作1”的名称_______ ;“操作2”的步骤是向滤液滴加少量_________ ,冷却结晶后过滤,用________ 洗涤晶体 次,低温干燥。
次,低温干燥。
 是制备其它三价钴配合物的重要试剂。实验室用活性炭作催化剂,
是制备其它三价钴配合物的重要试剂。实验室用活性炭作催化剂, 为主要原料合成
为主要原料合成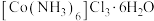 。反应原理为:
。反应原理为: 。该过程的流程如图:
。该过程的流程如图:
已知:①
 不易被氧化,
不易被氧化, 具有较强还原性。
具有较强还原性。②
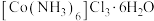 难溶于无水乙醇,在水中的溶解度随温度升高而增大。
难溶于无水乙醇,在水中的溶解度随温度升高而增大。③加入浓盐酸有利于
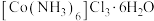 晶体析出。
晶体析出。回答下列问题:
(1)溶解
 时加入的
时加入的 有利于后续
有利于后续 与
与 的配合反应,还能抑制
的配合反应,还能抑制 的水解。写出
的水解。写出 水解的离子方程式
水解的离子方程式(2)发生“配合、氧化”的步骤在如下实验装置中进行。

①盛放混合液仪器的名称
②干燥管盛放的药品可以是
a.浓硫酸 b.五氧化二磷 c.碱石灰
③向混合溶液中首先滴加
 溶液”或“浓氨水”),完成该步骤的具体操作是
溶液”或“浓氨水”),完成该步骤的具体操作是④“配合、氧化”过程中,控制混合液温度不高于
 的原因
的原因(3)“操作1”的名称
 次,低温干燥。
次,低温干燥。
您最近半年使用:0次
6 . 下列仪器和用途对应错误的是
选项 | A | B | C | D |
仪器 |
|
|
|
|
用途 | 蒸发溶液 | 过滤 | 除去气体中杂质 | 配制溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
7 . 我国制碱工业先驱侯德榜发明了侯氏制碱法。其模拟流程如图:
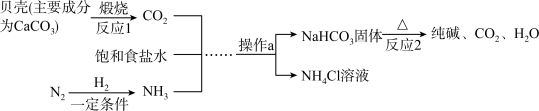
回答下列问题:
(1)饱和食盐水为氯化钠的饱和溶液,写出氯化钠在生活中的一种用途:________ 。
(2)写出N2与H2在一定条件下反应生成NH3的化学方程式:_________ 。
(3)进行操作a时所需的玻璃仪器有玻璃棒、________ 和________ 。
(4)NaHCO3固体受热分解的化学方程式为_______ 。
(5)现有ag质量分数为w的NH4Cl溶液(不考虑 与水发生的反应):
与水发生的反应):
①该溶液中所含溶质的总质量为________ (用含a、w的代数式表示,写出计算式即可)g。
②________ gNH3中所含的氮元素的总质量与该溶液中所含的氮元素的总质量相等。

回答下列问题:
(1)饱和食盐水为氯化钠的饱和溶液,写出氯化钠在生活中的一种用途:
(2)写出N2与H2在一定条件下反应生成NH3的化学方程式:
(3)进行操作a时所需的玻璃仪器有玻璃棒、
(4)NaHCO3固体受热分解的化学方程式为
(5)现有ag质量分数为w的NH4Cl溶液(不考虑
 与水发生的反应):
与水发生的反应):①该溶液中所含溶质的总质量为
②
您最近半年使用:0次
8 . 己二酸是一种重要的有机二元酸,在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用。
Ⅰ.反应原理(图甲):

Ⅱ.反应装置图(图乙):
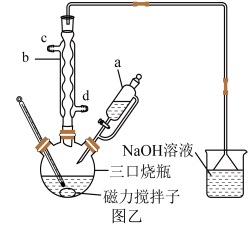
Ⅲ.反应步骤:
①在仪器a中加入环己醇,三口烧瓶中加入浓硝酸(适当过量),开启磁力搅拌,并通入冷凝水,打开仪器a的活塞,缓慢滴加环己醇。
②控制反应温度为80℃至反应结束,按顺序拆除导气吸收装置和冷凝回流装置,取下三口烧瓶,置于冰水中冷却20min以上,然后进行抽滤,用少量的冰水洗涤滤饼,即可制得己二酸粗品。
回答下列问题:
(1)加入实验药品前应进行的操作为___________ 。
(2)仪器a中的支管的用途为___________ 。
(3)仪器b的名称为___________ ,冷凝水的进水口为___________ (填“c”或“d”)。
(4)本实验最好在通风橱中进行,其原因是___________ 。
(5)写出己二酸与过量乙醇酯化反应的化学方程式___________ 。
(6)本实验需严格控制反应温度为80℃左右,温度过高可能产生的后果是___________ (写出一点即可)。
(7)己二酸可发生下列哪些反应类型___________ 。
a. 取代反应 b. 氧化反应 c. 消去反应 d. 加聚反应
Ⅰ.反应原理(图甲):

Ⅱ.反应装置图(图乙):

Ⅲ.反应步骤:
①在仪器a中加入环己醇,三口烧瓶中加入浓硝酸(适当过量),开启磁力搅拌,并通入冷凝水,打开仪器a的活塞,缓慢滴加环己醇。
②控制反应温度为80℃至反应结束,按顺序拆除导气吸收装置和冷凝回流装置,取下三口烧瓶,置于冰水中冷却20min以上,然后进行抽滤,用少量的冰水洗涤滤饼,即可制得己二酸粗品。
回答下列问题:
(1)加入实验药品前应进行的操作为
(2)仪器a中的支管的用途为
(3)仪器b的名称为
(4)本实验最好在通风橱中进行,其原因是
(5)写出己二酸与过量乙醇酯化反应的化学方程式
(6)本实验需严格控制反应温度为80℃左右,温度过高可能产生的后果是
(7)己二酸可发生下列哪些反应类型
a. 取代反应 b. 氧化反应 c. 消去反应 d. 加聚反应
您最近半年使用:0次
9 . 镁及其合金是用途很广的金属材料,可以通过以下步骤从海水中提取镁。下列说法不正确 的是
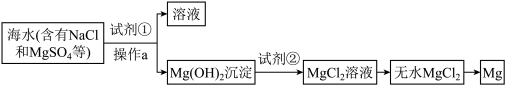

| A.试剂①常用石灰乳 |
| B.操作a是过滤 |
C.试剂②是盐酸,加入后发生反应: |
D.工业上常用加热无水 获得金属镁 获得金属镁 |
您最近半年使用:0次
10 . 单质碘有非常重要的用途,从海带燃烧后所得的海带灰中提取碘是单质碘的制备方法之一:海带燃烧后所得的海带灰中含有 ,从中获得
,从中获得 ,再由
,再由 制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:
制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:

请回答下列问题:
(1)步骤③的实验操作名称是______ (填“过滤”或“蒸发”);
(2)含碘离子溶液中加氧化剂转化为含单质碘的水溶液,能达到该目的的物质是______ (填“氯水”或“稀盐酸”);
(3)I-被氧化为I2的离子方程式为____________ ;
(4)工业上合成氨的反应为: ,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为
,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为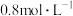
①用N2表示该反应的速率为______ ;
②其他条件不变时,升高温度,该反应的反应速率将______ (填“增大”或“减小”)。
 ,从中获得
,从中获得 ,再由
,再由 制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:
制备I2。某研究性学习小组为了从海带中提取碘,设计并进行了以下实验:
请回答下列问题:
(1)步骤③的实验操作名称是
(2)含碘离子溶液中加氧化剂转化为含单质碘的水溶液,能达到该目的的物质是
(3)I-被氧化为I2的离子方程式为
(4)工业上合成氨的反应为:
 ,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为
,一定条件下,将1molN2和3molH2置于1L的密闭容器中,10min后测得c(NH3)为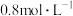
①用N2表示该反应的速率为
②其他条件不变时,升高温度,该反应的反应速率将
您最近半年使用:0次