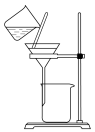
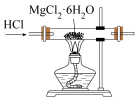
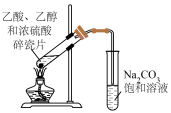
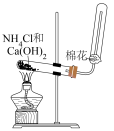
1 . 进行下列实验,装置或试剂选用错误 的是
除去 | 制取无水 |
|
|
A | B |
制备乙酸乙酯 | 制取并收集氨 |
|
|
C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 设计学生实验要注意安全、无污染、现象明显。根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(如图)。若关闭K,不能使反应停止,可将试管从烧杯中取出(会有部分气体逸散)。下列气体的制取宜使用该装置的是( )
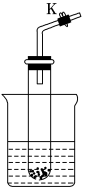

| A.用二氧化锰(粉末)与双氧水制氧气 | B.用大理石块与稀盐酸制CO2 |
| C.用硫化亚铁(块状)与盐酸制硫化氢 | D.铜片与浓硫酸制二氧化硫 |
您最近一年使用:0次
名校
解题方法
3 . “84”消毒液不能与洁厕灵混合使用。某研究小组受此启发利用以下装置进行实验,不能达到预期目的的是
|
|
|
|
| A.制备氯气 | B.净化、干燥氯气 | C.收集氯气 | D.氯气尾气处理 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-07更新
|
200次组卷
|
2卷引用:福建省厦门市国祺中学2023-2024学年高三上学期第三次月考化学试题
名校
解题方法
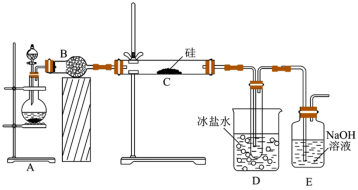
4 . 三氯硅烷(SiHCl3)可用于生产有机硅化合物、多晶硅。实验室先用NaCl固体与浓硫酸混合加热制取HCl,再利用HCl和硅粉制备三氯硅烷,实验装置如下图(加热仪器已略去)。回答下列问题: SiHCl3+H2
SiHCl3+H2
②三氯硅烷的熔点 ,沸点
,沸点 ;极易与水反应,易被氧化。
;极易与水反应,易被氧化。
(1)装置B的名称_______ ,装置B中所装药品是_______ (填“碱石灰”或“无水氯化钙”)。
(2)加热前要先通一段时间HCl气体,原因是_______ 。
(3)装置D中冰盐水的作用是_______ 。
(4)该实验装置存在明显不足,请指出:_______ 。
(5)已知 在高温条件下易分解生成
在高温条件下易分解生成 和HCl。利用
和HCl。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图所示,写出该反应的化学方程式:
)的装置如图所示,写出该反应的化学方程式:_______ 。_______ (填序号)。
 SiHCl3+H2
SiHCl3+H2 ②三氯硅烷的熔点
 ,沸点
,沸点 ;极易与水反应,易被氧化。
;极易与水反应,易被氧化。(1)装置B的名称
(2)加热前要先通一段时间HCl气体,原因是
(3)装置D中冰盐水的作用是
(4)该实验装置存在明显不足,请指出:
(5)已知
 在高温条件下易分解生成
在高温条件下易分解生成 和HCl。利用
和HCl。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图所示,写出该反应的化学方程式:
)的装置如图所示,写出该反应的化学方程式: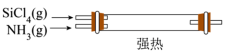
您最近一年使用:0次
名校
解题方法
5 . 利用如图装置模拟“侯氏制碱法”,通过制备的 NH3和 CO2,与饱和食盐水反应制备 NaHCO3。下列说法正确的是
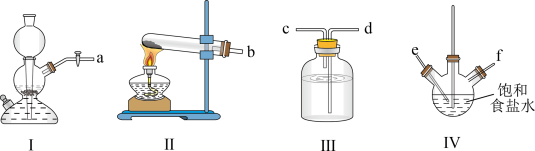

| A.实验时装置Ⅰ产生的气体应先通入装置Ⅳ中 |
| B.装置Ⅲ中的试剂为浓硫酸 |
| C.导管口的连接顺序为 aefdcb |
D.Ⅳ中反应的离子方程式为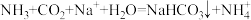 |
您最近一年使用:0次
2023-08-30更新
|
235次组卷
|
4卷引用: 福建省三明市第一中学2023-2024学年高三上学期暑假考试(开学考)化学试题
解题方法
6 .  号称绿色氧化剂,一般以30%或60%的水溶液形式存放,俗称双氧水,适用于医用伤口消毒、环境消毒和食品消毒。某制备方法及装置如图:
号称绿色氧化剂,一般以30%或60%的水溶液形式存放,俗称双氧水,适用于医用伤口消毒、环境消毒和食品消毒。某制备方法及装置如图: ;
;
② 、
、 等杂质易使催化剂
等杂质易使催化剂 中毒。
中毒。
下列说法正确的是
 号称绿色氧化剂,一般以30%或60%的水溶液形式存放,俗称双氧水,适用于医用伤口消毒、环境消毒和食品消毒。某制备方法及装置如图:
号称绿色氧化剂,一般以30%或60%的水溶液形式存放,俗称双氧水,适用于医用伤口消毒、环境消毒和食品消毒。某制备方法及装置如图: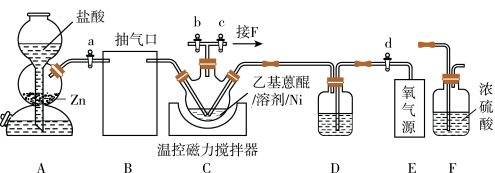
 ;
;②
 、
、 等杂质易使催化剂
等杂质易使催化剂 中毒。
中毒。下列说法正确的是
| A.可用装置A制备氯气、乙炔、乙烯 |
| B.装置B可为装有碱石灰的干燥管 |
C.反应结束装置C中混合物经过过滤加水萃取分液可获得纯净 |
| D.装置C的温控温度不能太高的主要目的是防乙基蒽醌溶剂挥发 |
您最近一年使用:0次
名校
解题方法
7 . 三氯硅烷( )可用于生产有机硅化合物、多晶硅。实验室利用硅粉和氯化氢气体制备三氯硅烷。回答下列问题:
)可用于生产有机硅化合物、多晶硅。实验室利用硅粉和氯化氢气体制备三氯硅烷。回答下列问题:
Ⅰ.实验室将 固体与浓硫酸混合加热制取
固体与浓硫酸混合加热制取 。
。

(1)上图盛装 固体的仪器名称是
固体的仪器名称是______ ,选用上图所示装置制取并收集干燥、纯净的 ,接口连接的正确顺序是
,接口连接的正确顺序是______  ______
______ ______
______ ______
______ ______
______ (每空填一个接口标号,仪器可重复使用)。
(每空填一个接口标号,仪器可重复使用)。
(2) 固体与浓硫酸制取
固体与浓硫酸制取 时发生复分解反应的化学方程式是
时发生复分解反应的化学方程式是______ 。
Ⅱ.硅粉和氯化氢反应制备三氯硅烷的装置如图所示(加热仪器已略去)。

已知:①制备三氯硅烷的化学方程式:
②三氯硅烷的熔点 ,沸点
,沸点 ;极易与水反应,易被氧化。
;极易与水反应,易被氧化。
(3)装置 所装药品是
所装药品是______ (填“碱石灰”或“无水氯化钙”),加热前要先通一段时间 气体,原因是
气体,原因是______ 。
(4)制备 时常伴有杂质
时常伴有杂质 (熔点
(熔点 ,沸点
,沸点 ),分离
),分离 和
和 的实验方法是
的实验方法是______ (填序号)。
a.过滤 b.萃取 c.蒸发结晶 d.蒸馏
(5)装置 中冰盐水的作用是
中冰盐水的作用是______ 。
(6)该实验装置存在明显不足,请指出:______ 。
 )可用于生产有机硅化合物、多晶硅。实验室利用硅粉和氯化氢气体制备三氯硅烷。回答下列问题:
)可用于生产有机硅化合物、多晶硅。实验室利用硅粉和氯化氢气体制备三氯硅烷。回答下列问题:Ⅰ.实验室将
 固体与浓硫酸混合加热制取
固体与浓硫酸混合加热制取 。
。
(1)上图盛装
 固体的仪器名称是
固体的仪器名称是 ,接口连接的正确顺序是
,接口连接的正确顺序是 ______
______ ______
______ ______
______ ______
______ (每空填一个接口标号,仪器可重复使用)。
(每空填一个接口标号,仪器可重复使用)。(2)
 固体与浓硫酸制取
固体与浓硫酸制取 时发生复分解反应的化学方程式是
时发生复分解反应的化学方程式是Ⅱ.硅粉和氯化氢反应制备三氯硅烷的装置如图所示(加热仪器已略去)。

已知:①制备三氯硅烷的化学方程式:

②三氯硅烷的熔点
 ,沸点
,沸点 ;极易与水反应,易被氧化。
;极易与水反应,易被氧化。(3)装置
 所装药品是
所装药品是 气体,原因是
气体,原因是(4)制备
 时常伴有杂质
时常伴有杂质 (熔点
(熔点 ,沸点
,沸点 ),分离
),分离 和
和 的实验方法是
的实验方法是a.过滤 b.萃取 c.蒸发结晶 d.蒸馏
(5)装置
 中冰盐水的作用是
中冰盐水的作用是(6)该实验装置存在明显不足,请指出:
您最近一年使用:0次
2024-01-31更新
|
434次组卷
|
2卷引用:福建省泉州市2023-2024学年高一上学期普通高中教学质量监测化学试卷
解题方法
8 . 某小组同学在实验室设计实验验证物质的性质及其相互转化。
I.选用如图所示的装置进行实验。

回答下列问题:
(1)实验室用 与
与 反应制取
反应制取 的发生装置为
的发生装置为___________ (填标号),该反应的化学方程式为___________________ , 的尾气处理装置为
的尾气处理装置为___________ (填标号)。
(2)实验室用 与稀硝酸反应制取NO,该气体的收集装置为
与稀硝酸反应制取NO,该气体的收集装置为___________ (填标号)。
II.设计了如图所示的实验装置模拟工业生产制备少量硝酸。
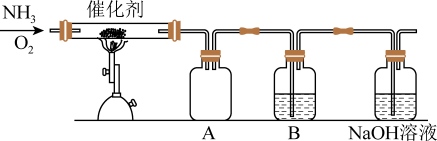
(3)B中试剂为___________ , 溶液的作用是
溶液的作用是___________ 。
(4)控制氨气和氧气的比例是制备硝酸的关键。
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。红棕色气体的化学式是___________ ,白烟的化学式是___________ 。
②欲检验尾气中是否含有氨气的方法是___________ 。
(5)工业生产中常用氨气检查输送氯气的管道是否有 泄漏。若
泄漏。若 有泄漏,可以观察到有大量的白烟生成(为
有泄漏,可以观察到有大量的白烟生成(为 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:_____ 。
I.选用如图所示的装置进行实验。

回答下列问题:
(1)实验室用
 与
与 反应制取
反应制取 的发生装置为
的发生装置为 的尾气处理装置为
的尾气处理装置为(2)实验室用
 与稀硝酸反应制取NO,该气体的收集装置为
与稀硝酸反应制取NO,该气体的收集装置为II.设计了如图所示的实验装置模拟工业生产制备少量硝酸。

(3)B中试剂为
 溶液的作用是
溶液的作用是(4)控制氨气和氧气的比例是制备硝酸的关键。
①当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。红棕色气体的化学式是
②欲检验尾气中是否含有氨气的方法是
(5)工业生产中常用氨气检查输送氯气的管道是否有
 泄漏。若
泄漏。若 有泄漏,可以观察到有大量的白烟生成(为
有泄漏,可以观察到有大量的白烟生成(为 固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
固体),同时会生成一种空气中含量最多的物质,试写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
9 . 食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少量 、
、 、
、 、
、 、
、 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:
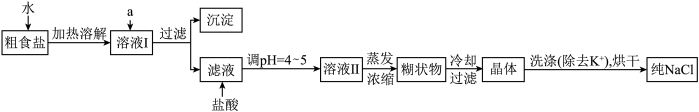
提供的试剂:饱和 溶液、饱和
溶液、饱和 溶液、NaOH溶液、
溶液、NaOH溶液、  溶液、
溶液、 溶液、75%乙醇、四氯化碳
溶液、75%乙醇、四氯化碳
①欲除去溶液Ⅰ中的 、
、 、
、 、
、 离子,选出a所代表的试剂,按滴加顺序依次是
离子,选出a所代表的试剂,按滴加顺序依次是_______ (只填化学式);
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为_______ ;
(2)用提纯的NaCl配制500 mL 4.00 NaCl溶液,所用仪器除药匙、玻璃棒外还有
NaCl溶液,所用仪器除药匙、玻璃棒外还有_______ 。
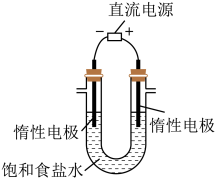
(3)电解饱和食盐水的装置如图所示,若收集的 为2 L,则同样条件下收集的
为2 L,则同样条件下收集的
_______ (填“>”、“=”或“<”)2 L,原因是_______ ,装置改进后可用于制备NaOH溶液。
(4)实验室制备 和
和 通常采用下列反应:
通常采用下列反应: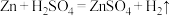 ,
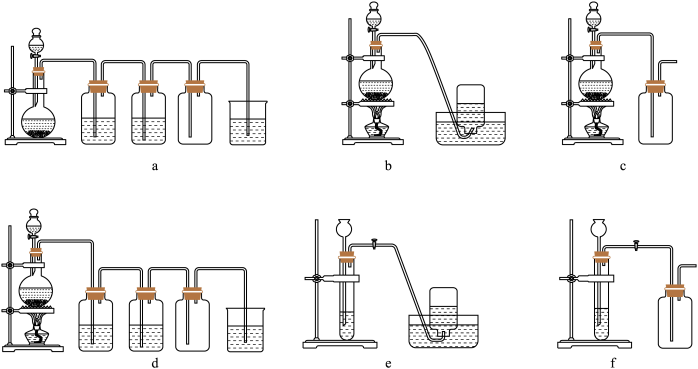
, ,据此,从下列所给仪器装置中选择制备并收集
,据此,从下列所给仪器装置中选择制备并收集 的装置
的装置_______ (填代号)和制备并收集干燥、纯净 的装置
的装置_______ (填代号)。可选用制备气体的装置见上图。
(1)粗食盐常含有少量
 、
、 、
、 、
、 、
、 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:
提供的试剂:饱和
 溶液、饱和
溶液、饱和 溶液、NaOH溶液、
溶液、NaOH溶液、  溶液、
溶液、 溶液、75%乙醇、四氯化碳
溶液、75%乙醇、四氯化碳①欲除去溶液Ⅰ中的
 、
、 、
、 、
、 离子,选出a所代表的试剂,按滴加顺序依次是
离子,选出a所代表的试剂,按滴加顺序依次是②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为
(2)用提纯的NaCl配制500 mL 4.00
 NaCl溶液,所用仪器除药匙、玻璃棒外还有
NaCl溶液,所用仪器除药匙、玻璃棒外还有(3)电解饱和食盐水的装置如图所示,若收集的
 为2 L,则同样条件下收集的
为2 L,则同样条件下收集的

(4)实验室制备
 和
和 通常采用下列反应:
通常采用下列反应: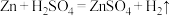 ,
, ,据此,从下列所给仪器装置中选择制备并收集
,据此,从下列所给仪器装置中选择制备并收集 的装置
的装置 的装置
的装置
您最近一年使用:0次
解题方法
10 . CS(NH2)2(硫脲,白色而有光泽的晶体,溶于水,20℃时溶解度为13.6g;在150 ℃时转变成NH4SCN)是用于制造药物、染料、金属矿物的浮选剂等的原料。某化学实验小组同学用Ca(HS)2与CaCN2(石灰氮)合成硫脲并探究其性质。
(1)制备 Ca(HS)2溶液,所用装置如图(已知酸性:H2CO3>H2S);

①装置b中盛放的试剂是_________ 。
②装置c中的长直导管的作用是_________ 。
(2)制备硫脲:将CaCN2与Ca(HS)2溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱,合适的加热方式是_________ ;该反应的化学方程式为_________ 。
(3)①取少量硫脲溶于水并加热生成NH4SCN,验证有SCN-生成的试剂是_________ 。(填化学式)
②取1.0g粗样品溶于水配制成100mL溶液,量取25.00mL于锥形瓶中,用0.5mol/L酸性KMnO4溶液滴定,滴定至终点时平均消耗酸性KMnO4溶液的体积为14.00mL,滴定至终点时的现象是_________ ,则样品纯度为_________ (已知: 5CS(NH2)2+14MnO +32H+=14Mn2++SCO2↑+5N2↑+5SO
+32H+=14Mn2++SCO2↑+5N2↑+5SO +26H2O)。
+26H2O)。
(1)制备 Ca(HS)2溶液,所用装置如图(已知酸性:H2CO3>H2S);

①装置b中盛放的试剂是
②装置c中的长直导管的作用是
(2)制备硫脲:将CaCN2与Ca(HS)2溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱,合适的加热方式是
(3)①取少量硫脲溶于水并加热生成NH4SCN,验证有SCN-生成的试剂是
②取1.0g粗样品溶于水配制成100mL溶液,量取25.00mL于锥形瓶中,用0.5mol/L酸性KMnO4溶液滴定,滴定至终点时平均消耗酸性KMnO4溶液的体积为14.00mL,滴定至终点时的现象是
 +32H+=14Mn2++SCO2↑+5N2↑+5SO
+32H+=14Mn2++SCO2↑+5N2↑+5SO +26H2O)。
+26H2O)。
您最近一年使用:0次

 胶体中的NaCl溶液
胶体中的NaCl溶液