名校
1 . 维生素C是一种水溶性维生素,有强还原性、水溶液显酸性。化学式为 。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:
。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:
【实验目的】测定某新鲜水果中维生素C的含量。
【实验原理】 ,
,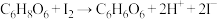 。
。
【实验用品】 标准溶液、指示剂、
标准溶液、指示剂、 溶液、
溶液、 溶液、蒸馏水等。
溶液、蒸馏水等。
【实验步骤】
(1)配制待测溶液:称取新鲜水果样品 ,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至
,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至 容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用
容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用___________ (填“酸式”或“碱式”)滴定管盛装。
(2)氧化还原滴定法:取(1)中配制好的待测溶液 于锥形瓶中,调节
于锥形瓶中,调节 至3,加入适量指示剂后,小心地滴入
至3,加入适量指示剂后,小心地滴入 标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素
标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素 的质量分数。
的质量分数。
①上述氧化还原滴定法应用___________ 作指示剂,滴定终点的现象为___________ 。
②除了样品的质量、待测溶液的体积外,计算新鲜水果中维生素C的质量分数还需要的数据有___________ 。
(3)库仑滴定法:取(1)中配制好的待测溶液 ,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。
,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。
已知:库仑仪中电解原理示意图如下。检测前,电解质溶液中 保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将
保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将 还原,库仑仪便立即自动进行电解到
还原,库仑仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。
又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。

①库仑仪工作时电解池的阳极反应式为___________ 。
②若电解消耗的电量为Q库仑,维生素C的摩尔质量为 ,则新鲜水果中维生素C的质量分数为
,则新鲜水果中维生素C的质量分数为___________ 。(用含 的代数式表示)已知:电解中转移
的代数式表示)已知:电解中转移 电子所消耗的电量为96500库仑。
电子所消耗的电量为96500库仑。
③测定过程中,需控制电解质溶液 ,当
,当 时,部分
时,部分 易被空气中的
易被空气中的 直接氧化为
直接氧化为 ,该过程的离子方程式为
,该过程的离子方程式为___________ 。这部分非电解生成的 ;将导致测得的维生素C的含量
;将导致测得的维生素C的含量___________ 。(填“偏大”或“偏小”)。
 。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:
。某小组同学测定了某新鲜水果中维生素C的含量,实验报告如下:【实验目的】测定某新鲜水果中维生素C的含量。
【实验原理】
 ,
,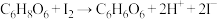 。
。【实验用品】
 标准溶液、指示剂、
标准溶液、指示剂、 溶液、
溶液、 溶液、蒸馏水等。
溶液、蒸馏水等。【实验步骤】
(1)配制待测溶液:称取新鲜水果样品
 ,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至
,加入适量蒸馏水进行粉碎、过滤,并将滤液转移至 容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用
容量瓶中,定容,随后将待测溶液加到滴定管中。根据维生素C的性质,待测溶液应用(2)氧化还原滴定法:取(1)中配制好的待测溶液
 于锥形瓶中,调节
于锥形瓶中,调节 至3,加入适量指示剂后,小心地滴入
至3,加入适量指示剂后,小心地滴入 标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素
标准溶液,直至滴定终点,记录相关数据。平行测定三次,计算新鲜水果中维生素 的质量分数。
的质量分数。①上述氧化还原滴定法应用
②除了样品的质量、待测溶液的体积外,计算新鲜水果中维生素C的质量分数还需要的数据有
(3)库仑滴定法:取(1)中配制好的待测溶液
 ,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。
,用库仑仪测定其中维生素C的含量。平行测定三次,计算新鲜水果中维生素C的质量分数。已知:库仑仪中电解原理示意图如下。检测前,电解质溶液中
 保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将
保持定值时,电解池不工作。将待测溶液加入电解池后,维生素C将 还原,库仑仪便立即自动进行电解到
还原,库仑仪便立即自动进行电解到 又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。
又回到原定值,测定结束,通过测定电解消托的电量可以求得维生素C的含量。
①库仑仪工作时电解池的阳极反应式为
②若电解消耗的电量为Q库仑,维生素C的摩尔质量为
 ,则新鲜水果中维生素C的质量分数为
,则新鲜水果中维生素C的质量分数为 的代数式表示)已知:电解中转移
的代数式表示)已知:电解中转移 电子所消耗的电量为96500库仑。
电子所消耗的电量为96500库仑。③测定过程中,需控制电解质溶液
 ,当
,当 时,部分
时,部分 易被空气中的
易被空气中的 直接氧化为
直接氧化为 ,该过程的离子方程式为
,该过程的离子方程式为 ;将导致测得的维生素C的含量
;将导致测得的维生素C的含量
您最近一年使用:0次
2023-12-11更新
|
105次组卷
|
3卷引用: 北京市第五中学2023-2024学年高二上学期12月月考化学试题
2 . 高一化学研修小组发现了一瓶消毒液(主要成分为 和
和 ),并对其展开研究:
),并对其展开研究:
已知: 和
和 在酸性条件下可发生反应:
在酸性条件下可发生反应: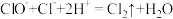 。
。
(1)消毒液中的 可吸收空气中的
可吸收空气中的 生成
生成 和
和 。写出反应的化学方程式
。写出反应的化学方程式__________________ 。而后 分解,使消毒液变质失效。
分解,使消毒液变质失效。
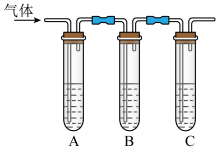
(2)取适量消毒液于试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分可以判断消毒液是否变质。
限选试剂: 浓硫酸、
浓硫酸、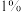 品红溶液(遇漂白性物质红色褪去)、
品红溶液(遇漂白性物质红色褪去)、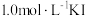 溶液(含淀粉)、
溶液(含淀粉)、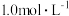
 溶液、澄清石灰水、饱和
溶液、澄清石灰水、饱和 溶液、
溶液、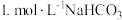 溶液。
溶液。
请完成下列实验方案。
(3)商业上常用“有效氯”来说明消毒剂的消毒能力。“有效氯”指一定质量的消毒剂与多少质量的氯气氧化能力相当,该数值以消毒剂中氯气的质量分数来表示。例如, 某消毒液与
某消毒液与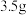 氯气的氧化能力相当,该产品的“有效氯”就是
氯气的氧化能力相当,该产品的“有效氯”就是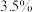 。研修小组的同学们对该瓶消毒液的“有效氯”含量进行了测定,实验步骤如下:
。研修小组的同学们对该瓶消毒液的“有效氯”含量进行了测定,实验步骤如下:
①取 消毒液放入锥形瓶中,加入过量的
消毒液放入锥形瓶中,加入过量的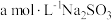 溶液
溶液 ;
;
②定量测定:向锥形瓶中滴加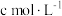 的酸性
的酸性 溶液,使之和剩余的
溶液,使之和剩余的 溶液反应,恰好完全反应时,消耗
溶液反应,恰好完全反应时,消耗 溶液
溶液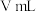 。
。
测定过程中涉及的反应有: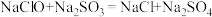 ;
;
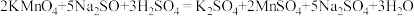
该消毒液的“有效氯”含量为____________________ 。(用含a、b、c、V的代数式表示)。
 和
和 ),并对其展开研究:
),并对其展开研究:已知:
 和
和 在酸性条件下可发生反应:
在酸性条件下可发生反应: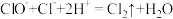 。
。(1)消毒液中的
 可吸收空气中的
可吸收空气中的 生成
生成 和
和 。写出反应的化学方程式
。写出反应的化学方程式 分解,使消毒液变质失效。
分解,使消毒液变质失效。(2)取适量消毒液于试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分可以判断消毒液是否变质。

限选试剂:
 浓硫酸、
浓硫酸、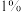 品红溶液(遇漂白性物质红色褪去)、
品红溶液(遇漂白性物质红色褪去)、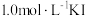 溶液(含淀粉)、
溶液(含淀粉)、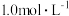
 溶液、澄清石灰水、饱和
溶液、澄清石灰水、饱和 溶液、
溶液、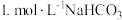 溶液。
溶液。请完成下列实验方案。
所加试剂 | 预期现象和结论 |
| 试管A中加① 试管B中加② 试管C中加澄清石灰水。 | 若A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊。则消毒液部分变质; 若③ |
(3)商业上常用“有效氯”来说明消毒剂的消毒能力。“有效氯”指一定质量的消毒剂与多少质量的氯气氧化能力相当,该数值以消毒剂中氯气的质量分数来表示。例如,
 某消毒液与
某消毒液与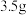 氯气的氧化能力相当,该产品的“有效氯”就是
氯气的氧化能力相当,该产品的“有效氯”就是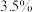 。研修小组的同学们对该瓶消毒液的“有效氯”含量进行了测定,实验步骤如下:
。研修小组的同学们对该瓶消毒液的“有效氯”含量进行了测定,实验步骤如下:①取
 消毒液放入锥形瓶中,加入过量的
消毒液放入锥形瓶中,加入过量的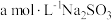 溶液
溶液 ;
;②定量测定:向锥形瓶中滴加
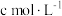 的酸性
的酸性 溶液,使之和剩余的
溶液,使之和剩余的 溶液反应,恰好完全反应时,消耗
溶液反应,恰好完全反应时,消耗 溶液
溶液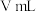 。
。测定过程中涉及的反应有:
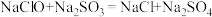 ;
;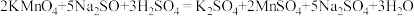
该消毒液的“有效氯”含量为
您最近一年使用:0次
名校
解题方法
3 . 大量燃烧含硫量高的煤容易造成酸雨污染,因此,我国北方地区在采暖季全面推行“煤改气”,同时提高煤的脱硫效率,减少污染的排放。
【提出问题】通过实验证明煤中含有碳元素和硫元素。
【查阅资料】二氧化硫能使高锰酸钾溶液褪色(由紫色变为无色),该反应的化学方程式为:
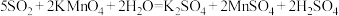 。
。
(1)预测性质:二氧化硫和二氧化碳都是酸性氧化物,两者应具有相似的化学性质。
请写出少量二氧化硫通入澄清石灰水产生白色沉淀所发生的反应的化学方程式:_______ 。
(2)设计实验:根据上述资料和预测,甲、乙、丙三位同学分别设计实验方案进行探究。
甲同学进行了如下图所示A、B两步实验:

甲同学的部分实验报告如下:
乙同学认为甲同学的实验方案不合理,其理由是:_______ 。
(3)丙同学进行了如下图所示实验(部分装置在图中略去):
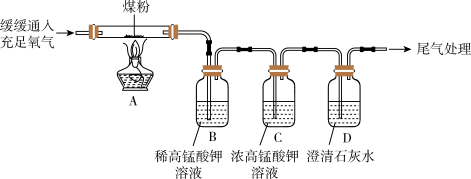
【探究与结论】
图C装置的作用是_______ 。
丙同学的实验能证明煤中含有碳元素的现象是:
C中溶液_______ ,D中溶液_______ 。
(4)【拓展研究】工业上通常用来吸收燃煤烟气中的 的方法有两种:
的方法有两种:
方法一:在燃煤过程中加入生石灰,称为“钙基固硫法”,反应可看作两步:
①_______ (写出方程式) ②产物进一步与 反应生成
反应生成
方法二:用足量的氨水(其溶质 是一种一元弱碱)吸收
是一种一元弱碱)吸收 ,生成铵盐可作为氮肥加以利用,写出吸收过程的化学方程式
,生成铵盐可作为氮肥加以利用,写出吸收过程的化学方程式_______ 。
【提出问题】通过实验证明煤中含有碳元素和硫元素。
【查阅资料】二氧化硫能使高锰酸钾溶液褪色(由紫色变为无色),该反应的化学方程式为:
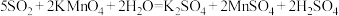 。
。(1)预测性质:二氧化硫和二氧化碳都是酸性氧化物,两者应具有相似的化学性质。
请写出少量二氧化硫通入澄清石灰水产生白色沉淀所发生的反应的化学方程式:
(2)设计实验:根据上述资料和预测,甲、乙、丙三位同学分别设计实验方案进行探究。
甲同学进行了如下图所示A、B两步实验:

甲同学的部分实验报告如下:
实验现象 | 实验结论 |
| A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。 | 煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。 |
(3)丙同学进行了如下图所示实验(部分装置在图中略去):

【探究与结论】
图C装置的作用是
丙同学的实验能证明煤中含有碳元素的现象是:
C中溶液
(4)【拓展研究】工业上通常用来吸收燃煤烟气中的
 的方法有两种:
的方法有两种:方法一:在燃煤过程中加入生石灰,称为“钙基固硫法”,反应可看作两步:
①
 反应生成
反应生成
方法二:用足量的氨水(其溶质
 是一种一元弱碱)吸收
是一种一元弱碱)吸收 ,生成铵盐可作为氮肥加以利用,写出吸收过程的化学方程式
,生成铵盐可作为氮肥加以利用,写出吸收过程的化学方程式
您最近一年使用:0次
2023-10-15更新
|
241次组卷
|
3卷引用:北京市八一学校2023-2024学年高一上学期10月月考化学(A卷)试题
名校
解题方法
4 . 红矾钠( )可用于制备制革产业中的铬鞣剂。对含铬污泥进行酸浸处理后,得到浸出液(主要含
)可用于制备制革产业中的铬鞣剂。对含铬污泥进行酸浸处理后,得到浸出液(主要含 和
和 ),经过如下主要流程,可制得红矾钠,实现铬资源的有效循环利用。
),经过如下主要流程,可制得红矾钠,实现铬资源的有效循环利用。

已知:i. 溶液中存在以下平衡:
溶液中存在以下平衡:
ii.相关金属离子形成氢氧化物沉淀的 范围如下:
范围如下:
(1)Ⅱ中,加入 调节
调节 至___________(填字母)。
至___________(填字母)。
(2)Ⅲ中, 氧化
氧化 沉淀的离子反应方程式为
沉淀的离子反应方程式为___________ 。
(3)Ⅲ中,在投料比、反应时间均相同时,若温度过高, 的产率反而降低,可能的原因是
的产率反而降低,可能的原因是___________ 。
(4)Ⅳ中,加入 的作用是
的作用是___________ (结合平衡移动原理解释)。
(5)为了测定获得红矾钠 的纯度,称取上述流程中的产品
的纯度,称取上述流程中的产品 配成
配成 溶液,取出
溶液,取出 放于锥形瓶中,加入稀硫酸和足量的
放于锥形瓶中,加入稀硫酸和足量的 溶液,置于暗处充分反应至
溶液,置于暗处充分反应至 全部转化为
全部转化为 后,滴入
后,滴入 滴淀粉溶液,最后用浓度为
滴淀粉溶液,最后用浓度为 的
的 标准溶液滴定,共消耗
标准溶液滴定,共消耗 。(已知:
。(已知: 。)
。)
①滴定终点的现象为___________ 。
②所得 (摩尔质量为
(摩尔质量为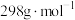 )的纯度表达式为
)的纯度表达式为___________ (用质量分数表示)。
 )可用于制备制革产业中的铬鞣剂。对含铬污泥进行酸浸处理后,得到浸出液(主要含
)可用于制备制革产业中的铬鞣剂。对含铬污泥进行酸浸处理后,得到浸出液(主要含 和
和 ),经过如下主要流程,可制得红矾钠,实现铬资源的有效循环利用。
),经过如下主要流程,可制得红矾钠,实现铬资源的有效循环利用。
已知:i.
 溶液中存在以下平衡:
溶液中存在以下平衡:
ii.相关金属离子形成氢氧化物沉淀的
 范围如下:
范围如下:| 金属离子 | 开始沉淀的 | 沉淀完全的 |
 | 4.3 | 5.6 |
 | 7.1 | 9.2 |
(1)Ⅱ中,加入
 调节
调节 至___________(填字母)。
至___________(填字母)。A. | B.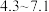 | C.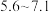 | D.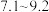 |
(2)Ⅲ中,
 氧化
氧化 沉淀的离子反应方程式为
沉淀的离子反应方程式为(3)Ⅲ中,在投料比、反应时间均相同时,若温度过高,
 的产率反而降低,可能的原因是
的产率反而降低,可能的原因是(4)Ⅳ中,加入
 的作用是
的作用是(5)为了测定获得红矾钠
 的纯度,称取上述流程中的产品
的纯度,称取上述流程中的产品 配成
配成 溶液,取出
溶液,取出 放于锥形瓶中,加入稀硫酸和足量的
放于锥形瓶中,加入稀硫酸和足量的 溶液,置于暗处充分反应至
溶液,置于暗处充分反应至 全部转化为
全部转化为 后,滴入
后,滴入 滴淀粉溶液,最后用浓度为
滴淀粉溶液,最后用浓度为 的
的 标准溶液滴定,共消耗
标准溶液滴定,共消耗 。(已知:
。(已知: 。)
。)①滴定终点的现象为
②所得
 (摩尔质量为
(摩尔质量为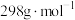 )的纯度表达式为
)的纯度表达式为
您最近一年使用:0次
2023-12-01更新
|
192次组卷
|
3卷引用:北京汇文中学2023-2024学年高二上学期期中考试化学试题
解题方法
5 . 以次氯酸盐为有效成分的消毒剂应用广泛。电解 溶液制备
溶液制备 溶液的装置示意如下。
溶液的装置示意如下。
(1)产生
①生成 的反应包括:
的反应包括: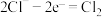 、
、 、
、___________ 。
②测所得溶液 ,试纸先变蓝
,试纸先变蓝 后褪色,说明溶液具有的性质是
后褪色,说明溶液具有的性质是___________ 。
(2)相同温度下,在不同初始 下电解
下电解 溶液,
溶液, 对
对 浓度影响如下所示。
浓度影响如下所示。 浓度在
浓度在 为3或13时较小的原因:
为3或13时较小的原因:
Ⅰ. 时,
时, 的溶解度减小
的溶解度减小
Ⅱ. 时,___________
时,___________
①根据化学平衡移动原理,推测Ⅰ合理。依据的化学平衡是___________ 。
②补全猜想Ⅱ,经过检验,推测Ⅱ成立___________ 。
根据上述实验,说明电解法制备 溶液,初始
溶液,初始 不宜过小或过大。
不宜过小或过大。
(3)用同样方法电解 溶液制备
溶液制备 ,电解难以持续,推测原因:
,电解难以持续,推测原因:___________ 。
【测量】
(4)取 所得
所得 样液,加水稀释。依次加入
样液,加水稀释。依次加入 溶液、稀
溶液、稀 。析出的
。析出的 用
用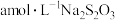 标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗
标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗 溶液
溶液 。(已知:
。(已知: )样液中
)样液中
___________  。
。
 溶液制备
溶液制备 溶液的装置示意如下。
溶液的装置示意如下。
(1)产生

①生成
 的反应包括:
的反应包括: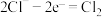 、
、 、
、②测所得溶液
 ,试纸先变蓝
,试纸先变蓝 后褪色,说明溶液具有的性质是
后褪色,说明溶液具有的性质是(2)相同温度下,在不同初始
 下电解
下电解 溶液,
溶液, 对
对 浓度影响如下所示。
浓度影响如下所示。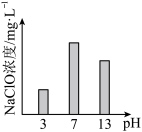
 浓度在
浓度在 为3或13时较小的原因:
为3或13时较小的原因:Ⅰ.
 时,
时, 的溶解度减小
的溶解度减小Ⅱ.
 时,___________
时,___________①根据化学平衡移动原理,推测Ⅰ合理。依据的化学平衡是
②补全猜想Ⅱ,经过检验,推测Ⅱ成立
根据上述实验,说明电解法制备
 溶液,初始
溶液,初始 不宜过小或过大。
不宜过小或过大。(3)用同样方法电解
 溶液制备
溶液制备 ,电解难以持续,推测原因:
,电解难以持续,推测原因:【测量】
(4)取
 所得
所得 样液,加水稀释。依次加入
样液,加水稀释。依次加入 溶液、稀
溶液、稀 。析出的
。析出的 用
用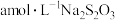 标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗
标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗 溶液
溶液 。(已知:
。(已知: )样液中
)样液中
 。
。
您最近一年使用:0次
2014·北京海淀·二模
名校
6 . 研究小组用下图装置制取Cl2,证明产生的气体中含有HCl。

(1)仪器A的名称为______ ;A中反应的离子方程式为_______ 。
(2)甲同学将A中产生的气体通入下列溶液:
①实验a中的现象为 ___ 。
②不能证明产生的气体中含有HCl的实验是__ (填字母序号)。
(3)已知将HCl气体通入饱和食盐水中有白色固体析出。乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因:___________ 。
(4)已知:2S2O +I2=S4O
+I2=S4O + 2I - 。丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl。
+ 2I - 。丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl。
I.测定X中溶解的Cl 2 。取25.00 mL溶液X,加入过量KI溶液,然后用0.04 molL -1 Na2O3 溶液滴定生成的I2,达滴定终点时消耗Na2 S2O3溶液V mL。
II.测定X中Cl元素总量。另取25.00 mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl-,再用0.10 molL -1 AgNO3 溶液滴定所得溶液中的Cl-。X中的HClO不会影响I的测定结果,原因是__ 。由I、II 中实验数据可证明A中产生的气体中含有HCl,则II中消耗0.10 molL -1 AgNO3 溶液的体积应大于 __ mL(用含V的代数式表示)。

(1)仪器A的名称为
(2)甲同学将A中产生的气体通入下列溶液:
| 实验序号 | 试剂 | 现象 |
| a | 紫色石蕊溶液 | |
| b | AgNO3 溶液 | 出现白色沉淀 |
②不能证明产生的气体中含有HCl的实验是
(3)已知将HCl气体通入饱和食盐水中有白色固体析出。乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因:
(4)已知:2S2O
 +I2=S4O
+I2=S4O + 2I - 。丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl。
+ 2I - 。丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl。 I.测定X中溶解的Cl 2 。取25.00 mL溶液X,加入过量KI溶液,然后用0.04 molL -1 Na2O3 溶液滴定生成的I2,达滴定终点时消耗Na2 S2O3溶液V mL。
II.测定X中Cl元素总量。另取25.00 mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl-,再用0.10 molL -1 AgNO3 溶液滴定所得溶液中的Cl-。X中的HClO不会影响I的测定结果,原因是
您最近一年使用:0次
2016-12-09更新
|
1273次组卷
|
3卷引用:2013-2014北京市海淀区高三第二学期二模理综化学试卷
(已下线)2013-2014北京市海淀区高三第二学期二模理综化学试卷北京市清华大学附属中学2018届高三10月月考化学试题人教版2017-2018学年高一化学必修1:4.2 富集在海水中的元素-氯 同步测试2



