名校
1 . 亚氯酸钠固体是一种重要氧化剂和漂白剂,用亚氯酸钠固体与纯净的氯气反应可以得到ClO2。ClO2是一种易溶于水而难溶于有机溶剂的气体,制取反应如下: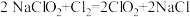 。回答下列问题:
。回答下列问题:
I.下图是实验室制备并收集一定量纯净ClO2的装置。
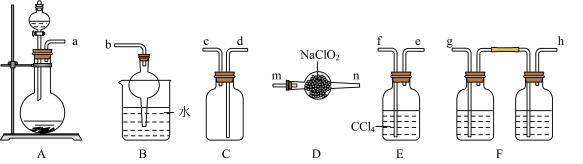
(1)装置连接顺序为a→___________ (按气流方向,用小写字母表示)。
(2)F中的试剂依次为___________ 、___________ ;E装置的作用是___________ 。
II.探究NaClO2的氧化性及测定其纯度时进行了如下实验:
(3)完成表格中内容。
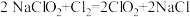 。回答下列问题:
。回答下列问题:I.下图是实验室制备并收集一定量纯净ClO2的装置。

(1)装置连接顺序为a→
(2)F中的试剂依次为
II.探究NaClO2的氧化性及测定其纯度时进行了如下实验:
(3)完成表格中内容。
| 实验目的 | 操作步骤 | 现象或原因 |
| ①证明NaClO2具有氧化性 | 取一定量的样品,用H2SO4酸化,再加入适量 | 溶液显红色 |
| ②测定NaClO2的纯度 | i.准确称一定质量的样品,在酸性条件下加入适量蒸馏水和足量的KI晶体 | 致溶液显黄色的离子方程式: |
| ii.用 | 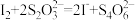 | |
| iii.用一定浓度的Na2S2O3标准液滴定,当 | 精确记录数据并进行计算 |
您最近一年使用:0次
2 . 实验目的:为研究铁质材料与热浓硫酸的反应
(1)称取铁钉(碳素钢 ) 放入
放入 浓硫酸中,加热,充分反应后得到溶液
浓硫酸中,加热,充分反应后得到溶液 并收集到气体
并收集到气体 。
。
①甲同学认为 中除
中除 外还可能含有
外还可能含有 。若要确认其中是否含有
。若要确认其中是否含有 ,应选择加入的试剂为
,应选择加入的试剂为___________ (选填序号)
A. 溶液和氯水 B.铁粉和
溶液和氯水 B.铁粉和 溶液 C.浓氨水 D.酸性
溶液 C.浓氨水 D.酸性 溶液
溶液
②乙同学取 (标准状况)气体
(标准状况)气体 通入足量溴水中,然后加入足量
通入足量溴水中,然后加入足量 溶液,经适当操作后得到干燥固体
溶液,经适当操作后得到干燥固体 。据此推知气体
。据此推知气体 中
中 的体积分数为
的体积分数为___________ 。(保留三位有效数字)。
(2)分析上述实验中 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有 和
和 气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有
气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有 的原因是
的原因是___________ 。

(3)装置A中试剂的作用是___________ ,反应的离子方程式___________ 。
(4)简述确认气体Y中含有 的实验现象
的实验现象___________ 。
(5)如果气体Y中含有 ,预计实验现象应是
,预计实验现象应是___________ 。
(1)称取铁钉(
 放入
放入 浓硫酸中,加热,充分反应后得到溶液
浓硫酸中,加热,充分反应后得到溶液 并收集到气体
并收集到气体 。
。①甲同学认为
 中除
中除 外还可能含有
外还可能含有 。若要确认其中是否含有
。若要确认其中是否含有 ,应选择加入的试剂为
,应选择加入的试剂为A.
 溶液和氯水 B.铁粉和
溶液和氯水 B.铁粉和 溶液 C.浓氨水 D.酸性
溶液 C.浓氨水 D.酸性 溶液
溶液②乙同学取
 (标准状况)气体
(标准状况)气体 通入足量溴水中,然后加入足量
通入足量溴水中,然后加入足量 溶液,经适当操作后得到干燥固体
溶液,经适当操作后得到干燥固体 。据此推知气体
。据此推知气体 中
中 的体积分数为
的体积分数为(2)分析上述实验中
 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有 和
和 气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有
气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有 的原因是
的原因是
(3)装置A中试剂的作用是
(4)简述确认气体Y中含有
 的实验现象
的实验现象(5)如果气体Y中含有
 ,预计实验现象应是
,预计实验现象应是
您最近一年使用:0次
2021-10-10更新
|
285次组卷
|
5卷引用:河北省衡水市武邑武罗学校2020-2021学年高三上学期期中考试化学试题
名校
3 . 下列所示装置或操作能达到实验目的的是
| A | B | C | D |
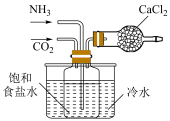 | 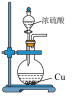 | 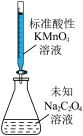 | 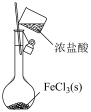 |
模拟侯氏制碱法获得 | 制备 | 测定未知 溶液的浓度 溶液的浓度 | 配制 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 含有实验装置类的试题,常常是围绕某一实验目的所进行的系统操作,解答时重在依据实验中各物质的性质与转化、装置的结构与功能、反应条件的控制等。
(1)某学习小组设计实验制备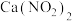 。实验装置如图1所示(夹持装置已略去)。
。实验装置如图1所示(夹持装置已略去)。
已知: ;
;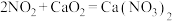 。
。

①向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的 ,目的是
,目的是_______ 。
②B中盛放的试剂是_______ 。
(2)硫代硫酸钠( )可用做分析试剂及鞣革还原剂。它受热、遇酸易分解。实验室模拟工业上制备硫代硫酸钠:
)可用做分析试剂及鞣革还原剂。它受热、遇酸易分解。实验室模拟工业上制备硫代硫酸钠: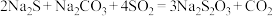 的装置如图2。
的装置如图2。
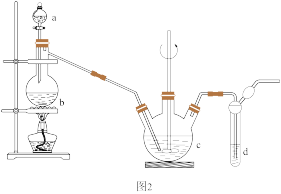
①a、b中试剂分别为 溶液和
溶液和 固体,c中试剂为
固体,c中试剂为_______ ,d中的试剂为_______ 。
②为了保证硫代硫酸钠的产量,实验中通入的 不能过量,原因是
不能过量,原因是_______ 。
(3)实验室用图3装置测定FeO和 固体混合物中
固体混合物中 的质量,D装置的硬质双通玻璃管中的固体物质是FeO和
的质量,D装置的硬质双通玻璃管中的固体物质是FeO和 的混合物。
的混合物。

装置B的作用是_______ ;装置C中装的液体是_______ ;F所起的作用是_______ 。
(1)某学习小组设计实验制备
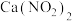 。实验装置如图1所示(夹持装置已略去)。
。实验装置如图1所示(夹持装置已略去)。已知:
 ;
;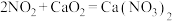 。
。
①向三颈烧瓶中加入稀硝酸之前,应向装置中通入一段时间的
 ,目的是
,目的是②B中盛放的试剂是
(2)硫代硫酸钠(
 )可用做分析试剂及鞣革还原剂。它受热、遇酸易分解。实验室模拟工业上制备硫代硫酸钠:
)可用做分析试剂及鞣革还原剂。它受热、遇酸易分解。实验室模拟工业上制备硫代硫酸钠: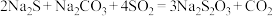 的装置如图2。
的装置如图2。
①a、b中试剂分别为
 溶液和
溶液和 固体,c中试剂为
固体,c中试剂为②为了保证硫代硫酸钠的产量,实验中通入的
 不能过量,原因是
不能过量,原因是(3)实验室用图3装置测定FeO和
 固体混合物中
固体混合物中 的质量,D装置的硬质双通玻璃管中的固体物质是FeO和
的质量,D装置的硬质双通玻璃管中的固体物质是FeO和 的混合物。
的混合物。
装置B的作用是
您最近一年使用:0次
5 . 氯酸钾(KClO3)和次氯酸钠(NaClO)是氯元素重要的含氧酸盐,实验室中利用下图装置制备这两种盐。
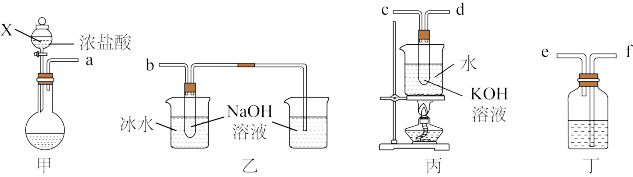
回答下列问题:
(1)仪器X名称是________ ,甲装置圆底烧瓶中的试剂为K2Cr2O7固体,写出发生反应的离子方程式________ 。
(2)为达成实验目的,上述仪器口连接顺序依次为:a-_________ 。
(3)丁装置中所盛试剂为_______ ;乙装置中采用冰水浴冷却的目的是_______ 。
(4)反应结束,取出b中试管,经冷却结晶,_____ ,______ ,干燥,得到KClO3晶体。
(5)为进一步测定所得KClO3晶体的纯度,设计了如下实验方案:
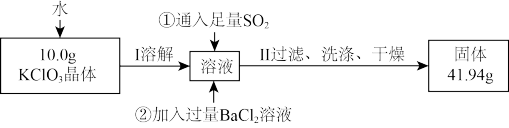
写出通入足量SO2时,溶液中发生反应的离子方程式_________ 。依据上述实验结果,测得该晶体的纯度为_________ 。

回答下列问题:
(1)仪器X名称是
(2)为达成实验目的,上述仪器口连接顺序依次为:a-
(3)丁装置中所盛试剂为
(4)反应结束,取出b中试管,经冷却结晶,
(5)为进一步测定所得KClO3晶体的纯度,设计了如下实验方案:

写出通入足量SO2时,溶液中发生反应的离子方程式
您最近一年使用:0次
名校
解题方法
6 . 某研究小组模拟工业上以黄铁矿为原料制备硫酸的第一步反应如下:4FeS2+11O2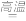 2Fe2O3+8SO2进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
2Fe2O3+8SO2进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
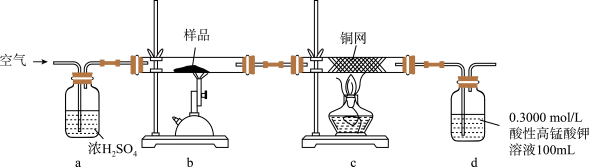
实验步骤:称取研细的样品4.000g放入上图b装置中,然后在空气中进行煅烧。为测定未反应高锰酸钾的量(假设其溶液体积保持不变),实验完成后取出d中溶液10mL置于锥形瓶里,用0.1000mol/L草酸(H2C2O4)标准溶液进行滴定。(已知:5SO2 + 2KMnO4 + 2H2O = K2SO4 + 2MnSO4 + 2H2SO4 )请回答下列问题:
(1)称量样品质量能否用托盘天平_______ (填“能”或“不能”),取出d中溶液10mL需要用______ 准确量取(填序号)
A.容量瓶 B.量筒 C.碱式滴定管 D.酸式滴定管
(2)上述反应结束后,仍需通一段时间的空气,其目的是__________
(3)已知草酸与高锰酸钾酸性溶液作用有CO2和Mn2+等物质生成,则滴定时发生反应的离子方程式为_______________ ﹔判断滴定到达终点的方法是___________ 。
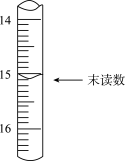
(4)已知滴定管初读数为0.10mL,末读数如图所示,消耗草酸溶液的体积为___________ mL。
下列操作会导致该样品中FeS2的纯度测定结果偏高的是_________ (填序号)
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(5)该样品中FeS2的纯度为__________________
(6)若用下图装置替代上述实验装置d,同样可以达到实验目的的是_______ (填编号)。
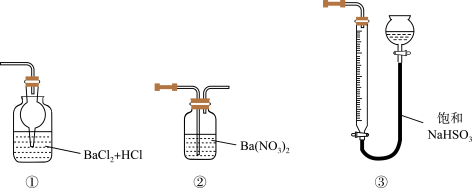
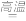 2Fe2O3+8SO2进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
2Fe2O3+8SO2进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
实验步骤:称取研细的样品4.000g放入上图b装置中,然后在空气中进行煅烧。为测定未反应高锰酸钾的量(假设其溶液体积保持不变),实验完成后取出d中溶液10mL置于锥形瓶里,用0.1000mol/L草酸(H2C2O4)标准溶液进行滴定。(已知:5SO2 + 2KMnO4 + 2H2O = K2SO4 + 2MnSO4 + 2H2SO4 )请回答下列问题:
(1)称量样品质量能否用托盘天平
A.容量瓶 B.量筒 C.碱式滴定管 D.酸式滴定管
(2)上述反应结束后,仍需通一段时间的空气,其目的是
(3)已知草酸与高锰酸钾酸性溶液作用有CO2和Mn2+等物质生成,则滴定时发生反应的离子方程式为
(4)已知滴定管初读数为0.10mL,末读数如图所示,消耗草酸溶液的体积为

下列操作会导致该样品中FeS2的纯度测定结果偏高的是
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(5)该样品中FeS2的纯度为
(6)若用下图装置替代上述实验装置d,同样可以达到实验目的的是

您最近一年使用:0次
2019-11-28更新
|
236次组卷
|
2卷引用:云南省玉溪一中2020届高三上学期期中考试理综化学试题
7 . 完成下列实验,所选装置正确的是
| A | B | C | D | |
| 实验目的 | 检查装置气密性 | 实验室用纯碱和稀硫酸制备二氧化碳 | 用已知浓度的氢氧化钠溶液测定未知浓度盐酸 | 选择合适的试剂,可分别制取少量CO2、NO和O2 |
| 实验 装置 | 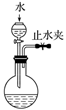 | 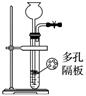 | 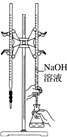 | 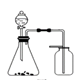 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-11-20更新
|
431次组卷
|
5卷引用:【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期期中考试化学试题
【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期期中考试化学试题天津市河北区2021届高三一模考试化学试题(已下线)押山东卷第05题 实验装置的评价-备战2021年高考化学临考题号押题(山东卷)福建省宁化第一中学2021-2022学年高三上学期第二次阶段考试化学试题(已下线)专题13 装置气密性的检查方法-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
名校
解题方法
8 .  常用于污水处理、金属蚀刻等领域,某兴趣小组利用如图所示的实验装置制备并收集
常用于污水处理、金属蚀刻等领域,某兴趣小组利用如图所示的实验装置制备并收集 。
。

已知:① 固体在潮湿空气中容易变质,且易升华;
固体在潮湿空气中容易变质,且易升华;
②向含 的溶液中滴加
的溶液中滴加 溶液,生成深蓝色沉淀。
溶液,生成深蓝色沉淀。
请回答下列问题:
(1)仪器a的名称是___________ 。
(2)装置A圆底烧瓶中的固体为 ,请写出装置A中发生反应的离子方程式:
,请写出装置A中发生反应的离子方程式:___________ 。
(3)装置C中的试剂c的作用是___________ ,装置F中加入试剂d的作用是___________ 。
(4)实验时,应先点燃___________ (填“A”或“D”)处酒精灯,理由是___________ 。
(5)该兴趣小组想要对反应后装置D中剩余物质的成分进行检验,设计了如下的实验方案:
甲同学认为,实验Ⅲ中的现象无法说明反应后装置D中剩余物质中含有 ,原因是④
,原因是④___________ (用化学方程式 表示)。
 常用于污水处理、金属蚀刻等领域,某兴趣小组利用如图所示的实验装置制备并收集
常用于污水处理、金属蚀刻等领域,某兴趣小组利用如图所示的实验装置制备并收集 。
。
已知:①
 固体在潮湿空气中容易变质,且易升华;
固体在潮湿空气中容易变质,且易升华;②向含
 的溶液中滴加
的溶液中滴加 溶液,生成深蓝色沉淀。
溶液,生成深蓝色沉淀。请回答下列问题:
(1)仪器a的名称是
(2)装置A圆底烧瓶中的固体为
 ,请写出装置A中发生反应的离子方程式:
,请写出装置A中发生反应的离子方程式:(3)装置C中的试剂c的作用是
(4)实验时,应先点燃
(5)该兴趣小组想要对反应后装置D中剩余物质的成分进行检验,设计了如下的实验方案:
| 实验序号 | 实验操作 | 预期现象 | 实验结论 |
| Ⅰ | 取少量D中的固体物质,用磁铁吸引 | 磁铁上吸引了黑色物质 | ① |
| Ⅱ | 另取少量固体于试管中,加入适量水溶解,向试管中滴加少量② | 固体物质完全溶解,③ | 固体中含有 |
| Ⅲ | 再取少量固体于试管中,加入适量水溶解,向试管中滴加 溶液 溶液 | 固体物质完全溶解,有深蓝色沉淀生成 | 固体中含有 |
 ,原因是④
,原因是④
您最近一年使用:0次
名校
9 . 某同学用 与浓盐酸反应制备纯净的
与浓盐酸反应制备纯净的 的装置如图所示。回答下列问题:
的装置如图所示。回答下列问题:
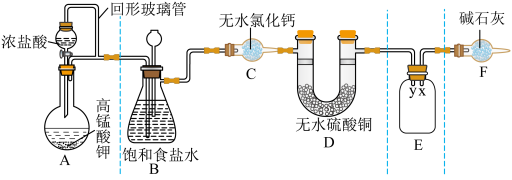
已知: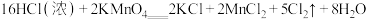
(1)装置A中盛放浓盐酸的仪器名称是
(2)E装置中导管(填“x”或“y”)
(3)装置F的作用有两个:一是
请写出氯气与碱石灰反应的化学方程式
(4)
 、HClO和
、HClO和 三种微粒的物质的量分数随pH(即
三种微粒的物质的量分数随pH(即 )变化的关系如图所示。
)变化的关系如图所示。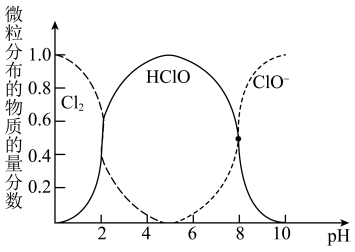
回答问题:①使用84消毒液时为增强消毒效果常调节4<pH<6,原因是
②通常购买的84消毒液pH在12左右,为增强消毒效果可向其中滴加
A.可口可乐 B.稀 C.食醋 D.浓盐酸
C.食醋 D.浓盐酸
(5)实验室将
 通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为
通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为 ,计算此时所得溶液中NaClO的质量分数为
,计算此时所得溶液中NaClO的质量分数为
您最近一年使用:0次
名校
10 . 三氯化六氨合钴 ,在钴化合物的合成中是重要原料。实验室以
,在钴化合物的合成中是重要原料。实验室以 为原料制备
为原料制备 ,步骤如下:
,步骤如下:
Ⅰ. 的制备。
的制备。
 可以通过钴和氯气反应制得,实验室制备纯净
可以通过钴和氯气反应制得,实验室制备纯净 可用下图实验装置实现(已知:钴单质在300℃以上易被氧气氧化,
可用下图实验装置实现(已知:钴单质在300℃以上易被氧气氧化, 易潮解)。
易潮解)。
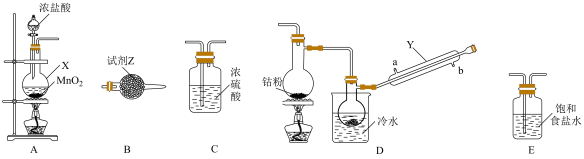
(1)仪器Y的名称为___________ ,试剂Z为___________ 。
(2)X中发生反应的化学方程式为___________ 。
(3)装置的连接顺序为A→___________ →B(按气流方向,用大写字母表示,反应开始前应先点燃___________ 处的酒精灯。
Ⅱ.三氯化六氨合钴(Ⅲ)的制备。
原理为:

(4)水浴温度不超过60℃的原因是___________ 。
(5)加入浓盐酸,析出产品的离子方程式为___________ 。
Ⅲ.测定 中钴的含量。
中钴的含量。
(6)原理:利用 将KI氧化成
将KI氧化成 ,
, 被还原为
被还原为 。然后用淀粉溶液作指示剂,0.015
。然后用淀粉溶液作指示剂,0.015
 标准溶液滴定生成的
标准溶液滴定生成的 ,
, 转化为
转化为 。若称取样品的质量为0.27g,滴定
。若称取样品的质量为0.27g,滴定 时,达到终点消耗
时,达到终点消耗 标准溶液的平均体积为54.00mL。滴定终点的现象为
标准溶液的平均体积为54.00mL。滴定终点的现象为___________ ,该样品中钴元素的质量分数为___________ 。
 ,在钴化合物的合成中是重要原料。实验室以
,在钴化合物的合成中是重要原料。实验室以 为原料制备
为原料制备 ,步骤如下:
,步骤如下:Ⅰ.
 的制备。
的制备。 可以通过钴和氯气反应制得,实验室制备纯净
可以通过钴和氯气反应制得,实验室制备纯净 可用下图实验装置实现(已知:钴单质在300℃以上易被氧气氧化,
可用下图实验装置实现(已知:钴单质在300℃以上易被氧气氧化, 易潮解)。
易潮解)。
(1)仪器Y的名称为
(2)X中发生反应的化学方程式为
(3)装置的连接顺序为A→
Ⅱ.三氯化六氨合钴(Ⅲ)的制备。
原理为:


(4)水浴温度不超过60℃的原因是
(5)加入浓盐酸,析出产品的离子方程式为
Ⅲ.测定
 中钴的含量。
中钴的含量。(6)原理:利用
 将KI氧化成
将KI氧化成 ,
, 被还原为
被还原为 。然后用淀粉溶液作指示剂,0.015
。然后用淀粉溶液作指示剂,0.015
 标准溶液滴定生成的
标准溶液滴定生成的 ,
, 转化为
转化为 。若称取样品的质量为0.27g,滴定
。若称取样品的质量为0.27g,滴定 时,达到终点消耗
时,达到终点消耗 标准溶液的平均体积为54.00mL。滴定终点的现象为
标准溶液的平均体积为54.00mL。滴定终点的现象为
您最近一年使用:0次
2023-10-22更新
|
672次组卷
|
4卷引用:福建省福州延安中学2023-2024学年高三上学期期中考试化学试题
福建省福州延安中学2023-2024学年高三上学期期中考试化学试题广东省广州市天河区2023-2024学年高三上学期10月份调研化学试题(已下线)实验探究题(已下线)题型四 以无机物制备为载体的综合实验-备战2024年高考化学答题技巧与模板构建



