1 . 根据下列实验操作和现象所得到的结论正确 的是。
| 选项 | 实验操作和现象 | 结论 |
| A | 向试管中加入2mL 5%  溶液,再滴加数滴10% NaOH溶液,振荡后加入某物质,加热,没有砖红色沉淀生成。 溶液,再滴加数滴10% NaOH溶液,振荡后加入某物质,加热,没有砖红色沉淀生成。 | 该物质中不存在醛基 |
| B | 向淀粉溶液中加适量20%  溶液,加热,冷却后加NaOH溶液至中性,再滴加少量碘水,溶液变蓝 溶液,加热,冷却后加NaOH溶液至中性,再滴加少量碘水,溶液变蓝 | 淀粉未水解 |
| C | 取少量 样品溶于蒸馏水,加入足量稀盐酸,再加入足量 样品溶于蒸馏水,加入足量稀盐酸,再加入足量 溶液,若有白色沉淀产生。 溶液,若有白色沉淀产生。 | 则该 样品已经变质 样品已经变质 |
| D | 向 溶液中滴加 溶液中滴加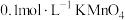 溶液,溶液褪色 溶液,溶液褪色 |  具有氧化性 具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-06-27更新
|
187次组卷
|
2卷引用:浙江省温州新力量联盟2021-2022学年高二下学期期末联考化学试题
解题方法
2 . 某学习小组在实验室中利用如图装置(夹持装置略去)测定某铁硫化物(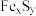 )的组成,并探究反应后D装置所得溶液中含硫化合物的组成。
)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。
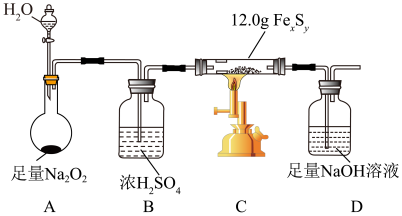
实验步骤:
步骤I
如图连接装置,检查装置气密性,装入试剂;
步骤II
旋开分液漏斗活塞与旋塞,并点燃酒精喷灯;
步骤III
足够长时间后,D中产生气泡速率变快时,停止加热,继续向烧瓶中滴水一段时间;
步骤IV
实验结束后,将D中所得溶液加水配制成250mL溶液;
请回答:
(1)写出A中发生反应的离子方程式_______ 。
(2)有同学认为D中应设置防倒吸装置,你认为是否有必要?_______ (填“是”或“否”),说明理由_______ 。
(3)在步骤IV所得溶液的主要溶质为_______ ,检验溶液中存在 的方法是
的方法是_______ 。
(4)取25.00mL步骤IV中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的 溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66g。写出
溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66g。写出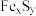 的与
的与 反应的化学方程式
反应的化学方程式_______ 。
(5)若步骤D配制溶液时俯视容量瓶的刻度线,则测得铁硫化物的x:y的值_______ (填“偏大”、“不影响”或“偏小”)
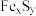 )的组成,并探究反应后D装置所得溶液中含硫化合物的组成。
)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。
实验步骤:
步骤I
如图连接装置,检查装置气密性,装入试剂;
步骤II
旋开分液漏斗活塞与旋塞,并点燃酒精喷灯;
步骤III
足够长时间后,D中产生气泡速率变快时,停止加热,继续向烧瓶中滴水一段时间;
步骤IV
实验结束后,将D中所得溶液加水配制成250mL溶液;
请回答:
(1)写出A中发生反应的离子方程式
(2)有同学认为D中应设置防倒吸装置,你认为是否有必要?
(3)在步骤IV所得溶液的主要溶质为
 的方法是
的方法是(4)取25.00mL步骤IV中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的
 溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66g。写出
溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66g。写出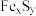 的与
的与 反应的化学方程式
反应的化学方程式(5)若步骤D配制溶液时俯视容量瓶的刻度线,则测得铁硫化物的x:y的值
您最近一年使用:0次
2022-06-26更新
|
227次组卷
|
2卷引用:浙江省宁波市九校2021-2022学年高一下学期6月联考化学试题
3 . 下列关于实验操作、现象及结论均正确的是
实验 | 操作 | 现象 | 结论 |
A | 向硫酸酸化的 溶液中加入 溶液中加入 溶液,再滴加 溶液,再滴加 溶液 溶液 | 产生白色沉淀 |  将 将 氧化为 氧化为 |
B | 将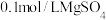 溶液滴入NaOH溶液中至不再有沉淀产生,再滴加 溶液滴入NaOH溶液中至不再有沉淀产生,再滴加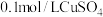 溶液 溶液 | 白色沉淀变为蓝色沉淀 | 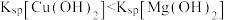 |
C | 在淀粉溶液中加入稀硫酸,水浴加热一段时间,冷却后再加入新制 浊液并煮沸 浊液并煮沸 | 生成砖红色沉淀 | 淀粉在酸性条件下可以水解,产物中有葡萄糖 |
D | 用玻璃棒蘸取某无色溶液进行焰色试验 | 焰色呈黄色 | 溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 根据实验操作和现象得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向某溶液中滴加Ba(NO3)2溶液,再滴加足量的稀硝酸,有白色沉淀产生 | 该溶液中一定含有SO |
| B | 在某待检盐溶液中,滴加NaOH溶液,加热,用湿润的红色石蕊试纸检验产生的气体,试纸变蓝色 | 某待检盐中含有NH |
| C | 将乙烯分别通入酸性KMnO4溶液和Br2的四氯化碳溶液中,两种溶液均褪色 | 均发生了氧化反应 |
| D | 将气体X通入品红溶液中,品红褪色 | 气体X一定是SO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 下列方案设计、现象、解释或结论有错误的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 摘下几根火柴头浸于水中,一定时间后取适量溶液于试管中,加 溶液、稀硝酸和 溶液、稀硝酸和 溶液。 溶液。 | 出现白色沉淀 | 火柴头含有氯元素 |
| B | 向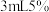 的 的 溶液中加入几滴 溶液中加入几滴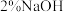 溶液,制得新制 溶液,制得新制 然后加入适量牙膏 然后加入适量牙膏 | 绛蓝色溶液 | 牙膏中存在甘油 |
| C | 将石蜡油与碎瓷片混合加强热,产生的气体通入酸性重铬酸钾钾溶液中 | 酸性重铬酸钾溶液褪色 | 石蜡油加强热产生的气体是不饱和烃 |
| D | 取 溶液于试管中,滴加 溶液于试管中,滴加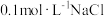 溶液,待不再出现白色沉淀后,再滴加 溶液,待不再出现白色沉淀后,再滴加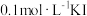 溶液 溶液 | 白色沉淀转化为黄色沉淀 |  溶解度大于 溶解度大于 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 下列叙述正确的是
| A.金属钠着火时,可用水去灭火 |
| B.将一小块钠投入CuSO4溶液中可置换出红色的固体 |
| C.向某待测溶液中加入足量盐酸酸化,再加入AgNO3溶液,产生白色沉淀,说明待测溶液中含Cl- |
| D.Na2O与Na2O2中阳、阴离子的个数比均为2:1 |
您最近一年使用:0次
2022-10-13更新
|
183次组卷
|
4卷引用:高中化学-高一上-13
7 . 下列有关实验的操作、现象以及得出的解释或结论均正确的是
| 选项 | 操作 | 现象 | 解释或结论 |
| A | 向溶液中加入NaOH溶液,然后加热,并用湿润的蓝色石蕊试纸检验产生的气体 | 试纸不变红色 | 溶液中不含有 |
| B | 向某溶液中逐滴加入盐酸 | 立即产生无色无味的气体,该气体能使澄清石灰水变浑浊 | 溶液中一定含有大量的 |
| C | 向某溶液中加入盐酸,再加入 溶液 溶液 | 加入盐酸后无明显现象,再加入 溶液,产生白色沉淀 溶液,产生白色沉淀 | 溶液中一定有 |
| D | 将固体试样完全溶于盐酸,再滴加KSCN溶液 | 不变红色 | 该固体试样中不存在 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 下列实验方案设计中,能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 检验溶液中的S | 向溶液中加入盐酸酸化的氯化钡溶液,观察是否产生白色沉淀 |
| B | 探究浓度对化学平衡的影响 | 向5 mL含0.0025 mol·L-1 FeCl3和0.005 mol·L-1 KSCN的混合溶液加4滴饱和FeCl3溶液,观察溶液颜色变化 |
| C | 提纯混有少量硝酸钾的氯化钠固体 | 在较高温度下制得浓溶液再冷却结晶、过滤、洗涤、干燥 |
| D | 探究蔗糖水解产物的还原性 | 在蔗糖中加入稀硫酸,水浴加热,再加入新制氢氧化铜悬浊液并加热,观察是否产生砖红色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 化合物A由4种元素组成,实验如下:
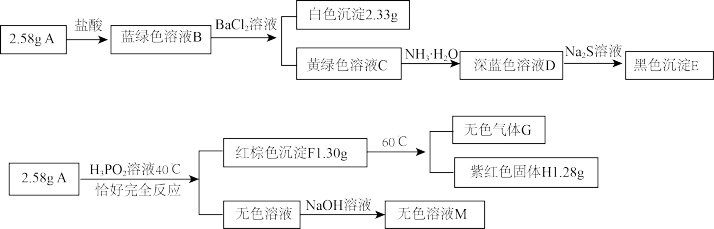
已知:除说明外,加入试剂均为足量;生成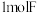 时消耗
时消耗 的
的
回答下列问题:
(1) 的分子式为
的分子式为_______ , 的化学式为
的化学式为_______ 。
(2)溶液B中溶质成分是_______ (用化学式表示),根据 的现象,给出相应微粒与阳离子结合由强到弱的排序
的现象,给出相应微粒与阳离子结合由强到弱的排序_______ 。
(3)写出 与
与 反应的化学方程式
反应的化学方程式_______ 。
(4)检验溶液 的主要阴离子(任选2种)
的主要阴离子(任选2种)_______ 。

已知:除说明外,加入试剂均为足量;生成
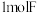 时消耗
时消耗 的
的
回答下列问题:
(1)
 的分子式为
的分子式为 的化学式为
的化学式为(2)溶液B中溶质成分是
 的现象,给出相应微粒与阳离子结合由强到弱的排序
的现象,给出相应微粒与阳离子结合由强到弱的排序(3)写出
 与
与 反应的化学方程式
反应的化学方程式(4)检验溶液
 的主要阴离子(任选2种)
的主要阴离子(任选2种)
您最近一年使用:0次
10 . 化合物X是由三种主族元素组成的液体物质,某兴趣小组对化合物X开展探究实验。

已知:①X遇水反应剧烈,产生白雾;
②气体A和气体B是纯净物;
③ 为不溶于水的白色沉淀。
为不溶于水的白色沉淀。
请回答:
(1)写出气体A的化学式___________ ,组成X的三种元素___________ (填元素符号)
(2)写出X与水反应的化学方程式是___________
(3)将A通入到还原性气体Y的水溶液中,生成一种淡黄色沉淀。则Y、A、 三种微粒还原性由强到弱的顺序为
三种微粒还原性由强到弱的顺序为___________ (用化学式表示)。
(4)用硫磺(用S表示)、液氯和三氧化硫为原料,在一定条件下合成X,如果总原子利用率最大化(即期望产物的总质量与生成物的总质量之比),则相对应的三种物质的物质的量之比为___________ 。
(5)将气体A和B通入足量的氢氧化钠溶液中,充分反应,请设计实验方案,检验所得溶液中的阴离子(不考虑水解和溶液中的 )
)___________ 。

已知:①X遇水反应剧烈,产生白雾;
②气体A和气体B是纯净物;
③
 为不溶于水的白色沉淀。
为不溶于水的白色沉淀。请回答:
(1)写出气体A的化学式
(2)写出X与水反应的化学方程式是
(3)将A通入到还原性气体Y的水溶液中,生成一种淡黄色沉淀。则Y、A、
 三种微粒还原性由强到弱的顺序为
三种微粒还原性由强到弱的顺序为(4)用硫磺(用S表示)、液氯和三氧化硫为原料,在一定条件下合成X,如果总原子利用率最大化(即期望产物的总质量与生成物的总质量之比),则相对应的三种物质的物质的量之比为
(5)将气体A和B通入足量的氢氧化钠溶液中,充分反应,请设计实验方案,检验所得溶液中的阴离子(不考虑水解和溶液中的
 )
)
您最近一年使用:0次



