1 . 某化学兴趣小组对有关SO2性质进行如下探究活动。_______ ,装置A中发生反应的化学方程式为_______ ,该反应属于_______ 反应。
(2)B中品红溶液褪色,是因为SO2具有______ (填“氧化”“还原”或“漂白”,下同)性,C装置中酸性KMnO4溶液褪色,表明SO2具有_______ 性,除此之外SO2还有一种性质, 请写出一个能表现该性质的化学方程式_______ 。
(3)证明亚硫酸酸性比碳酸酸性强的实验现象是_______ 。
(4)若将SO2气体直接通入澄清石灰水中,溶液变浑浊,则该反应的离子方程式为_______ ,说明SO2是_______ 氧化物。
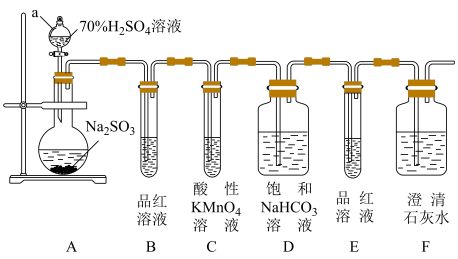
(2)B中品红溶液褪色,是因为SO2具有
(3)证明亚硫酸酸性比碳酸酸性强的实验现象是
(4)若将SO2气体直接通入澄清石灰水中,溶液变浑浊,则该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
2 . 连四硫酸钠( )是生物酶、生物键的修复剂,其与盐酸反应的离子方程式为:
)是生物酶、生物键的修复剂,其与盐酸反应的离子方程式为: ,按如下装置制备足量
,按如下装置制备足量 并探究其性质。下列表述不正确的是
并探究其性质。下列表述不正确的是
 )是生物酶、生物键的修复剂,其与盐酸反应的离子方程式为:
)是生物酶、生物键的修复剂,其与盐酸反应的离子方程式为: ,按如下装置制备足量
,按如下装置制备足量 并探究其性质。下列表述不正确的是
并探究其性质。下列表述不正确的是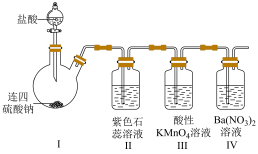
| A.Ⅱ中溶液由紫色变成红色 |
B.Ⅲ中溶液褪色说明 有还原性 有还原性 |
| C.Ⅳ中溶液无明显变化 |
| D.基于环保,本实验应连接尾气处理装置 |
您最近一年使用:0次
2024-03-15更新
|
867次组卷
|
5卷引用:陕西省西安市航天中学2023-2024学年高一下学期第一次月考化学试题
名校
解题方法
3 . 下列装置所示的实验,能达到相应实验目的的是
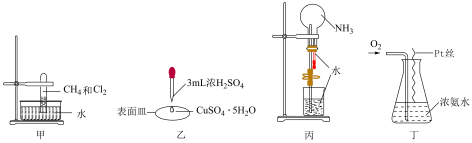

| A.甲可以验证甲烷和氯气能发生反应 | B.乙可以探究浓硫酸的脱水性 |
| C.丙可以进行喷泉实验 | D.丁可以验证氨气的还原性 |
您最近一年使用:0次
名校
解题方法
4 . 化合物(YW4)2X2Z4·W2Z为无色柱状晶体,受热易分解,已知W、X、Y、Z的原子序数依次增大,其和为22,X、Y、Z为同一周期相邻元素。可利用下图装置检验该化合物分解出的相同元素组成的不同产物。
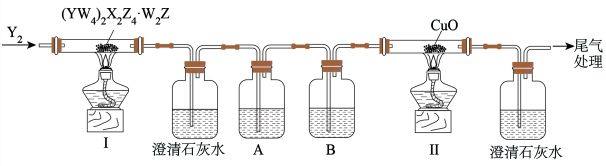
| A.(YW4)2X2Z4的物质类别为正盐 |
| B.装置B中盛装的试剂是氢氧化钠溶液 |
| C.反应开始前通入Y2,可以避免装置中的空气干扰产物的检验 |
| D.装置中两处澄清石灰水都变浑浊,证明分解产物中含有两种由X、Z组成的物质 |
您最近一年使用:0次
2024-02-19更新
|
281次组卷
|
2卷引用:陕西省西安交通大学附属中学2023-2024学年高一上学期期末考试化学试卷
5 . 某学习小组探究铜跟浓硫酸的反应时,利用如图实验装置进行相关实验。
按要求填写下列空白:
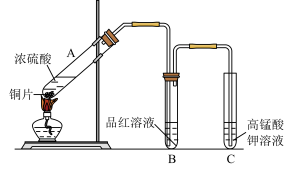
(1)装置A中发生的化学反应方程式为___________ 。
(2)实验过程中装置C中溶液褪色说明装置A中产生的气体具有___________ 性。
(3)有学生提出装置C的试管口还应放置一团浸有NaOH溶液的棉花,其目的是___________ 。
(4)实验结束拆开装置后,加热装置B的试管,观察到的现象是___________ 。
(5)根据氮及其化合物 转化关系回答下列问题:
转化关系回答下列问题:
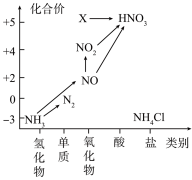
①X的化学式为___________ ,从化合价上看,X具有___________ 性(填“氧化”或“还原”)。
②写出实验制取氨气的化学方程式___________ ;
③下列试剂不能用于干燥NH3的是___________ (填字母)。
A.浓硫酸 B.碱石灰 C.NaOH固体
④NH3→NO的化学方程式为___________ 。
按要求填写下列空白:

(1)装置A中发生的化学反应方程式为
(2)实验过程中装置C中溶液褪色说明装置A中产生的气体具有
(3)有学生提出装置C的试管口还应放置一团浸有NaOH溶液的棉花,其目的是
(4)实验结束拆开装置后,加热装置B的试管,观察到的现象是
(5)根据氮及其化合物
 转化关系回答下列问题:
转化关系回答下列问题:
①X的化学式为
②写出实验制取氨气的化学方程式
③下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.NaOH固体
④NH3→NO的化学方程式为
您最近一年使用:0次
6 . 元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。
Ⅰ.如图是元素周期表的一部分,回答下列问题:
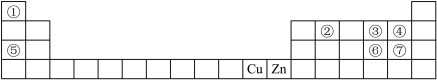
(1)①~⑦号元素中原子半径最大的是___________ (填元素符号),其最高价氧化物对应的水化物中含有的化学键是___________ 。该元素的单质与氧气在加热条件下反应生成R,用电子式表示R的形成过程___________ 。
(2)①~⑦号元素的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式,下同),碱性最强的是___________ 。
(3)将锌片、铜片用导线连接后浸入⑥的最高价氧化物对应水化物的稀溶液中,构成了原电池,则负极的电极反应式是___________ 。一段时间后,若锌片的质量减少了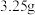 ,则导线中通过电子
,则导线中通过电子___________  。
。
Ⅱ.某小组为探究 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
(4)实验①可得出氧化性强弱:___________ 。
(5)实验②观察到的现象是___________ ,甲同学根据此现象得出结论:氧化性 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,他补做了实验③。
,他补做了实验③。
补做实验③的目的是___________ 。
Ⅰ.如图是元素周期表的一部分,回答下列问题:

(1)①~⑦号元素中原子半径最大的是
(2)①~⑦号元素的最高价氧化物对应的水化物中,酸性最强的是
(3)将锌片、铜片用导线连接后浸入⑥的最高价氧化物对应水化物的稀溶液中,构成了原电池,则负极的电极反应式是
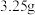 ,则导线中通过电子
,则导线中通过电子 。
。Ⅱ.某小组为探究
 的氧化性强弱,设计实验如下:
的氧化性强弱,设计实验如下:资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
| 序号 | 实验① | 实验② |
| 实验操作 | 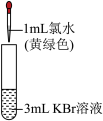 | 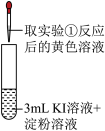 |
| 现象 | 溶液变为黄色 |
(5)实验②观察到的现象是
 。乙同学认为实验②不能充分证明氧化性
。乙同学认为实验②不能充分证明氧化性 ,他补做了实验③。
,他补做了实验③。| 实验③ | 另取实验①反应后的黄色溶液少许,先加入足量的 固体,充分振荡,然后加入 固体,充分振荡,然后加入 溶液和淀粉溶液。 溶液和淀粉溶液。 |
您最近一年使用:0次
7 . 氨是一种重要的化工原料,在工农业生产中有广泛的应用
Ⅰ.工业合成氨的反应为: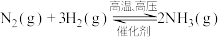 。
。
(1)合成氨的微观历程示意图如下, 过程需要
过程需要___________ (填“吸收”或“放出”)能量。
 、
、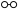 、
、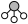 、
、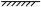 分别表示
分别表示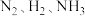 、催化剂)
、催化剂)

(2)工业上可用天然气来制取合成氨的原料气氢气,发生的反应为: 。在一定温度下,体积为
。在一定温度下,体积为 的恒容密闭容器中测得如表所示数据。
的恒容密闭容器中测得如表所示数据。
分析表中数据,判断 时反应是否处于平衡状态?
时反应是否处于平衡状态?___________ (填“是”或“否”)。 内,用
内,用 的浓度变化表示的平均反应速率为
的浓度变化表示的平均反应速率为___________  。
。
Ⅱ.实验小组为探究氨与二氧化氮的反应,设计如图实验装置:
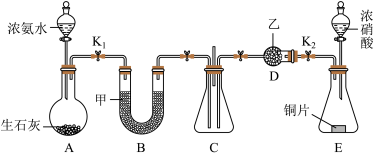
(3)装置A中生石灰的作用是___________ 实验室也常用氯化铵和氢氧化钙混合固体制取氨气,写出发生反应的化学方程式___________ 。
(4)装置B和D的作用都是干燥气体,其中盛装的干燥剂选择合理的是___________ (填字母)。
a.甲、乙都是碱石灰 b.甲、乙都是无水氯化钙
c.甲是碱石灰,乙是五氧化二磷 d.甲是浓硫酸,乙是碱石灰
(5)若氨气与二氧化氮反应生成的产物为水和氮气,则C中发生反应的化学方程式为___________ 。
(6)该实验设计中存在着一个很严重的缺陷是___________ 。
(7)取 铜于装置
铜于装置 的锥形瓶中,再加入
的锥形瓶中,再加入 一定浓度的浓硝酸,充分反应后铜全部溶解,收集到
一定浓度的浓硝酸,充分反应后铜全部溶解,收集到 和
和 的混合气体
的混合气体 (标准状况),则
(标准状况),则
___________ 。
Ⅰ.工业合成氨的反应为:
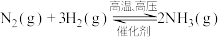 。
。(1)合成氨的微观历程示意图如下,
 过程需要
过程需要 、
、 、
、 、
、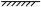 分别表示
分别表示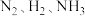 、催化剂)
、催化剂)
(2)工业上可用天然气来制取合成氨的原料气氢气,发生的反应为:
 。在一定温度下,体积为
。在一定温度下,体积为 的恒容密闭容器中测得如表所示数据。
的恒容密闭容器中测得如表所示数据。时间 |  |  |  |  |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 |  | 0.80 |  | 0.60 |
| 7 | 0.20 | 0.80 | 0.20 | 0.60 |
 时反应是否处于平衡状态?
时反应是否处于平衡状态?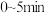 内,用
内,用 的浓度变化表示的平均反应速率为
的浓度变化表示的平均反应速率为 。
。Ⅱ.实验小组为探究氨与二氧化氮的反应,设计如图实验装置:

(3)装置A中生石灰的作用是
(4)装置B和D的作用都是干燥气体,其中盛装的干燥剂选择合理的是
a.甲、乙都是碱石灰 b.甲、乙都是无水氯化钙
c.甲是碱石灰,乙是五氧化二磷 d.甲是浓硫酸,乙是碱石灰
(5)若氨气与二氧化氮反应生成的产物为水和氮气,则C中发生反应的化学方程式为
(6)该实验设计中存在着一个很严重的缺陷是
(7)取
 铜于装置
铜于装置 的锥形瓶中,再加入
的锥形瓶中,再加入 一定浓度的浓硝酸,充分反应后铜全部溶解,收集到
一定浓度的浓硝酸,充分反应后铜全部溶解,收集到 和
和 的混合气体
的混合气体 (标准状况),则
(标准状况),则
您最近一年使用:0次
名校
解题方法
8 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,图2装置探究其相关性质。
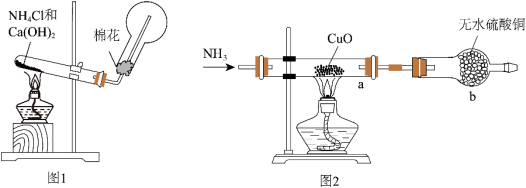
I.实验室制取氨气。
(1)图1装置中生成NH3的化学方程式为______ 。检验圆底烧瓶中已收集满氨气的方法是______ 。
II.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
(2)无水硫酸铜的作用是______ ;仪器b的名称为______ ;有同学认为需要在无水硫酸铜的后面再接一个装有CaCl2固体的球形干燥管,这样做的目的是______ 。
(3)实验中观察到a中CuO粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为______ 。
(4)若a中消耗标准状况下3.36L的氨气,理论得到铜的质量为______ g。

I.实验室制取氨气。
(1)图1装置中生成NH3的化学方程式为
II.探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。
(2)无水硫酸铜的作用是
(3)实验中观察到a中CuO粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
(4)若a中消耗标准状况下3.36L的氨气,理论得到铜的质量为
您最近一年使用:0次
2023-05-11更新
|
508次组卷
|
2卷引用:陕西省西安市第八十五中学2022-2023学年高一下学期期中考试化学试题
名校
解题方法
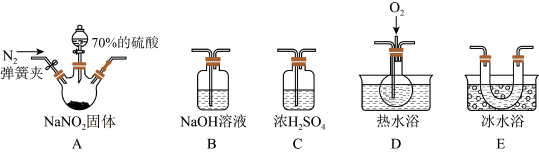
9 . 亚硝酸钠(NaNO2)在纤维纺织品的染色和漂白、照相、生产橡胶、制药等领域有广泛应用,也常用于鱼类、肉类等食品的染色和防腐。但因其有毒,所以在食品行业中的用量有严格限制。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应及气体产物的成分。
已知:①NO+NO2+2OH-=2 +H2O;
+H2O;
②气体液化的温度:NO2为21℃,NO为-152℃。___________ 、___________ 、B。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是___________ 。
(3)在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是___________ ;
②装置E的作用是___________ 。
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为___________ 。
(5)通过上述实验探究过程,可得出装置A中反应的化学方程式是___________ 。
已知:①NO+NO2+2OH-=2
 +H2O;
+H2O;②气体液化的温度:NO2为21℃,NO为-152℃。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是
(3)在关闭弹簧夹、打开分液漏斗活塞、滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体含有NO,依据的现象是
②装置E的作用是
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为
(5)通过上述实验探究过程,可得出装置A中反应的化学方程式是
您最近一年使用:0次
2023-05-11更新
|
806次组卷
|
6卷引用:陕西省西安市第一中学2022-2023学年高一下学期5月月考化学试题
陕西省西安市第一中学2022-2023学年高一下学期5月月考化学试题江西省宜春市上高中学2022-2023学年高一下学期7月期末考试化学试题湖南师大附中博才实验中学2022-2023年高一下学期期末考试化学试题广西柳州铁一中学2023-2024学年高一上学期期末考试化学试卷 (已下线)重难点02 常见物质的制取与性质探究-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)广西南宁市第八中学2023-2024学年高二上学期开学考化学试题
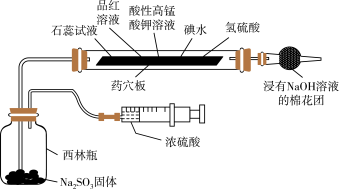
10 . 某小组为验证 的性质设计如图所示的实验装置,下列说法错误的是
的性质设计如图所示的实验装置,下列说法错误的是
 的性质设计如图所示的实验装置,下列说法错误的是
的性质设计如图所示的实验装置,下列说法错误的是
| A.该装置能体现实验的微型化和绿色化 |
B.一段时间后氢硫酸溶液中有淡黄色沉淀生成,说明 有氧化性 有氧化性 |
C.一段时间后石蕊试液和品红溶液均褪色,说明 有漂白性 有漂白性 |
D.一段时间后酸性高锰酸钾溶液、碘水褪色,说明 有还原性 有还原性 |
您最近一年使用:0次



