1 . 亚硫酸钠(Na2SO3)是一种重要的化工产品,常用作防腐剂、漂白剂、脱氯剂等。为探究 Na2SO3的性质,进行了如下实验。
【性质预测】
(1)Na2SO3中硫元素的化合价是_______ ,属于S元素的中间价态,既具有氧化性,又具有还原性。
【实验验证】
资料:酸性条件下,KMnO4 被还原为无色的 Mn2+。
【分析解释】
(2)实验ⅰ中,反应的离子方程式是_______ 。
(3)实验ⅱ中,能说明 Na2S 在酸性条件下被氧化的实验现象是_______ 。
【继续探究】
(4)甲同学认为实验ⅱ的现象不能直接得出“Na2SO3 具有氧化性”。
①对淡黄色浑浊产生的原因作出如下假设:
假设 a:酸性溶液中的 SO 具有氧化性,可产生 S;
具有氧化性,可产生 S;
假设 b:空气中存在 O2,在酸性条件下,由于_______ (用离子方程式表示),可产生 S;
假设 c:酸性溶液中的 SO 具有氧化性,可产生 S。
具有氧化性,可产生 S。
②设计实验 iii 证实了假设 a和b不是产生 S 的主要原因。
实验 iii:向 Na2S溶液中加入_______ (填试剂名称),产生有臭鸡蛋气味的气体,离子方程式为_______ ,溶液未变浑浊。
(5)结合实验 ii 和 iii,用离子方程式解释实验ⅱ中产生淡黄色浑浊的原因:_______ 。
【性质预测】
(1)Na2SO3中硫元素的化合价是
【实验验证】
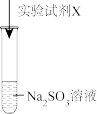 | 实验序号 | 实验试剂X | 实验现象 |
| ⅰ | KMnO4溶液、稀硫酸 | 紫色褪去,变为无色 | |
| ⅱ | Na2S 溶液、稀硫酸 | 加入Na2S溶液,无明显现象;再加入稀硫酸,产生淡黄色浑浊。 |
【分析解释】
(2)实验ⅰ中,反应的离子方程式是
(3)实验ⅱ中,能说明 Na2S 在酸性条件下被氧化的实验现象是
【继续探究】
(4)甲同学认为实验ⅱ的现象不能直接得出“Na2SO3 具有氧化性”。
①对淡黄色浑浊产生的原因作出如下假设:
假设 a:酸性溶液中的 SO
 具有氧化性,可产生 S;
具有氧化性,可产生 S;假设 b:空气中存在 O2,在酸性条件下,由于
假设 c:酸性溶液中的 SO
 具有氧化性,可产生 S。
具有氧化性,可产生 S。②设计实验 iii 证实了假设 a和b不是产生 S 的主要原因。
实验 iii:向 Na2S溶液中加入
(5)结合实验 ii 和 iii,用离子方程式解释实验ⅱ中产生淡黄色浑浊的原因:
您最近一年使用:0次
2 . 亚硫酸钠(Na2SO3)是一种重要的化工产品,常用作防腐剂、漂白剂、脱氯剂等。为探究 Na2SO3的性质,进行了如下实验。
【性质预测】
(1)Na2SO3中硫元素的化合价是_____ ,属于 S 元素的中间价态,既具有氧化性,又具有还原性。
【实验验证】
资料:酸性条件下,KMnO4被还原为无色的 Mn2+。
【分析解释】
(2)实验ⅰ中,反应的离子方程式是___________ 。
(3)实验ⅱ中,能说明 Na2S 在酸性条件下被氧化的实验现象是___________ 。
【继续探究】
(4)甲同学认为实验ⅱ的现象不能直接得出“Na2SO3具有氧化性”。
①对淡黄色浑浊产生的原因作出如下假设:
假设 a:酸性溶液中的 SO 具有氧化性,可产生 S;
具有氧化性,可产生 S;
假设 b:空气中存在 O2,在酸性条件下,由于___________ (用离子方程式表示),可产生 S;
假设 c:酸性溶液中的 SO 具有氧化性,可产生 S。
具有氧化性,可产生 S。
②设计实验 iii 证实了假设 a 和 b 不是产生 S 的主要原因。
实验 iii:向 Na2S 溶液中加入___________ (填试剂),产生有臭鸡蛋气味的气体,溶液未变浑浊。
(5)结合实验 ii 和 iii,用离子方程式解释实验ⅱ中产生淡黄色浑浊的原因:_______
【性质预测】
(1)Na2SO3中硫元素的化合价是
【实验验证】
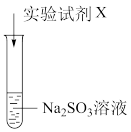 | 实验序号 | 实验试剂X | 实验现象 |
| ⅰ | KMnO4溶液、稀硫酸 | 紫色褪去,变为无色 | |
| ⅱ | Na2S 溶液、稀硫酸 | 加入Na2S溶液,无明显现象;再加入稀硫酸,产生淡黄色浑浊 |
【分析解释】
(2)实验ⅰ中,反应的离子方程式是
(3)实验ⅱ中,能说明 Na2S 在酸性条件下被氧化的实验现象是
【继续探究】
(4)甲同学认为实验ⅱ的现象不能直接得出“Na2SO3具有氧化性”。
①对淡黄色浑浊产生的原因作出如下假设:
假设 a:酸性溶液中的 SO
 具有氧化性,可产生 S;
具有氧化性,可产生 S;假设 b:空气中存在 O2,在酸性条件下,由于
假设 c:酸性溶液中的 SO
 具有氧化性,可产生 S。
具有氧化性,可产生 S。②设计实验 iii 证实了假设 a 和 b 不是产生 S 的主要原因。
实验 iii:向 Na2S 溶液中加入
(5)结合实验 ii 和 iii,用离子方程式解释实验ⅱ中产生淡黄色浑浊的原因:
您最近一年使用:0次
2021-02-01更新
|
1110次组卷
|
4卷引用:甘肃省兰州第一中学2021-2022学年高一下学期4月月考化学试题
名校
解题方法
3 . 化学是以实验为基础的学科。下列根据实验操作和现象能得到相应结论的是
| 选项 | 实验操作和现象 | 结论 |
| A | 常温下,将两块相同的未经打磨的铝片分别投入5.0mL饱和的 溶液和 溶液和 溶液中,前者无明显现象,后者迅速反应,现象明显 溶液中,前者无明显现象,后者迅速反应,现象明显 |  能加速破坏铝片表面的氧化膜 能加速破坏铝片表面的氧化膜 |
| B | 常温下,向 溶液中加入 溶液中加入 溶液,将带火星的木条放在试管口,木条复燃 溶液,将带火星的木条放在试管口,木条复燃 | 氧化性: |
| C | 向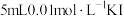 溶液中加入 溶液中加入 溶液(pH=1),溶液呈棕黄色,再滴加几滴KSCN溶液,溶液变为红色 溶液(pH=1),溶液呈棕黄色,再滴加几滴KSCN溶液,溶液变为红色 |  和 和 的反应存在限度 的反应存在限度 |
| D | 将浓盐酸和亚硫酸钠反应产生的气体通入酸性 溶液中,溶液紫红色褪去 溶液中,溶液紫红色褪去 |  具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-27更新
|
492次组卷
|
6卷引用:选择题6-10
4 . 浓硫酸分别和三种钠盐反应,下列分析正确的是
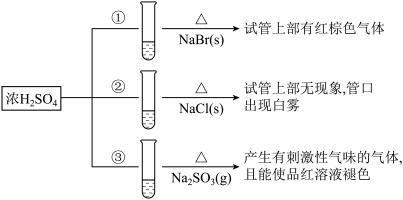
| A.对比①和②可以说明还原性Br->Cl- |
| B.①和③相比可说明氧化性Br2>SO2 |
| C.②中试管口白雾是HCl遇水蒸气所致,说明酸性H2SO4>HCl |
| D.③中浓H2SO4被还原成SO2 |
您最近一年使用:0次
2020-11-07更新
|
1201次组卷
|
33卷引用:2016-2017学年甘肃省天水市第一中学高一下学期第一阶段考试化学试卷
2016-2017学年甘肃省天水市第一中学高一下学期第一阶段考试化学试卷上海市徐汇区2018届高三化学二模试卷(已下线)2019年8月19日《每日一题》2020年高考一轮复习—— 浓硫酸的性质山西大学附中2020届高三上学期第二次模块诊断化学试题安徽省怀宁中学2020届高三上学期第二次月考化学试题夯基提能2020届高三化学选择题对题专练——氧化还原反应的基本概念(基础过关)山东省淄博市2020届高三下学期第二次网考化学试题山东省济宁市汶上圣泽中学2019-2020学年高一下学期第二次月考化学试题北京首都师范大学第二附属中学2021届高三9月月考化学试题专题4 第一单元 第2课时硫酸的制备与性质-高中化学苏教2019版必修第一册(已下线)5.1.3 不同价态含硫物质的转化(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)广东省汕头市金山中学2021届高三下学期学科素养测试化学试题辽宁省大连市普兰店区第三十八中学2020-2021学年高一下学期第一次考试化学试题河北省承德市隆化县存瑞中学2020-2021学年高二下学期期末联考化学试题(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)黑龙江省双鸭山市第一中学2020-2021学年高一下学期第一次月考化学试题新疆哈密市第十五中学2021-2022学年高三上学期第一次月考化学试题山东省泰安市2021-2022年高三上学期期中统考化学试题山东省泰安市2022届高三上学期期中考试化学试题(已下线)4.1.2 硫酸的工业制备 浓硫酸的性质(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)上海外国语大学附属浦东外国语学校2021-2022学年高一下学期线上诊断化学试题黑龙江省七台河市勃利县高级中学2021-2022学年高一下学期期中考试化学试题上海市川沙中学2020-2021学年高一下学期期中线上测试化学试题广州大学附属中学2021-2022学年高一下学期5月月考化学试题(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)3.1.2 浓硫酸和硫酸盐-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)河南省安阳市第二中学2021-2022学年高一下学期第一次段考化学试题(已下线)第15讲 硫酸-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)(已下线)考点10 硫及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第4讲 浓硫酸 不同价态含硫物质的转化上海市川沙中学2023-2024学年高一下学期期中考试化学试卷 吉林省通化市辉南县第六中学2023-2024学年高一下学期3月半月考化学试卷
5 . 某化学兴趣小组为探究铜跟浓硫酸的反应,用如下图所示装置进行有关实验。
(1)装置A中发生反应的化学方程式为_________________________________________ ;
(2)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是________________ ,B中应放置的溶液是________ (填字母);
a.水 b.酸性KMnO4溶液 c.浓溴水 d.饱和NaHSO3溶液
(3)若装置C中盛有酸性KMnO4溶液,反应现象为_____________________ ,体现该气体的_____________ (填“氧化性”或“还原性”);
(4)装置D中试管口放置的棉花应浸一种溶液,这种溶液是_____________ ,其作用是___________ ;
(5)实验中,取一定质量的铜片和一定体积18 mol·L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,其原因是________ 。

(1)装置A中发生反应的化学方程式为
(2)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是
a.水 b.酸性KMnO4溶液 c.浓溴水 d.饱和NaHSO3溶液
(3)若装置C中盛有酸性KMnO4溶液,反应现象为
(4)装置D中试管口放置的棉花应浸一种溶液,这种溶液是
(5)实验中,取一定质量的铜片和一定体积18 mol·L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,其原因是
您最近一年使用:0次
名校
解题方法
6 . 向溴水中加入足量的乙醛溶液,可以看到溴水褪色,对产生该现象的原因有如下三种猜想:①溴水与乙醛发生取代反应;②由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应;③由于乙醛具有还原性,溴水将乙醛氧化为乙酸。为探究哪种猜想正确,一研究性学习小组提出了如下两种实验方案:
方案一:检验褪色后溶液的酸碱性;
方案二:测定反应前溴水中 Br2 的物质的量和反应后溶液中 Br—离子的物质的量。
(1)方案一是否可行__________ 填(“是”或“否”),理由是____________________ 。
(2)假设测得反应前溴水中 Br2 的物质的量为 amol,
若测得反应后 n(Br-)=__________ mol,则说明溴水与乙醛发生取代反应;
若测得反应后 n(Br-)=__________ mol,则说明溴水与乙醛发生加成反应;
若测得反应后 n(Br-)=__________ mol,则说明溴水将乙醛氧化为乙酸。
(3)按物质的量之比为 1︰5 配制 1000mLKBrO3-KBr 溶液,该溶液在酸性条件下完全反应可生成 0.5molBr2。取该溶液 10mL 加入足量乙醛溶液,使其褪色,然后将所得溶液稀释为 100mL,准确量取其中 10mL,加入过量的 AgNO3溶液,过滤、洗涤、干燥后称量得到固体 0.188g。若已知 CH3COOAg 易溶于水,试通过计算判断溴水与乙醛发生反应的类型为__________ (选填猜想序号)。
(4)写出上述测定过程中的三个反应的离子方程式:
①KBrO3和KBr 在酸性条件下的反应:______________________________ ;
②溴水与乙醛的反应:______________________________ ;
③测定 Br-离子含量的反应:______________________________ ;
方案一:检验褪色后溶液的酸碱性;
方案二:测定反应前溴水中 Br2 的物质的量和反应后溶液中 Br—离子的物质的量。
(1)方案一是否可行
(2)假设测得反应前溴水中 Br2 的物质的量为 amol,
若测得反应后 n(Br-)=
若测得反应后 n(Br-)=
若测得反应后 n(Br-)=
(3)按物质的量之比为 1︰5 配制 1000mLKBrO3-KBr 溶液,该溶液在酸性条件下完全反应可生成 0.5molBr2。取该溶液 10mL 加入足量乙醛溶液,使其褪色,然后将所得溶液稀释为 100mL,准确量取其中 10mL,加入过量的 AgNO3溶液,过滤、洗涤、干燥后称量得到固体 0.188g。若已知 CH3COOAg 易溶于水,试通过计算判断溴水与乙醛发生反应的类型为
(4)写出上述测定过程中的三个反应的离子方程式:
①KBrO3和KBr 在酸性条件下的反应:
②溴水与乙醛的反应:
③测定 Br-离子含量的反应:
您最近一年使用:0次
2019-01-30更新
|
324次组卷
|
3卷引用:甘肃省张掖市高台县第一中学2019-2020学年高二下学期期中考试化学试题
名校
解题方法
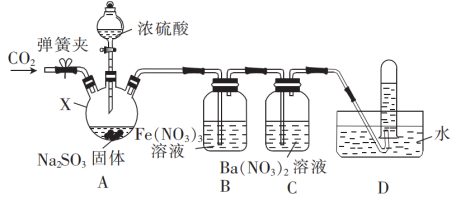
7 . 某小组设计实验探究SO2的还原性(部分夹持仪器省略)。
回答下列问题:
(1)分液漏斗中浓硫酸的浓度宜选择_______ (填标号)。
a.98.3% b.70% c.30% d.10%
(2)仪器X的名称是_______ ,装置A中发生反应的化学方程式为_______ 。
(3)为了探究装置B中 、
、 是否与SO2发生反应,设计如下实验:
是否与SO2发生反应,设计如下实验:
由操作I及其现象可知
_______ (填“部分”或“全部”,下同)参与了反应,由操作II及其现象可知
_______ 参与了反应。
(4)测定装置B溶液中 的浓度(只考虑
的浓度(只考虑 与
与 的反应)。用
的反应)。用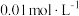 的酸性
的酸性 溶液滴定20mL装置B中溶液,共消耗酸性
溶液滴定20mL装置B中溶液,共消耗酸性 溶液16mL,则装置B溶液中
溶液16mL,则装置B溶液中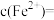
_______  。
。
(5)经分析,装置C中反应可能有两种情况:
①若通入少量SO2,则反应为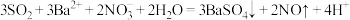 ;
;
②若通入过量SO2,则反应为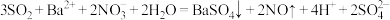 。
。
为了探究发生了哪一种情况,取装置C中溶液分别装入甲、乙、丙、丁四支试管中,进行如下实验:
能说明发生的是情况①的实验是____ (填标号,下同),能说明发生的是情况②的实验是_____ 。

回答下列问题:
(1)分液漏斗中浓硫酸的浓度宜选择
a.98.3% b.70% c.30% d.10%
(2)仪器X的名称是
(3)为了探究装置B中
 、
、 是否与SO2发生反应,设计如下实验:
是否与SO2发生反应,设计如下实验:| 实验操作 | 现象 |
| I.取装置B中溶液于试管,滴加KSCN溶液 | 溶液不变红 |
| II.取装置B中溶液于试管,加入适量浓硫酸,再加入铜粉 | 铜粉不溶解,溶液不变蓝 |
III.取装置B中溶液于试管,滴加 溶液和盐酸 溶液和盐酸 | 产生白色沉淀 |


(4)测定装置B溶液中
 的浓度(只考虑
的浓度(只考虑 与
与 的反应)。用
的反应)。用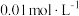 的酸性
的酸性 溶液滴定20mL装置B中溶液,共消耗酸性
溶液滴定20mL装置B中溶液,共消耗酸性 溶液16mL,则装置B溶液中
溶液16mL,则装置B溶液中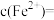
 。
。(5)经分析,装置C中反应可能有两种情况:
①若通入少量SO2,则反应为
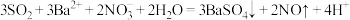 ;
;②若通入过量SO2,则反应为
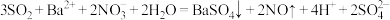 。
。为了探究发生了哪一种情况,取装置C中溶液分别装入甲、乙、丙、丁四支试管中,进行如下实验:
| 实验 | 操作及现象 |
| a | 向甲中加入锌粒,产生气泡 |
| b | 向乙中加入铜粉,溶液颜色发生了变化 |
| c | 向丙中加入 粉末,产生气泡 粉末,产生气泡 |
| d | 向丁中加入 溶液,产生沉淀 溶液,产生沉淀 |
您最近一年使用:0次
2022-07-07更新
|
345次组卷
|
4卷引用:甘肃省白银市2012-2022学年高一下学期期末考试化学试题
8 . 过二硫酸钾( )是一种白色结晶性粉末,溶于水、不溶于乙醇,具有强氧化性,加热至100℃时会完全分解。某学习小组拟探究过二硫酸钾的性质。
)是一种白色结晶性粉末,溶于水、不溶于乙醇,具有强氧化性,加热至100℃时会完全分解。某学习小组拟探究过二硫酸钾的性质。
实验(一):探究过二硫酸钾的强氧化性。
探究 溶液与
溶液与 溶液反应,实验操作与现象如下:
溶液反应,实验操作与现象如下:
(1)同学甲用碰撞理论分析,实验Ⅰ中 和
和 反应很慢的主要原因是
反应很慢的主要原因是___________
(2)同学乙猜想实验Ⅱ中 起催化作用,其总反应分两步进行:
起催化作用,其总反应分两步进行:
(ⅰ)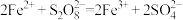 ;(ⅱ)___________。
;(ⅱ)___________。
①补充反应(ⅱ):___________ 。
②请你设计实验证明同学乙的猜想:___________ 。
(3)查阅文献知,氧化性: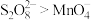 。在稀硫酸酸化的
。在稀硫酸酸化的 溶液中滴加1滴
溶液中滴加1滴 溶液作催化剂,再滴加
溶液作催化剂,再滴加 溶液,实验现象是
溶液,实验现象是___________ ,该反应的离子方程式为___________ 。
实验(二):探究过二硫酸钾的热稳定性。
已知几种气体的熔点、沸点如下表所示:
取适量的 装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D。实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。
装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D。实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。
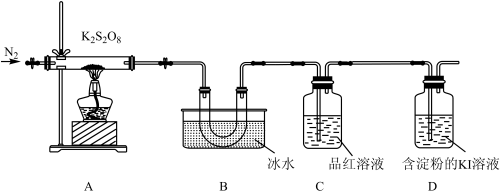
(4)加热之前,先通入一段时间 ,当观察到D中
,当观察到D中___________ (填实验现象)时点燃酒精灯。
(5)B中U形管收集的物质是___________ (填化学式)。
(6)当A中硬质玻璃管中固体完全分解,停止加热,残留的固体产物只有一种。待冷却至室温时取少量残留固体于试管,加入蒸馏水,溶解后滴加BaCl2溶液和盐酸,产生白色沉淀。A中 完全分解发生反应的化学方程式为
完全分解发生反应的化学方程式为___________ 。
 )是一种白色结晶性粉末,溶于水、不溶于乙醇,具有强氧化性,加热至100℃时会完全分解。某学习小组拟探究过二硫酸钾的性质。
)是一种白色结晶性粉末,溶于水、不溶于乙醇,具有强氧化性,加热至100℃时会完全分解。某学习小组拟探究过二硫酸钾的性质。实验(一):探究过二硫酸钾的强氧化性。
探究
 溶液与
溶液与 溶液反应,实验操作与现象如下:
溶液反应,实验操作与现象如下:| 实验 | 操作 | 现象 |
| Ⅰ | 在10L含淀粉的 的 的 溶液中滴加 溶液中滴加   溶液 溶液 | 一段时间后,溶液缓慢变蓝 |
| Ⅱ | 在 含淀粉的 含淀粉的 的 的 溶液中先滴几滴 溶液中先滴几滴 的 的 溶液,再滴加 溶液,再滴加   溶液 溶液 | 溶液迅速变蓝 |
 和
和 反应很慢的主要原因是
反应很慢的主要原因是(2)同学乙猜想实验Ⅱ中
 起催化作用,其总反应分两步进行:
起催化作用,其总反应分两步进行:(ⅰ)
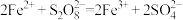 ;(ⅱ)___________。
;(ⅱ)___________。①补充反应(ⅱ):
②请你设计实验证明同学乙的猜想:
(3)查阅文献知,氧化性:
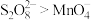 。在稀硫酸酸化的
。在稀硫酸酸化的 溶液中滴加1滴
溶液中滴加1滴 溶液作催化剂,再滴加
溶液作催化剂,再滴加 溶液,实验现象是
溶液,实验现象是实验(二):探究过二硫酸钾的热稳定性。
已知几种气体的熔点、沸点如下表所示:
| 气体 |  |  |  |
| 熔点/℃ | 16.8 | -72.7 | -218.4 |
| 沸点/℃ | 44.8 | -10 | -182.9 |
 装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D。实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。
装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D。实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。
(4)加热之前,先通入一段时间
 ,当观察到D中
,当观察到D中(5)B中U形管收集的物质是
(6)当A中硬质玻璃管中固体完全分解,停止加热,残留的固体产物只有一种。待冷却至室温时取少量残留固体于试管,加入蒸馏水,溶解后滴加BaCl2溶液和盐酸,产生白色沉淀。A中
 完全分解发生反应的化学方程式为
完全分解发生反应的化学方程式为
您最近一年使用:0次
2022-04-13更新
|
536次组卷
|
5卷引用:甘肃省平凉市2022届高三下学期第二次模拟考试理科综合化学试题
甘肃省平凉市2022届高三下学期第二次模拟考试理科综合化学试题甘肃省兰州第一中学2022-2023学年高三上学期期中考试化学试题陕西省榆林市2022届高三第二次联考化学试题(已下线)秘籍21 性质探究实验-备战2022年高考化学抢分秘籍(全国通用)热点1物质性质探究类实验
名校
9 . 请用下列装置设计一个实验,证明Cl2的氧化性比I2的氧化性强。
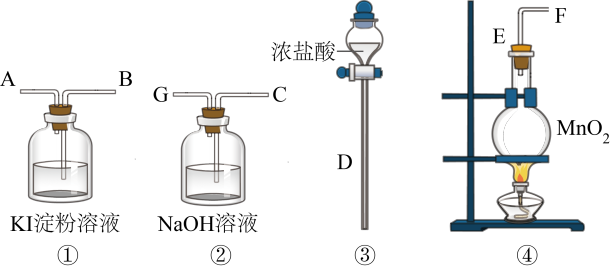
请回答下列问题:
(1)圆底烧瓶中发生反应的化学方程式为___________ 。
(2)证明Cl2比I2的氧化性强的实验现象是___________ ,反应的离子方程式是___________ 。
(3)装置②的作用是___________ 。
(4)若要证明Cl2的氧化性比Br2强,则需做的改动是___________ 。

请回答下列问题:
(1)圆底烧瓶中发生反应的化学方程式为
(2)证明Cl2比I2的氧化性强的实验现象是
(3)装置②的作用是
(4)若要证明Cl2的氧化性比Br2强,则需做的改动是
您最近一年使用:0次
10 . Na2O2可用作漂白剂和呼吸面具中的供氧剂
(1)某学习小组发现:在盛有Na2O2的试管中加入足量水,固体完全溶解,并立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞溶液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量MnO2粉末,又有气泡产生。
①写出Na2O2作供氧剂的化学反应方程式____________ ;
②使酚酞溶液变红是因为________ ,红色褪去的可能原因是___________ ;
③加入MnO2反应的化学方程式为____________ ;
(2)Na2O2有强氧化性,H2具有还原性,有同学猜想Na2O2与H2能反应。为了验证此猜想,该小组同学进行加下实验,实验步骤和现象如下:
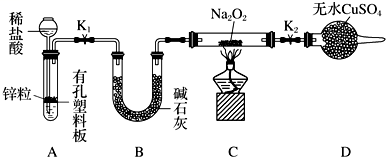
步骤1:按上图组装仪器(图中夹持仪器省略),检查气密性,装入药品。
步骤2:打开K1、K2,产生的氢气流经装有Na2O2的硬质玻璃管,一段时间后没有任何现象。
步骤3: ,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末变成了白色固体,干燥管内硫酸铜未变蓝色。
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1。
①添加稀盐酸的仪器名称是______ ,B装置的作用_________ 。
②步骤3在点燃C处酒精灯前必须进行的操作是______________ ;
③装置D的目的是_________ ;
④你得到的结论是________ (若能反应请用化学方程式表示);
⑤该实验设计中存在着明显不足之处,应该如何改进:___________ 。
(1)某学习小组发现:在盛有Na2O2的试管中加入足量水,固体完全溶解,并立即产生大量气泡,当气泡消失后,向其中滴入1~2滴酚酞溶液,溶液变红;将试管轻轻振荡,红色很快褪去;此时再向试管中加入少量MnO2粉末,又有气泡产生。
①写出Na2O2作供氧剂的化学反应方程式
②使酚酞溶液变红是因为
③加入MnO2反应的化学方程式为
(2)Na2O2有强氧化性,H2具有还原性,有同学猜想Na2O2与H2能反应。为了验证此猜想,该小组同学进行加下实验,实验步骤和现象如下:

步骤1:按上图组装仪器(图中夹持仪器省略),检查气密性,装入药品。
步骤2:打开K1、K2,产生的氢气流经装有Na2O2的硬质玻璃管,一段时间后没有任何现象。
步骤3: ,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末变成了白色固体,干燥管内硫酸铜未变蓝色。
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1。
①添加稀盐酸的仪器名称是
②步骤3在点燃C处酒精灯前必须进行的操作是
③装置D的目的是
④你得到的结论是
⑤该实验设计中存在着明显不足之处,应该如何改进:
您最近一年使用:0次
2018-05-31更新
|
816次组卷
|
3卷引用:【全国百强校】甘肃省兰州市第一中学2018-2019学年高一上学期12月月考化学试题
【全国百强校】甘肃省兰州市第一中学2018-2019学年高一上学期12月月考化学试题【全国校级联考】河北省廊坊市省级示范高中联合体2017-2018学年高二下学期第二次联考化学试题(已下线)《2018-2019学年同步单元双基双测AB卷》 第三单元 金属及其化合物单元测试 B卷



