名校
解题方法
1 . 某化学兴趣小组探究镁粉与溴水反应的原理(已知: ),做了如下四组实验:
),做了如下四组实验:
①将镁粉投入蒸馏水中,未观察到任何明显现象。
②将镁粉放入溴水中,观察到只有开始时产生极少量气泡,但溴水的颜色逐渐褪去。
③将镁粉放入液溴中,未观察到任何明显现象。
④向加入足量镁粉后的液溴中滴加几滴水,观察到溴的红棕色很快褪去。
下列关于镁粉与溴水反应的叙述错误的是
 ),做了如下四组实验:
),做了如下四组实验:①将镁粉投入蒸馏水中,未观察到任何明显现象。
②将镁粉放入溴水中,观察到只有开始时产生极少量气泡,但溴水的颜色逐渐褪去。
③将镁粉放入液溴中,未观察到任何明显现象。
④向加入足量镁粉后的液溴中滴加几滴水,观察到溴的红棕色很快褪去。
下列关于镁粉与溴水反应的叙述错误的是
| A.实验①可以说明Mg的金属性比Na弱 |
B.实验②中产生的气泡是 |
| C.实验③、④可以说明镁粉在水的催化作用下与溴反应 |
D.通过上述实验可以推测,氧化性: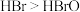 |
您最近一年使用:0次
2023-05-04更新
|
187次组卷
|
2卷引用:云南省楚雄东兴中学2023-2024学年高三上学期10月月考化学试题
2 . 某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。请回答下列问题:
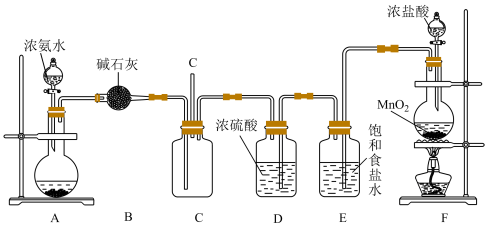
(1)E装置的作用____________________ 。
(2)写出F中发生反应的离子反应方程式_______________________________ 。
(3)上述制氨为快速制氨,实验室则常用氯化铵和氢氧化钙制备氨,其化学方程式为:_________ 。
(4)装置A的烧瓶中装有生石灰,随着浓氨水的滴入,氨气产生的原因是_________ 。
(5)通入C装置的两根导管左边较长、右边较短,目的是__________________________ 。
(6)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,当有a mol氯气参加反应时,转移的电子总数为b个,则阿伏加德罗常数为(用含a、b的代数式表示)____ mol−1。

(1)E装置的作用
(2)写出F中发生反应的离子反应方程式
(3)上述制氨为快速制氨,实验室则常用氯化铵和氢氧化钙制备氨,其化学方程式为:
(4)装置A的烧瓶中装有生石灰,随着浓氨水的滴入,氨气产生的原因是
(5)通入C装置的两根导管左边较长、右边较短,目的是
(6)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一,当有a mol氯气参加反应时,转移的电子总数为b个,则阿伏加德罗常数为(用含a、b的代数式表示)
您最近一年使用:0次
解题方法
3 . 根据如图所示装置,回答下列问题。
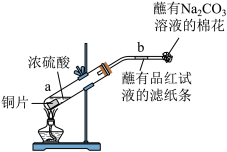
(1)开始加热后,产生的现象是:a处_______ ;b处_______ 。
(2)停止反应后,用酒精灯在b处微微加热,产生的现象是_______ 。
(3)写出a处发生反应的化学方程式:_______ 。
(4)蘸有Na2CO3溶液的棉花的作用是_______ 。
(5)实验中,取一定质量的铜片和一定体积18 mol·L-1的浓硫酸放在试管中共热,直到反应完毕,发现试管中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是_______ 。
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是_______ (填字母)。
a.铁粉 b.BaCl2溶液 c.银粉 d.NaHCO3溶液
③向反应后的溶液中加入_______ (填字母)能使Cu继续溶解。
a.KNO3溶液 b.FeCl3溶液 c.NaOH溶液 d.稀盐酸

(1)开始加热后,产生的现象是:a处
(2)停止反应后,用酒精灯在b处微微加热,产生的现象是
(3)写出a处发生反应的化学方程式:
(4)蘸有Na2CO3溶液的棉花的作用是
(5)实验中,取一定质量的铜片和一定体积18 mol·L-1的浓硫酸放在试管中共热,直到反应完毕,发现试管中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是
a.铁粉 b.BaCl2溶液 c.银粉 d.NaHCO3溶液
③向反应后的溶液中加入
a.KNO3溶液 b.FeCl3溶液 c.NaOH溶液 d.稀盐酸
您最近一年使用:0次
4 . 氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx反应进行了探究。回答下列问题:
氨与二氧化氮的反应:将收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置(部分装置已略去)进行实验。
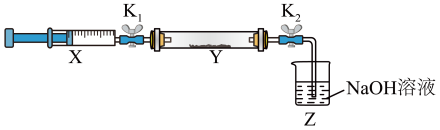
氨与二氧化氮的反应:将收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置(部分装置已略去)进行实验。

| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞使X中的气体缓慢通入Y管中 | (1)Y管中 | (2)反应的化学方程式为 |
| 将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝聚 |
| 打开K2 | (3) | (4) |
您最近一年使用:0次
5 . 某同学利用如图所示的装置,验证氨气的喷泉实验,回答下列问题:
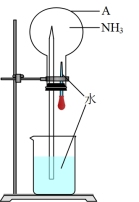
(1)仪器A的名称是____ 。
(2)写出实验室用NH4Cl和Ca(OH)2制氨气的化学方程式:____ 。
(3)喷泉实验前需要在仪器A中充满干燥的氨气。
①可用向____ (填“上”或“下”)排空气法收集氨气。
②下列物质可用于干燥氨气的是_____ (填序号)。
A.浓硫酸 B.碱石灰 C.浓硝酸

(1)仪器A的名称是
(2)写出实验室用NH4Cl和Ca(OH)2制氨气的化学方程式:
(3)喷泉实验前需要在仪器A中充满干燥的氨气。
①可用向
②下列物质可用于干燥氨气的是
A.浓硫酸 B.碱石灰 C.浓硝酸
您最近一年使用:0次
6 . 氨气在工农业生产中有重要应用。某化学小组同学利用以下装置制备氨气,并探究氨气的性质(夹持仪器略)。
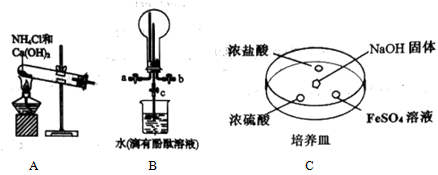
(1)实验室用装置A制备氨气的化学方程式为___________ 。
(2)用装置B收集氨气时,进气口是___________ (选填“a”或“b”)。打开装置B中的活塞c,烧瓶内产生了红色喷泉,则说明氨具有的性质是___________ ,___________ 。
(3)向C中 固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为___________ ,检验白烟中阴离子的方法是___________ 。 液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有
液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有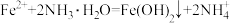 和
和___________ 。

(1)实验室用装置A制备氨气的化学方程式为
(2)用装置B收集氨气时,进气口是
(3)向C中
 固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
固体上滴几滴浓氨水,迅速盖上玻璃片,浓盐酸液滴附近会出现白烟,发生反应的化学方程式为 液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有
液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应有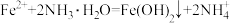 和
和
您最近一年使用:0次
7 . 应用分类的方法可以发现物质及其变化的规律,预测物质的性质及可能发生的变化。某小同学通过实验探究Na2CO3和NaHCO3的性质,请你与他们一起完成实验探究过程,并回答问题。
[观察]
(1)Na2CO3和 NaHCO3均为_______ 色的固体,
(2)从物质的类别来看, Na2CO3和NaHCO3均属于化合物中的_______ 类,能溶于水,可与部分_______ 、_______ 、盐等类别的物质发生反应。
[实验过程]
(3)实验II试管B中的现象为_______ 。
[分析与解释]
(4)实验I所得实验数据证明,溶解时吸收热量的物质是_______ 。
(5)实验II中的现象证明,Na2CO3的热稳定性_______ (填“强”或“弱”)于NaHCO3
(6)实验III中的现象证明,Na2CO3盐酸反应是分步进行的,发生反应的离子方程式为:
第一步:CO + H+=HCO
+ H+=HCO ;第二步:
;第二步:_______ 。
[观察]
(1)Na2CO3和 NaHCO3均为
(2)从物质的类别来看, Na2CO3和NaHCO3均属于化合物中的
[实验过程]
| 编号 | 实验内容 | 实验数据或者现象 |
| 实验I | 利用传感器探究两种物质分别溶水时的温度变化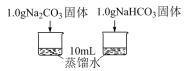 |  |
| 实验II | 探究两种物质得到热稳定性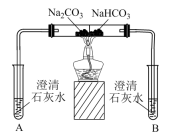 | 一段时间后,A中无明显现象,B中… |
| 实验III | 探究两种物质分别与盐酸反应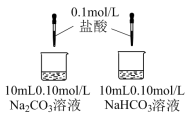 | A中开始无大量气泡,一段时间后产生大量气泡;B中立即产生大量气泡。 |
[分析与解释]
(4)实验I所得实验数据证明,溶解时吸收热量的物质是
(5)实验II中的现象证明,Na2CO3的热稳定性
(6)实验III中的现象证明,Na2CO3盐酸反应是分步进行的,发生反应的离子方程式为:
第一步:CO
 + H+=HCO
+ H+=HCO ;第二步:
;第二步:
您最近一年使用:0次
2021-07-11更新
|
661次组卷
|
5卷引用:云南省2020-2021学年高一下学期普通高中学业水平考试化学试题
名校
8 . 氨及其化合物在生产、生活中应用广泛。某同学设计实验制备氨气并探究其性质。
Ⅰ.制备氨气(选用试剂为生石灰和浓氨水),实验装置如图1所示。

(1)实验室还可用氯化铵固体和氢氧化钙固体制备氨气,该反应的化学方程式为___ 。
(2)D装置中的物质甲可能是___ (填标号),选择的理由为___ 。
①四氯化碳②四氯化碳和水③苯和水
Ⅱ.将B装置中的碱石灰换为无水氯化钙重复实验Ⅰ,以实验后的B装置中的物质为样品探究无水氯化钙吸收的气体的成分。
[提出假设]
(3)假设1:无水氯化钙只吸收水蒸气。假设2:无水氯化钙__ 。假设3:无水氯化钙吸收水蒸气和氨气。
[设计实验]
取24.9g的样品置于E装置的玻璃管中充分反应,设产生的气体全部吸收后恢复至室温,经测定F装置的总质量增加了3.6g,G装置中吸收了10.2g气体,实验装置如图2所示。
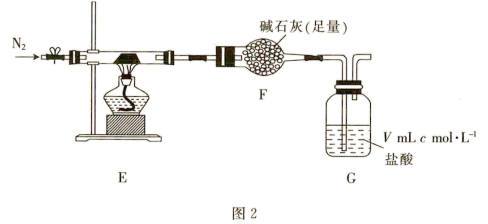
(4)根据实验结果,假设__ (填“1”、“2”或“3”)符合实验事实,那么该样品的化学式为___ (示例:CuSO4•5H2O)。
Ⅰ.制备氨气(选用试剂为生石灰和浓氨水),实验装置如图1所示。

(1)实验室还可用氯化铵固体和氢氧化钙固体制备氨气,该反应的化学方程式为
(2)D装置中的物质甲可能是
①四氯化碳②四氯化碳和水③苯和水
Ⅱ.将B装置中的碱石灰换为无水氯化钙重复实验Ⅰ,以实验后的B装置中的物质为样品探究无水氯化钙吸收的气体的成分。
[提出假设]
(3)假设1:无水氯化钙只吸收水蒸气。假设2:无水氯化钙
[设计实验]
取24.9g的样品置于E装置的玻璃管中充分反应,设产生的气体全部吸收后恢复至室温,经测定F装置的总质量增加了3.6g,G装置中吸收了10.2g气体,实验装置如图2所示。

(4)根据实验结果,假设
您最近一年使用:0次
2021-06-19更新
|
232次组卷
|
3卷引用:云南大理部分学校2020-2021学年高一下学期6月份月考化学试题
9 . 某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。

(1)实验室用装置A制备SO2.某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:___________ ;
(2)实验室用装置E制备Cl2,其反应的化学方程式为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。若有6mol的HCl参加反应,则转移的电子总数为
MnCl2+Cl2↑+2H2O。若有6mol的HCl参加反应,则转移的电子总数为___________ ;
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是B:___________ ,D:___________ ;
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:___________ 。D:___________ 。

(1)实验室用装置A制备SO2.某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:
(2)实验室用装置E制备Cl2,其反应的化学方程式为MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O。若有6mol的HCl参加反应,则转移的电子总数为
MnCl2+Cl2↑+2H2O。若有6mol的HCl参加反应,则转移的电子总数为(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是B:
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:
您最近一年使用:0次
解题方法
10 . 实验室里研究不同价态硫元素之间的转化
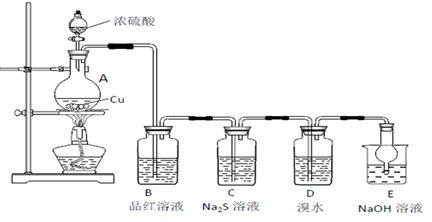
(1)A中发生反应的化学方程式为_______ 。
(2)B中的现象是_______ 。
(3)C中出现淡黄色沉淀,反应中Na2S做_______ (填“氧化剂”或“还原剂”)。
(4)D溴水褪色,该反应S元素的价态变化是由+4价变为_______ 价。

(1)A中发生反应的化学方程式为
(2)B中的现象是
(3)C中出现淡黄色沉淀,反应中Na2S做
(4)D溴水褪色,该反应S元素的价态变化是由+4价变为
您最近一年使用:0次



