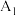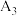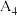1 . 实验室可用图中装置(略去部分夹持仪器)制取SO2并验证其性质。___________ 。
(2)仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若___________ ,则整个装置气密性良好。
(3)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择___________ (填序号)。
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(4)试管C中的试剂可以验证二氧化硫的氧化性,现象为___________ 。
(5)试管D中发生反应的化学方程式为___________ 。
(6)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案I:向第一份溶液中加入Ba(OH)2溶液,有白色沉淀生成;
方案II:向第二份溶液中加入Ba(NO3)2溶液,有白色沉淀生成;
方案III:向第三份溶液中加入BaCl2溶液,有产生白色沉淀。
上述方案中合理的是方案___________ (填“I”、“II”或“III”)。
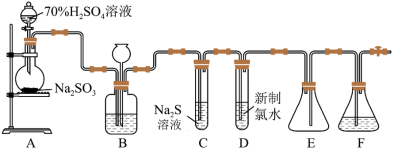
(2)仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若
(3)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(4)试管C中的试剂可以验证二氧化硫的氧化性,现象为
(5)试管D中发生反应的化学方程式为
(6)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案I:向第一份溶液中加入Ba(OH)2溶液,有白色沉淀生成;
方案II:向第二份溶液中加入Ba(NO3)2溶液,有白色沉淀生成;
方案III:向第三份溶液中加入BaCl2溶液,有产生白色沉淀。
上述方案中合理的是方案
您最近一年使用:0次
名校
解题方法
2 . 草酸是一种用途广泛的二元有机中强酸,某同学通过查阅资料设计了如图所示的装置(夹持仪器省略)制备一定量的草酸晶体( ),并验证其具有的某些性质。回答下列问题:
),并验证其具有的某些性质。回答下列问题:
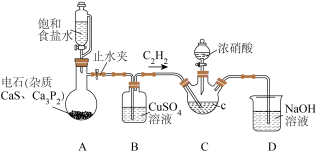
(1)装置B的作用是
 溶液检验有乙炔生成,则气体通过B后应先通入到盛有
溶液检验有乙炔生成,则气体通过B后应先通入到盛有 溶液中。
溶液中。(2)草酸在装置C中生成,反应的化学方程式为
(3)待反应结束后,从C中分离出草酸晶体,然后用0.1000 mol/L的酸性
 溶液进行滴定以测定其纯度。
溶液进行滴定以测定其纯度。①称量3.500 g草酸晶体配制100 mL溶液,下列配制操作中错误的是

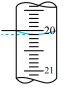
②三次平行滴定实验中消耗 溶液的体积如表所示,其中第一次实验滴定后的液面位置如图所示:
溶液的体积如表所示,其中第一次实验滴定后的液面位置如图所示:
滴定次数 | 待测溶液体积/mL | 标准溶液的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液的体积/mL | ||
第一次 | 20.00 | 0.20 |
| |
第二次 | 20.00 | 2.56 | 28.40 | |
第三次 | 20.00 | 0.22 | 20.32 | |
则
您最近一年使用:0次
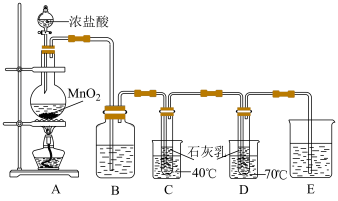
3 . 某小组设计如下实验装置制备漂白粉和氯酸钙并探究 的性质。
的性质。
查阅资料:① 。
。
② 。
。
回答下列问题:
(1)B中试剂是______ 。
(2)写出A中反应的离子方程式:_______________________ 。
(3)C、D中常采用的加热方式为__________________ 。
(4)探究影响 漂白性的因素。
漂白性的因素。
①设计实验Ⅰ、Ⅱ的目的是_______________ 。
②实验测得: 。由此得出的结论是
。由此得出的结论是___________________ 。
③某同学根据相关原理预测: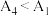 ,实验结果:
,实验结果: 。原理预测与实验结果相反的主要原因可能是
。原理预测与实验结果相反的主要原因可能是____________________________ 。
 的性质。
的性质。
查阅资料:①
 。
。②
 。
。回答下列问题:
(1)B中试剂是
(2)写出A中反应的离子方程式:
(3)C、D中常采用的加热方式为
(4)探究影响
 漂白性的因素。
漂白性的因素。实验 |
| 添加试剂 | 1%品红溶液 | 水浴温度 | 定溶液褪色时间/s |
I | 10mL | 2mL蒸馏水 | 2滴 | 25℃ |
|
Ⅱ | 10mL | 2mL | 2滴 | 25℃ |
|
Ⅲ | 10mL | 2mL | 2滴 | 25℃ |
|
Ⅳ | 10mL | 2mL蒸馏水 | 2滴 | 50℃ |
|
②实验测得:
 。由此得出的结论是
。由此得出的结论是③某同学根据相关原理预测:
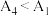 ,实验结果:
,实验结果: 。原理预测与实验结果相反的主要原因可能是
。原理预测与实验结果相反的主要原因可能是
您最近一年使用:0次
4 .  (四氢铝钠)是一种重要的还原剂和供氢剂,在有机合成中广泛应用。实验室制备原理为
(四氢铝钠)是一种重要的还原剂和供氢剂,在有机合成中广泛应用。实验室制备原理为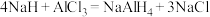 (在乙醚中进行,乙醚沸点:34.5℃)。某实验小组选择下列装置制备
(在乙醚中进行,乙醚沸点:34.5℃)。某实验小组选择下列装置制备 (装置可以重复使用,
(装置可以重复使用, 遇水蒸气剧烈反应)。下列叙述错误的是
遇水蒸气剧烈反应)。下列叙述错误的是
 (四氢铝钠)是一种重要的还原剂和供氢剂,在有机合成中广泛应用。实验室制备原理为
(四氢铝钠)是一种重要的还原剂和供氢剂,在有机合成中广泛应用。实验室制备原理为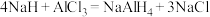 (在乙醚中进行,乙醚沸点:34.5℃)。某实验小组选择下列装置制备
(在乙醚中进行,乙醚沸点:34.5℃)。某实验小组选择下列装置制备 (装置可以重复使用,
(装置可以重复使用, 遇水蒸气剧烈反应)。下列叙述错误的是
遇水蒸气剧烈反应)。下列叙述错误的是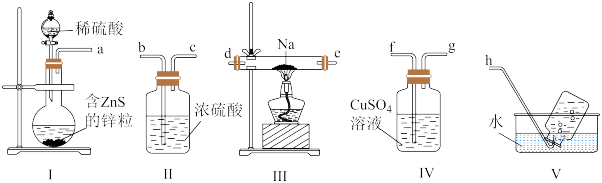
A.装置连接顺序为 |
| B.不能用浓硫酸、硝酸替代装置Ⅰ中的稀硫酸 |
| C.实验中观察到装置Ⅳ中产生黑色沉淀 |
D.实验室制备 的装置要保持干燥 的装置要保持干燥 |
您最近一年使用:0次
名校
5 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,探究其相关性质。

I.实验室制取氨气。
(1)图1装置中生成 的化学方程式为
的化学方程式为___________ 。
II.用图2所示装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。

(2)仪器b的名称是___________ ,b中无水硫酸铜的作用是___________ 。
(3)实验中观察到a中粉末变红(一种单质),b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为___________ 。
(4)若向a中通入标准状况下3.36L的氨气,最终得到铜的质量为_____ g(保留小数点后一位)。
III.按下图装置进行 其他性质实验,A、B容器的容积相同。
其他性质实验,A、B容器的容积相同。

(5)先打开旋塞1,B瓶中的现象是___________ ,原因是___________ ;稳定后,关闭旋塞1,再打开旋塞2,B瓶中的现象是___________ 。

I.实验室制取氨气。
(1)图1装置中生成
 的化学方程式为
的化学方程式为II.用图2所示装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。

(2)仪器b的名称是
(3)实验中观察到a中粉末变红(一种单质),b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
(4)若向a中通入标准状况下3.36L的氨气,最终得到铜的质量为
III.按下图装置进行
 其他性质实验,A、B容器的容积相同。
其他性质实验,A、B容器的容积相同。
(5)先打开旋塞1,B瓶中的现象是
您最近一年使用:0次
名校
解题方法
6 . 亚硝酸钠 主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用氮氧化物(可用
主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用氮氧化物(可用 表示)制备亚硝酸钠,简易流程如图。
表示)制备亚硝酸钠,简易流程如图。

已知: ,
,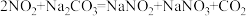
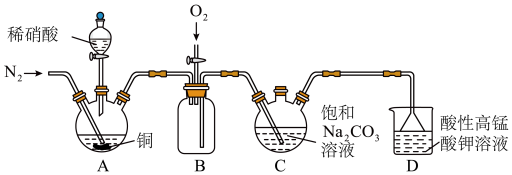
回答下列问题:
(1)利用饱和 溶液和饱和
溶液和饱和 溶液在加热条件下反应可制得
溶液在加热条件下反应可制得 ,该反应的化学方程式为
,该反应的化学方程式为_______ ;实验时装置B中应间断性通入适量的 ,其目的是
,其目的是_______ 。
(2)装置C中盛装饱和 溶液的仪器的名称是
溶液的仪器的名称是_______ ;NO不能单独被纯碱溶液吸收,为了使 完全被纯碱溶液吸收且产品纯度最高,
完全被纯碱溶液吸收且产品纯度最高,
_______ 。
(3)装置D的作用是_______ ,采用“倒置漏斗”措施的目的是_______ 。
(4)设计实验探究 的性质。实验完毕后,从装置C中分离出
的性质。实验完毕后,从装置C中分离出 固体粗产品(不含
固体粗产品(不含 杂质),取少量上述产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。
杂质),取少量上述产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。
上述实验_______ (填标号)的结论不可靠,理由是_______ 。经实验测得实验丙反应后的溶液中氮元素仅以 的形式存在,酸性
的形式存在,酸性 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为_______ 。
 主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用氮氧化物(可用
主要用于医药、染料和漂白等行业,也常用于食品保鲜剂。某小组拟利用氮氧化物(可用 表示)制备亚硝酸钠,简易流程如图。
表示)制备亚硝酸钠,简易流程如图。
已知:
 ,
,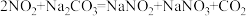

回答下列问题:
(1)利用饱和
 溶液和饱和
溶液和饱和 溶液在加热条件下反应可制得
溶液在加热条件下反应可制得 ,该反应的化学方程式为
,该反应的化学方程式为 ,其目的是
,其目的是(2)装置C中盛装饱和
 溶液的仪器的名称是
溶液的仪器的名称是 完全被纯碱溶液吸收且产品纯度最高,
完全被纯碱溶液吸收且产品纯度最高,
(3)装置D的作用是
(4)设计实验探究
 的性质。实验完毕后,从装置C中分离出
的性质。实验完毕后,从装置C中分离出 固体粗产品(不含
固体粗产品(不含 杂质),取少量上述产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。
杂质),取少量上述产品配制成溶液,分成三份分别进行甲、乙、丙三组实验,实验操作及现象、结论如表。| 实验 | 实验操作及现象 | 结论 |
| 甲 | 滴入无色酚酞溶液中,无色酚酞溶液变红 |  是弱酸 是弱酸 |
| 乙 | 滴入少量酸性KI-淀粉溶液中,振荡,酸性KI-淀粉溶液变蓝 | 酸性条件下, 具有氧化性 具有氧化性 |
| 丙 | 滴入少量酸性 溶液中,振荡,酸性 溶液中,振荡,酸性 溶液褪色 溶液褪色 | 酸性条件下, 具有还原性 具有还原性 |
 的形式存在,酸性
的形式存在,酸性 溶液与
溶液与 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次
7 . 实验室以浓硫酸、铜与NaOH溶液为原料制取少量NaHSO3并探究其性质,已知CuCl为白色难溶于水的化合物。
I.制备NaHSO3(装置如图所示)。

(1)仪器a的名称是____ 。
(2)装置丙的作用是____ 。
II.探究:NaHSO3与Cu2+的反应,设计实验:向2mL1mol·L-1NaHSO3溶液中加入2mL1mol·L-1CuSO4溶液,得到绿色溶液,3min内无明显变化。将所得混合液分为两等份。
①第一份加入适量Na2SO4固体,瞬间无明显变化,30s时也无明显变化。
②另一份加入适量NaCl固体,瞬间无明显变化,30s时有无色气体和白色沉淀生成,上层溶液颜色变浅。
(3)推测实验②产生的无色气体为SO2,用新制的氯水检验该无色气体,可观察到淡黄绿色消失,滴加BaCl2溶液有白色沉淀生成。写出SO2与氯气反应的离子方程式:____ 。
(4)对实验II产生SO2的原因进行分析,提出两种假设:
假设1:Cu2+水解使溶液中c(H+)增大。
假设2:Cl-存在时,Cu2+与HSO 反应生成CuCl白色沉淀,溶液中c(H+)增大。
反应生成CuCl白色沉淀,溶液中c(H+)增大。
①假设1不合理,实验证据是____ 。
②实验证实假设2合理,实验II中发生反应的离子方程式有____ 和H++HSO =SO2↑+H2O。
=SO2↑+H2O。
III.与碘酸盐的反应:向用H2SO4酸化的KIO3溶液中滴加NaHSO3溶液(以及少量淀粉溶液)。实验现象为“无色→蓝色→无色→蓝色→……”的周期性变化,此反应过程分为三步:①IO +3HSO
+3HSO =3SO
=3SO +3H++I-(慢);②IO
+3H++I-(慢);②IO +5I-+6H+=3I2+3H2O(慢);③I2+HSO
+5I-+6H+=3I2+3H2O(慢);③I2+HSO +H2O=2I-+SO
+H2O=2I-+SO +3H+(快)。
+3H+(快)。
(5)请解释出现该实验现象可能的原因:____ 。
IV.NaHSO3固体的纯度测定:称取wgNaHSO3固体溶于水配成100mL溶液,取25.00mL已配好的溶液置于锥形瓶中,用0.1000mol·L-1的酸性KMnO4溶液进行滴定,消耗KMnO4溶液VmL。(已知:2MnO +5HSO
+5HSO +H+=2Mn2++5SO
+H+=2Mn2++5SO +3H2O)
+3H2O)
(6)滴定终点的颜色变化为____ ,NaHSO3固体的纯度为____ (用含V和w的代数式表示)。
I.制备NaHSO3(装置如图所示)。

(1)仪器a的名称是
(2)装置丙的作用是
II.探究:NaHSO3与Cu2+的反应,设计实验:向2mL1mol·L-1NaHSO3溶液中加入2mL1mol·L-1CuSO4溶液,得到绿色溶液,3min内无明显变化。将所得混合液分为两等份。
①第一份加入适量Na2SO4固体,瞬间无明显变化,30s时也无明显变化。
②另一份加入适量NaCl固体,瞬间无明显变化,30s时有无色气体和白色沉淀生成,上层溶液颜色变浅。
(3)推测实验②产生的无色气体为SO2,用新制的氯水检验该无色气体,可观察到淡黄绿色消失,滴加BaCl2溶液有白色沉淀生成。写出SO2与氯气反应的离子方程式:
(4)对实验II产生SO2的原因进行分析,提出两种假设:
假设1:Cu2+水解使溶液中c(H+)增大。
假设2:Cl-存在时,Cu2+与HSO
 反应生成CuCl白色沉淀,溶液中c(H+)增大。
反应生成CuCl白色沉淀,溶液中c(H+)增大。①假设1不合理,实验证据是
②实验证实假设2合理,实验II中发生反应的离子方程式有
 =SO2↑+H2O。
=SO2↑+H2O。III.与碘酸盐的反应:向用H2SO4酸化的KIO3溶液中滴加NaHSO3溶液(以及少量淀粉溶液)。实验现象为“无色→蓝色→无色→蓝色→……”的周期性变化,此反应过程分为三步:①IO
 +3HSO
+3HSO =3SO
=3SO +3H++I-(慢);②IO
+3H++I-(慢);②IO +5I-+6H+=3I2+3H2O(慢);③I2+HSO
+5I-+6H+=3I2+3H2O(慢);③I2+HSO +H2O=2I-+SO
+H2O=2I-+SO +3H+(快)。
+3H+(快)。(5)请解释出现该实验现象可能的原因:
IV.NaHSO3固体的纯度测定:称取wgNaHSO3固体溶于水配成100mL溶液,取25.00mL已配好的溶液置于锥形瓶中,用0.1000mol·L-1的酸性KMnO4溶液进行滴定,消耗KMnO4溶液VmL。(已知:2MnO
 +5HSO
+5HSO +H+=2Mn2++5SO
+H+=2Mn2++5SO +3H2O)
+3H2O)(6)滴定终点的颜色变化为
您最近一年使用:0次
8 . 依据下列实验操作和现象,得出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向2mL0.1mol/LNa2S溶液中滴加0.1mol/LZnSO4溶液至不再有沉淀产生,再滴加几滴0.1mol/LCuSO4溶液 | 先产生白色沉淀,又出现黑色沉淀 |  |
| B | 将Cu与浓硫酸在加热条件下反应产生的气体通入BaCl2溶液中 | 有白色沉淀产生 |  能与 能与 溶液反应产生 溶液反应产生 |
| C | 向洁净的铁片上滴加几滴含有酚酞的氯化钠溶液 | 一段时间后,氯化钠溶液水滴的边缘显浅红色 | 铁发生了吸氧腐蚀 |
| D | 将溴乙烷、氢氧化钠的乙醇溶液混合加热反应产生的气体通入酸性KMnO4溶液中 | 溶液的紫红色变浅 | 溴乙烷能发生消去反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 回答下列问题
(1)①黑火药爆炸时发生的反应是S+2KNO3+3C K2S+3CO2↑+N2↑,反应中的还原剂是
K2S+3CO2↑+N2↑,反应中的还原剂是___________ ,每生成1molN2转移___________ mol电子,
②分离黑火药中三种成分的方法是将黑火药溶于水,过滤,蒸发滤液得___________ ,再将滤纸上的物质溶于___________ ,过滤,滤纸上留下的物质是___________ ;
(2)在空气中加热S粉和Fe粉的混合物,可观察到下列现象,请写出有关反应化学方程式。
①有淡蓝色火焰,且生成刺激性气味的气体___________ ,
②混合粉末变红,放出热量,最后变为黑色固体___________ ;
(3)在元旦联欢会上,某同学给同学们表演了一段魔术:首先收集一瓶红棕色的气体,用玻璃片盖好,然后向其中加入少量水,振荡后变为无色,然后轻轻移动玻璃片使少量空气进入集气瓶,气体又变为红棕色,振荡,又变为无色……
①集气瓶中红棕色的气体是___________ (写化学式),
②气体颜色变化的原因是___________ ,写出有关反应的化学方程式:___________ 。
(1)①黑火药爆炸时发生的反应是S+2KNO3+3C
 K2S+3CO2↑+N2↑,反应中的还原剂是
K2S+3CO2↑+N2↑,反应中的还原剂是②分离黑火药中三种成分的方法是将黑火药溶于水,过滤,蒸发滤液得
(2)在空气中加热S粉和Fe粉的混合物,可观察到下列现象,请写出有关反应化学方程式。
①有淡蓝色火焰,且生成刺激性气味的气体
②混合粉末变红,放出热量,最后变为黑色固体
(3)在元旦联欢会上,某同学给同学们表演了一段魔术:首先收集一瓶红棕色的气体,用玻璃片盖好,然后向其中加入少量水,振荡后变为无色,然后轻轻移动玻璃片使少量空气进入集气瓶,气体又变为红棕色,振荡,又变为无色……
①集气瓶中红棕色的气体是
②气体颜色变化的原因是
您最近一年使用:0次
名校
10 . 实验室可用下列装置(部分夹持仪器略去)制取 并验证其性质。
并验证其性质。
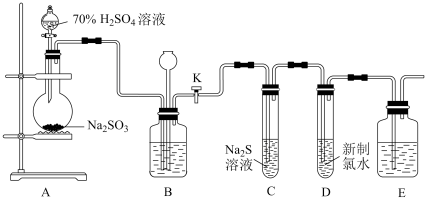
(1)检查装置A、B气密性的操作为:先关闭装置A中分液漏斗活塞和装置B中止水夹K,往长颈漏斗中注水至水柱高于广口瓶液面,若观察到_______ ,则气密性良好。
(2) 和HClO都能使品红褪色,鉴别
和HClO都能使品红褪色,鉴别 和HClO漂白品红差异的方法:
和HClO漂白品红差异的方法:_______ ;
(3)实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,证明二氧化硫具有_______ (填“还原性”、“氧化性”或“漂白性”)
(4)实验结束时,关闭止水夹K,装置B所起的作用是_______ 。
(5)取少量试管D中的溶液,加入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
①该白色沉淀为_______ (写化学式);
② 通入试管D中反应的化学方程式为
通入试管D中反应的化学方程式为_______ 。
(6)用下图装置验证 酸性比
酸性比 强。
强。

请从下列试剂中选择合适试剂以完成实验(要求:试剂不重复,填代号):
A.品红溶液 B.酸性 溶液 C.饱和
溶液 C.饱和 溶液 D.饱和
溶液 D.饱和
则溶液X为_______ ,Y为B,Z为_______ 。
 并验证其性质。
并验证其性质。
(1)检查装置A、B气密性的操作为:先关闭装置A中分液漏斗活塞和装置B中止水夹K,往长颈漏斗中注水至水柱高于广口瓶液面,若观察到
(2)
 和HClO都能使品红褪色,鉴别
和HClO都能使品红褪色,鉴别 和HClO漂白品红差异的方法:
和HClO漂白品红差异的方法:(3)实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,证明二氧化硫具有
(4)实验结束时,关闭止水夹K,装置B所起的作用是
(5)取少量试管D中的溶液,加入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。①该白色沉淀为
②
 通入试管D中反应的化学方程式为
通入试管D中反应的化学方程式为(6)用下图装置验证
 酸性比
酸性比 强。
强。
请从下列试剂中选择合适试剂以完成实验(要求:试剂不重复,填代号):
A.品红溶液 B.酸性
 溶液 C.饱和
溶液 C.饱和 溶液 D.饱和
溶液 D.饱和
则溶液X为
您最近一年使用:0次