1 . 氯气是一种重要的工业原料,某研究性学习小组查阅资料得知,漂白粉与硫酸反应可制取氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O。他们利用该反应设计如图所示制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O。他们利用该反应设计如图所示制取氯气并验证其性质的实验。

回答下列问题:
(1)该实验中A部分的装置是______ (填标号)。
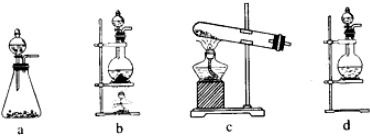
(2)装置B中产生的现象为______ 。
(3)请设计实验验证装置C中的Na2SO3已被氧化______ 。
(4)写出D装置中发生反应的离子方程式______ 。
(5)该实验存在明显的缺陷,请你提出改进的方法______ 。
(6)若将上述装置改为制取SO2并分别验证SO2的漂白性、氧化性和还原性等性质。B中______ 溶液褪色,则说明产生的气体为SO2;C中Na2S溶液出现______ ;D中______ 溶液褪色,说明SO2有还原性。
 2CaSO4+2Cl2↑+2H2O。他们利用该反应设计如图所示制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O。他们利用该反应设计如图所示制取氯气并验证其性质的实验。
回答下列问题:
(1)该实验中A部分的装置是

(2)装置B中产生的现象为
(3)请设计实验验证装置C中的Na2SO3已被氧化
(4)写出D装置中发生反应的离子方程式
(5)该实验存在明显的缺陷,请你提出改进的方法
(6)若将上述装置改为制取SO2并分别验证SO2的漂白性、氧化性和还原性等性质。B中
您最近一年使用:0次
解题方法
2 . 戴口罩是新冠肺炎疫情常态化防控的措施之一。一次性医用口罩绒布的主要成分是聚丙烯[(C3H6)n],随意丢弃易引起白色污染。某兴趣小组尝试用焚烧法对口罩绒布进行处理,并将燃烧产物用氢氧化钠溶液吸收。
(1)聚丙烯完全燃烧的化学方程式为:2(C3H6)n+9nO2 6nCO2+6nX,X的化学式为
6nCO2+6nX,X的化学式为________ 。
(2)为“看见”CO2与NaOH的反应,甲同学设计了如图所示的实验方案,当观察到______ 现象时,说明两者发生反应。
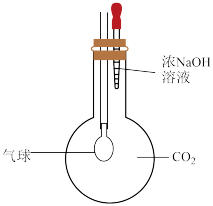
(3)将完全燃烧后的产物全部通入一定量的氢氧化钠溶液中,得到吸收液。乙同学对吸收液的成分产生兴趣,进行如下探究:
【提出问题】
吸收液中溶质的成分是什么?
【查阅资料】
①Na2CO3、NaHCO3的溶液均呈碱性;CaCl2溶液呈中性。
②NaOH与NaHCO3能反应
③Na2CO3+CaCl2=CaCO3↓+2NaCl
2NaHCO3+CaCl2=CaCO3↓+2NaCl+H2O+CO2↑
【猜想假设】
猜想一:NaOH、Na2CO3
猜想二:________
猜想三:Na2CO3、NaHCO3
猜想四:NaHCO3
【实验探究】
【交流反思】
实验结束后,为了对吸收液进行无害化处理,丙同学向吸收液中加入稀盐酸至不再产生气泡为止。写出其中一个反应的化学方程式:________ 。
(1)聚丙烯完全燃烧的化学方程式为:2(C3H6)n+9nO2
 6nCO2+6nX,X的化学式为
6nCO2+6nX,X的化学式为(2)为“看见”CO2与NaOH的反应,甲同学设计了如图所示的实验方案,当观察到

(3)将完全燃烧后的产物全部通入一定量的氢氧化钠溶液中,得到吸收液。乙同学对吸收液的成分产生兴趣,进行如下探究:
【提出问题】
吸收液中溶质的成分是什么?
【查阅资料】
①Na2CO3、NaHCO3的溶液均呈碱性;CaCl2溶液呈中性。
②NaOH与NaHCO3能反应
③Na2CO3+CaCl2=CaCO3↓+2NaCl
2NaHCO3+CaCl2=CaCO3↓+2NaCl+H2O+CO2↑
【猜想假设】
猜想一:NaOH、Na2CO3
猜想二:
猜想三:Na2CO3、NaHCO3
猜想四:NaHCO3
【实验探究】
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 取吸收液少许于试管中,滴加2~3滴无色酚酞溶液 | 溶液呈碱性 | |
| 2 | 向步骤1所得溶液中加入过量的CaCl2溶液 | 产生白色沉淀,溶液为红色 | 猜想 |
实验结束后,为了对吸收液进行无害化处理,丙同学向吸收液中加入稀盐酸至不再产生气泡为止。写出其中一个反应的化学方程式:
您最近一年使用:0次
名校
3 . 实验室进行二氧化硫制备与性质实验的组合装置如图所示,部分夹持装置未画出。
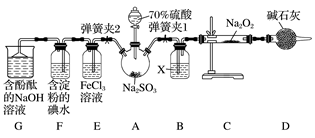
请回答下列问题:
(1)在组装好装置后,首先要进行的实验操作为_______________ 。
(2)为检验SO2与Na2O2的反应是否有氧气生成,装置B中盛放的试剂X应为________ ,装置D中碱石灰的作用是_______________________________________________ 。
(3)关闭弹簧夹2,打开弹簧夹1,注入70%的硫酸至浸没三颈烧瓶中的固体,检验SO2与Na2O2反应是否有氧气生成的操作及现象是_____________________________________ 。
(4)关闭弹簧夹1,打开弹簧夹2,残余气体进入装置E、F、G中,能说明I-的还原性弱于SO2的现象为_________________ 。发生反应的离子方程式是_______________ 。
(5)为了验证装置E中SO2与FeCl3发生了氧化还原反应,某学生设计了如下实验:取少量装置E中的溶液于试管中,向其中加入稀硝酸酸化的BaCl2溶液,产生白色沉淀,并由此判断SO2与FeCl3发生了氧化还原反应。上述方案是否合理?________ (填“合理”或“不合理”),原因是________ 。

请回答下列问题:
(1)在组装好装置后,首先要进行的实验操作为
(2)为检验SO2与Na2O2的反应是否有氧气生成,装置B中盛放的试剂X应为
(3)关闭弹簧夹2,打开弹簧夹1,注入70%的硫酸至浸没三颈烧瓶中的固体,检验SO2与Na2O2反应是否有氧气生成的操作及现象是
(4)关闭弹簧夹1,打开弹簧夹2,残余气体进入装置E、F、G中,能说明I-的还原性弱于SO2的现象为
(5)为了验证装置E中SO2与FeCl3发生了氧化还原反应,某学生设计了如下实验:取少量装置E中的溶液于试管中,向其中加入稀硝酸酸化的BaCl2溶液,产生白色沉淀,并由此判断SO2与FeCl3发生了氧化还原反应。上述方案是否合理?
您最近一年使用:0次
2017-06-03更新
|
607次组卷
|
5卷引用:西藏山南地区第二高级中学2017届高三第三次模拟考试理综化学试题
西藏山南地区第二高级中学2017届高三第三次模拟考试理综化学试题【全国百强校】陕西省西安中学2019届高三上学期期中考试化学试题陕西省咸阳百灵中学2020届高三上学期期中考试化学试题浙江省杭州地区(含周边)重点中学2020-2021学年高一下学期期中考试化学试题(已下线)【2023】【高一下】【其他】【杭高-期中复习卷】【高中化学】【刘尼尼收集】
4 . 某研究小组用下图装置进行SO2 与FeCl3溶液反应的相关实验(夹持装置已略去)。
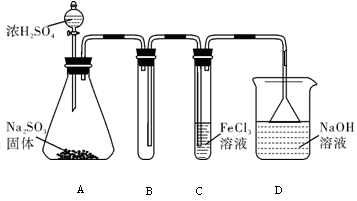
(1)配制氯化铁溶液时,需先把氯化铁晶体溶解在______ 中,再加水稀释,这样操作的目的是__________________________________________ 。
(2)通入足量SO2时,装置C中观察到的现象为___________________________________ 。
(3)根据以上现象,该小组同学认为SO2 与 FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式____________________________________ ;
②请设计实验方案检验有Fe2+ 生成___________________________________________ ;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42 -,该做法____ (填“合理”或“不合理”),理由是__________ 。
(4)D装置中倒置漏斗的作用是_________________________________________________ 。
(5)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有____________ (填字母)。
a.浓H2SO4 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液

(1)配制氯化铁溶液时,需先把氯化铁晶体溶解在
(2)通入足量SO2时,装置C中观察到的现象为
(3)根据以上现象,该小组同学认为SO2 与 FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式
②请设计实验方案检验有Fe2+ 生成
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42 -,该做法
(4)D装置中倒置漏斗的作用是
(5)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有
a.浓H2SO4 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液
您最近一年使用:0次
2018-10-17更新
|
246次组卷
|
2卷引用:西藏自治区林芝二高2019届高三上学期第四次月考化学试题
名校
5 . 某同学欲探究Na2O2与水的反应,可供使用的试剂有:Na2O2、蒸馏水、酸性KMnO4溶液、MnO2。该同学取一定量Na2O2样品与过量水反应,待完全反应后,得到溶液X和一定量O2,该同学推测反应中可能生成了H2O2,并进行实验探究。
(1)写出Na2O2与水反应的化学方程式_______________________________________ 。
(2)试设计实验证明溶液X中含过氧化氢____________________________________ 。
(3)通过上述实验证明溶液中确实存在H2O2。取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:______ H2O2+______ Fe2++_____ OH-===______ Fe(OH)3↓,该反应中H2O2表现了_______ (填“氧化”或“还原”)性。
(4)已知溶液X可使酸性KMnO4溶液褪色,已知高锰酸钾产物为Mn2+,此时H2O2表现了______ (填“氧化”或“还原”)性。该反应的离子方程式为____________________ 。
(1)写出Na2O2与水反应的化学方程式
(2)试设计实验证明溶液X中含过氧化氢
(3)通过上述实验证明溶液中确实存在H2O2。取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,配平下列反应的离子方程式:
(4)已知溶液X可使酸性KMnO4溶液褪色,已知高锰酸钾产物为Mn2+,此时H2O2表现了
您最近一年使用:0次



