1 . 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应,应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”,请回答该实验中的问题。_______ ,该反应的氧化剂是_______ 。
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是_______ ;烧瓶底部放置了几片碎瓷片,其作用是_______ 。
(3)酒精灯和酒精喷灯点燃的顺序是先点燃_______ 。
(4)试管中收集气体是_______ ,如果要在A处玻璃管处点燃该气体,则必须对该气体进行_______ 。
(5)若该反应中有16.8gFe参加反应,则生成H2的质量为_______ g。
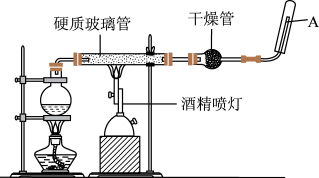
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是
(3)酒精灯和酒精喷灯点燃的顺序是先点燃
(4)试管中收集气体是
(5)若该反应中有16.8gFe参加反应,则生成H2的质量为
您最近一年使用:0次
2023-03-02更新
|
134次组卷
|
2卷引用:吉林省洮南市第一中学2022-2023学年高一上学期期末考试化学试题
2014高三·全国·专题练习
名校
解题方法
2 . 某兴趣小组为了探究SO2气体还原Fe3+的反应,他们使用的药品和装置如下图所示,下列说法不合理的是
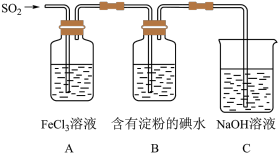
| A.能表明I-的还原性弱于SO2的现象是B中蓝色溶液褪色 |
| B.装置C的作用是吸收SO2尾气,防止污染空气 |
| C.为了验证A中发生了氧化还原反应,加入酸性KMnO4溶液,紫色褪去 |
| D.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2溶液,产生白色沉淀 |
您最近一年使用:0次
2023-02-21更新
|
960次组卷
|
56卷引用:2015-2016学年吉林省松原市油田高中高二下期末化学试卷
2015-2016学年吉林省松原市油田高中高二下期末化学试卷2015-2016学年黑龙江省大庆铁人中学高一上期末化学试卷【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高一上学期期末考试化学试题安徽省滁州市定远县重点中学2018-2019学年高一上学期期末考试化学试题云南省丽江市宁蒗县第一中学2019—2020学年高一上学期期末考试化学试题云南省曲靖市罗平县第三中学2019-2020学年高一上学期期末考试化学试题云南省曲靖市沾益县炎方一中2019-2020学年高一上学期期末考试化学试题(已下线)2014年高考化学鲁科版3.3硫的转化练习卷2015-2016学年河北石家庄一中高一下学情反馈一化学卷2017届广东省中山一中高三上学期第一次统测化学试卷2017届黑龙江省牡丹江高级中学高三10月月考化学卷2017届河北省衡水中学高三上期中化学卷2017届山东省莱芜一中高三上学期10月月考化学试卷2017届河南省南阳一中高三上第三次周考化学卷福建省泰宁第一中学2018届高三上学期第一阶段考试化学试题宁夏石嘴山市第三中学2018届高三上学期期中考试化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【押题专练】(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【教学案】【全国百强校】黑龙江省牡丹江市第一高级中学2019届高三上学期期中考试化学试题山东省东营市第二中学2019届高三上学期模块考试(期中)化学试题贵州省剑河县第二中学2018-2019学年高一上学期12月份考试化学试题甘肃省甘谷第一中学2020届高三上学期第一次检测化学试题云南省西畴县二中2019-2020学年高二上学期开学考试化学试题苏教版高中化学必修1专题4《硫 氮可持续发展》测试卷河南省商丘市第一高级中学2020届高三上学期期中考试化学试题河南省开封市第二十五中2019-2020高一下学期初分科考试化学试卷(已下线)专题4.3 硫及其化合物(练)——2020年高考化学一轮复习讲练测河北省衡水市桃城区第十四中学2019-2020学年高一下学期第五次综合测试化学试题(已下线)第四单元 非金属及其化合物测试题-2021年高考化学一轮复习名师精讲练(已下线)第15讲 硫及其化合物(精练)-2021年高考化学一轮复习讲练测福建省福州市闽江口联盟校2021届高三上学期期中联考化学试题(已下线)练习9 硫和二氧化硫-2020-2021学年【补习教材·寒假作业】高一化学(人教版2019)浙江省温州市瑞安市上海新纪元高级中学2021-2022学年高一9月份月考(5-6班)化学试题(已下线)4.2.1 含硫物质之间的转化(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)河南省林州市第一中学2021-2022学年高一下学期开学检测化学试题课后-5.1.3 不同价态含硫物质的转化-人教2019必修第二册广东省佛山市第一中学2021-2022学年高一下学期第一次段考(3月)化学试题湖南省常德市安乡县第一中学2021-2022 学年高二下学期期中考试化学试题湖南省湘潭市湘潭县第一中学2021-2022学年高三下学期期中考试化学试题上海交通大学附属中学2022-2023学年高二上学期开学摸底考试化学试题湖北省公安县第三中学2021-2022学年高三上学期8月质量检测化学试题安徽省宿州市第二中学2022-2023学年高一上学期第一次月考化学试题安徽省阜阳市第一中学2022-2023学年高一下学期第一次月考化学试题安徽省安庆市第一中学2022-2023学年高一下学期第一次月考化学试题安徽省亳州市第一中学2022-2023学年高一下学期第一次月考化学试题河南省郑州外国语学校2022-2023学年高一下学期第一次月考化学试题安徽省阜阳市太和中学2022-2023学年高一下学期第一次质量检测化学试题四川省广安市育才学校2022-2023学年高一下学期3月月考化学试题广东省广州市培英中学2022-2023学年高一下学期期中考试化学试题湖南省衡阳县第四中学2022-2023学年高一下学期第一次(3月)月考化学试题湖南省株洲市炎陵县2022-2023学年高一下学期3月月考化学试题安徽省淮北市树人高级中学2023-2024学年高一下学期开学考试化学试题北京师范大学第二附属中学2023-2024学年高一下学期3月化学测试题安徽省芜湖市第一中学2022-2023学年高一下学期3月份教学质量诊断测试化学试卷山西省大同市第一中学校2023-2024学年高一下学期4月期中考试化学试题云南省丽江润泽高级中学2023-2024学年高一下学期3月月中考试化学试题
名校
3 . 某课外活动小组设计实验验证二氧化碳跟过氧化钠反应时需要与水接触。下列说法中正确的是
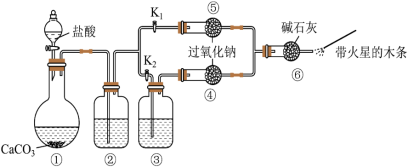

| A.装置①中盐酸不能换成硫酸 |
B.装置②中的试剂是饱和 溶液 溶液 |
C.打开弹簧夹 ,关闭 ,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃 |
| D.上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应 |
您最近一年使用:0次
2022-12-07更新
|
193次组卷
|
2卷引用:吉林省延边州2022-2023学年高一上学期期末学业质量检测化学试题
解题方法
4 . 某同学为了验证硫铁矿(主要成分为FeS2。含有少量的碳)焙烧产物(产生的气体是SO2,CO2),设计如下装置进行实验:
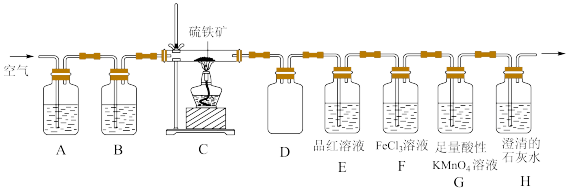
回答下列问题:
(1)装置A、B中的试剂分别是_______ 、_______ 。
(2)装置D的作用是_______ 。
(3)验证焙烧后气体产物的实验现象分别为_______ 、_______ ;若F中颜色发生改变,写出产生颜色变化反应的离子方程式:_______ 。取F中反应后的溶液于洁净的试管中。滴加少量KSCN溶液,溶液不变红,说明溶液中_______ (填“含有”或“不含有”)Fe3+;再继续滴加少量氯水,溶液也不变红。产生这种现象的原因可能是_______ 。
(4)G中盛放足量酸性KMnO4溶液的目的是_______ (用离子方程式表示)。
(5)反应完成后经检验,C中剩余固体物质只有Fe2O3,写出FeS2焙烧反应的化学方程式:_______ 。

回答下列问题:
(1)装置A、B中的试剂分别是
(2)装置D的作用是
(3)验证焙烧后气体产物的实验现象分别为
(4)G中盛放足量酸性KMnO4溶液的目的是
(5)反应完成后经检验,C中剩余固体物质只有Fe2O3,写出FeS2焙烧反应的化学方程式:
您最近一年使用:0次
名校
5 . 用如图所示实验装置进行相关实验探究,下列说法不合理的是

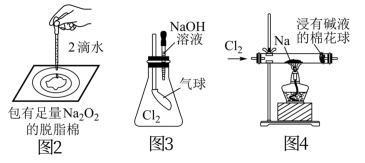


| A.图1若二氧化锰过量,则浓盐酸可全部反应完 |
| B.图2证明Na2O2与水反应放热 |
| C.图3证明Cl2能与烧碱溶液反应 |
| D.图4探究钠与Cl2反应 |
您最近一年使用:0次
2022-01-05更新
|
289次组卷
|
2卷引用:吉林省吉林松花江中学2022-2023学年高一上学期1月期末考试化学试题
解题方法
6 . I.在碘化钾和硫酸的混合溶液中加入过氧化氢水溶液,迅速发生反应放出大量气体,反应过程可表示如下:
①H2O2+2KI+H2SO4=I2+K2SO4+2H2O;
②H2O2+I2=2HIO;
③H2O2+2HIO=I2+O2↑+2H2O
(1)H2O2在反应③中的作用是______ (填正确选项的标号)
A.氧化剂 B.还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂也不是还原剂
(2)有人认为上述反应说明了碘单质是过氧化氢分解的催化剂,你认为______ (填“对”或“不对”),其理由是______ 。
(3)上述反应说明H2O2、I2、HIO氧化性从强到弱的顺序是______ >______ >______ 。
II.硫酸亚铁(FeSO4·7H2O)是一种重要的食品和饲料添加剂。实验室通过如下实验由废铁屑制备FeSO4·7H2O晶体:
①将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗涤2~3遍;
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50~80℃之间至铁屑耗尽;
③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次,再用滤纸将晶体吸干;
⑤将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存。请回答下列问题:
(1)Fe(OH)3在碱性介质中与NaClO反应生成Na2FeO4和NaCl,写出Fe(OH)3与NaClO在碱性介质中反应的离子方程式是______ 。
(2)硫酸亚铁制备中实验步骤①的目的是______ 。
(3)实验步骤②明显不合理,理由是______ 。
(4)实验步骤④中用少量冰水洗涤晶体,其目的是______ 。
①H2O2+2KI+H2SO4=I2+K2SO4+2H2O;
②H2O2+I2=2HIO;
③H2O2+2HIO=I2+O2↑+2H2O
(1)H2O2在反应③中的作用是
A.氧化剂 B.还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂也不是还原剂
(2)有人认为上述反应说明了碘单质是过氧化氢分解的催化剂,你认为
(3)上述反应说明H2O2、I2、HIO氧化性从强到弱的顺序是
II.硫酸亚铁(FeSO4·7H2O)是一种重要的食品和饲料添加剂。实验室通过如下实验由废铁屑制备FeSO4·7H2O晶体:
①将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗涤2~3遍;
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50~80℃之间至铁屑耗尽;
③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次,再用滤纸将晶体吸干;
⑤将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存。请回答下列问题:
(1)Fe(OH)3在碱性介质中与NaClO反应生成Na2FeO4和NaCl,写出Fe(OH)3与NaClO在碱性介质中反应的离子方程式是
(2)硫酸亚铁制备中实验步骤①的目的是
(3)实验步骤②明显不合理,理由是
(4)实验步骤④中用少量冰水洗涤晶体,其目的是
您最近一年使用:0次
解题方法
7 . 某同学用如图装置(夹持装置略)探究铜丝与过量浓硫酸的反应。
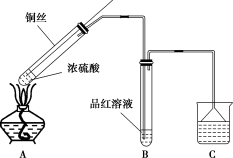
回答下列问题:
(1)铜与浓硫酸反应的化学方程式为___ 。
(2)B中观察到的现象为___ 。
(3)C中应加入的试剂为___ ,倒置漏斗的作用是___ 。
(4)与向浓硫酸中直接加入铜片相比,该装置用可上下移动的铜丝,优点是___ 。

回答下列问题:
(1)铜与浓硫酸反应的化学方程式为
(2)B中观察到的现象为
(3)C中应加入的试剂为
(4)与向浓硫酸中直接加入铜片相比,该装置用可上下移动的铜丝,优点是
您最近一年使用:0次
2021-05-26更新
|
269次组卷
|
4卷引用:吉林省延边州汪清县第六中学2021-2022学年高一下学期期末考试化学试题
解题方法
8 . 钠和氯是我们熟悉的典型金属元素与非金属元素,研究它们的性质对于生产、生活、科研具有重要意义。
I.某化学兴趣小组为了探究“干燥的CO2不能与Na2O2反应”而“潮湿的CO2能与Na2O2反应”,设计了如图1所示装置进行实验(夹持仪器已省略)。
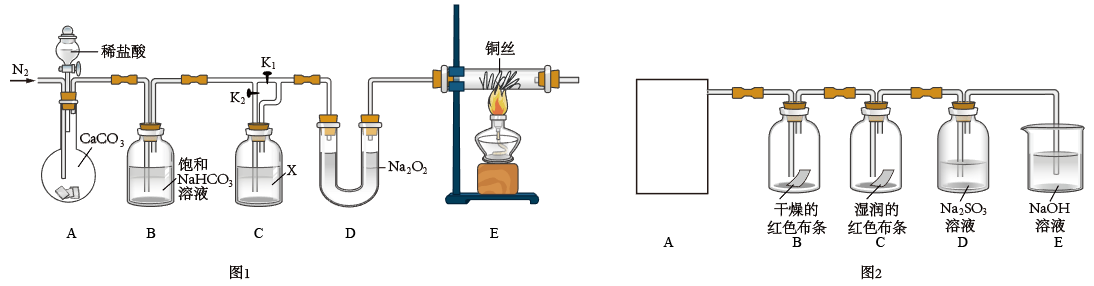
回答下列问题:
(1)实验开始前先通入一段时间的N2,目的是___ 。
(2)饱和NaHCO3溶液的作用是___ ,试剂X是___ 。
(3)实验时,首先打开装置A中分液漏斗的活塞,加入稀盐酸;然后关闭K1,打开K2,实验中观察到E中灼热的铜丝颜色未发生变化,则得出的结论是___ 。
(4)写出D中CO2与Na2O2反应的化学方程式___ 。
II.为探究氯气的性质,某同学利用此原理制氯气并设计了如图2所示的实验装置(A为氯气制取装置,未画出)。
(1)装置B、C中依次盛放的是干燥的红色布条和湿润的红色布条,其目的是___ 。实验过程中该同学发现装置B中的布条也褪色,说明该装置存在明显的缺陷,改进的方法是___ 。
(2)E中NaOH溶液吸收氯气时发生反应的化学方程式是___ 。
(3)D中氯气可将SO 氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是
氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是___ (提示:SO 遇盐酸生成SO2气体。写出操作试剂和现象)
遇盐酸生成SO2气体。写出操作试剂和现象)
(4)“84消毒液”是生活中常用的消毒剂,可与硫酸反应制取氯气,反应原理为NaClO+NaCl+H2SO4 Na2SO4+Cl2↑+H2O,制备氯气的反应中,每生成1molCl2,转移的电子的物质的量是
Na2SO4+Cl2↑+H2O,制备氯气的反应中,每生成1molCl2,转移的电子的物质的量是___ mol。
I.某化学兴趣小组为了探究“干燥的CO2不能与Na2O2反应”而“潮湿的CO2能与Na2O2反应”,设计了如图1所示装置进行实验(夹持仪器已省略)。

回答下列问题:
(1)实验开始前先通入一段时间的N2,目的是
(2)饱和NaHCO3溶液的作用是
(3)实验时,首先打开装置A中分液漏斗的活塞,加入稀盐酸;然后关闭K1,打开K2,实验中观察到E中灼热的铜丝颜色未发生变化,则得出的结论是
(4)写出D中CO2与Na2O2反应的化学方程式
II.为探究氯气的性质,某同学利用此原理制氯气并设计了如图2所示的实验装置(A为氯气制取装置,未画出)。
(1)装置B、C中依次盛放的是干燥的红色布条和湿润的红色布条,其目的是
(2)E中NaOH溶液吸收氯气时发生反应的化学方程式是
(3)D中氯气可将SO
 氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是
氧化,若通过实验验证该反应发生的是氧化还原反应,可采取的方法是 遇盐酸生成SO2气体。写出操作试剂和现象)
遇盐酸生成SO2气体。写出操作试剂和现象)(4)“84消毒液”是生活中常用的消毒剂,可与硫酸反应制取氯气,反应原理为NaClO+NaCl+H2SO4
 Na2SO4+Cl2↑+H2O,制备氯气的反应中,每生成1molCl2,转移的电子的物质的量是
Na2SO4+Cl2↑+H2O,制备氯气的反应中,每生成1molCl2,转移的电子的物质的量是
您最近一年使用:0次
名校
解题方法
9 . 如图装置用来检验氯气的部分性质。

(1)装置A的作用是___ 。
(2)装置B、C中的布条褪色的是___ 。
(3)装置D中发生的反应方程式为___ 。
(4)氯气可以用于自来水消毒,请用化学方程式和简要文字说明理由___ 。

(1)装置A的作用是
(2)装置B、C中的布条褪色的是
(3)装置D中发生的反应方程式为
(4)氯气可以用于自来水消毒,请用化学方程式和简要文字说明理由
您最近一年使用:0次
名校
10 . 向CuSO4溶液中加入H2O2溶液,很快又大量气体逸出,同时放热,一段时间后,蓝色溶液变为红色浑浊(Cu2O),继续加入H2O2溶液,红色浑浊又变为蓝色溶液,这个过程可以反复多次。下列关于上述过程的说法中不正确的是
| A.Cu2+将H2O2氧化为O2 |
| B.H2O2只表现还原性 |
| C.Cu2+是H2O2分解的催化剂 |
| D.红色浑浊变蓝色溶液的原因是:Cu2O+H2O2+4H+=2Cu2++3H2O |
您最近一年使用:0次



