1 . 为探究 的性质,进行了如下实验(
的性质,进行了如下实验( 和
和 溶液浓度均为
溶液浓度均为 )。
)。
依据上述实验现象,结论不合理的是
 的性质,进行了如下实验(
的性质,进行了如下实验( 和
和 溶液浓度均为
溶液浓度均为 )。
)。| 实验 | 操作与现象 |
| ① | 在 水中滴加2滴 水中滴加2滴 溶液,呈棕黄色;煮沸,溶液变红褐色。 溶液,呈棕黄色;煮沸,溶液变红褐色。 |
| ② | 在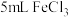 溶液中滴加2滴 溶液中滴加2滴 溶液,变红褐色; 溶液,变红褐色;再滴加  溶液,产生蓝色沉淀。 溶液,产生蓝色沉淀。 |
| ③ | 在 溶液中滴加2滴 溶液中滴加2滴 溶液,变红褐色; 溶液,变红褐色;将上述混合液分成两份,一份滴加  溶液,无蓝色沉淀生成; 溶液,无蓝色沉淀生成;另一份煮沸,产生红褐色沉淀。 |
A.实验①说明加热促进 水解反应 水解反应 |
B.实验②说明 既发生了水解反应,又发生了还原反应 既发生了水解反应,又发生了还原反应 |
C.实验③说明 发生了水解反应,但没有发生还原反应 发生了水解反应,但没有发生还原反应 |
D.整个实验说明 对 对 的水解反应无影响,但对还原反应有影响 的水解反应无影响,但对还原反应有影响 |
您最近一年使用:0次
2022-06-10更新
|
12802次组卷
|
48卷引用:辽宁省大连市滨城高中联盟2022-2023学年高二上学期期中考试化学试题
辽宁省大连市滨城高中联盟2022-2023学年高二上学期期中考试化学试题2022年新高考湖南化学高考真题(已下线)2022年湖南卷高考真题变式题(11-14)(已下线)专题10 水溶液中的离子平衡-2022年高考真题模拟题分项汇编(已下线)专题11 化学实验基础-2022年高考真题模拟题分项汇编(已下线)专题11 化学实验基础-三年(2020-2022)高考真题分项汇编(已下线)专题12 化学实验方案的设计与评价-三年(2020-2022)高考真题分项汇编(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第06讲 氧化还原反应(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)考点28 盐类的水解-备战2023年高考化学一轮复习考点帮(全国通用)内蒙古通辽市开鲁县第一中学2021-2022学年高二下学期6月检测化学试题(已下线)第03讲 氧化还原反应(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第07练 铁及其化合物-2023年高考化学一轮复习小题多维练(全国通用)湖北省荆州市公安县第三中学2022-2023学年高三上学期8月月考化学试题山东省枣庄市第三中学2022-2023学年高三上学期开学考试化学试题(已下线)第23讲 盐类水解 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)湖南省株洲市攸县第三中学2022-2023学年高三上学期第一次月考化学试题广东省广州市海珠外国语实验中学2022-2023学年高三上学期第二次阶段性考试化学试题(已下线)易错点34 化学实验方案的设计与评价-备战2023年高考化学考试易错题河北省石家庄市第二中学2022-2023学年高二上学期10月月考化学试题(已下线)专题06 水溶液中的离子平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)宁夏银川外国语实验学校2023届高三上学期第二次月考化学试题(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破河南省顶级名校2022-2023学年高三上学期12月摸底考试化学试题坚持素养导向 突出创新命题湖南省长沙市第一中学2022-2023学年高三上学期月考卷(五)化学试题(已下线)第一部分 二轮专题突破 专题18 物质检验、鉴别简单实验方案的设计及评价湖南省攸县第三中学2022-2023学年高三第六次月考化学试题趋势1 创新命题形式河南省商丘市第一高级中学2022-2023学年高二上学期期末考试化学试题(已下线)题型181 “实验-现象-结论”微型实验方案的设计与评价(已下线)题型45 物质性质探究型综合实验(已下线)专题14 化学实验方案的设计与评价(已下线)专题14 化学实验方案的设计与评价(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点巩固卷12 化学实验基础(一)(3大考点67题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)专题09 水溶液中的离子平衡-2023年高考化学真题题源解密(新高考专用)(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)辽宁省沈阳市第二中学2023-2024学年高三上学期开学暑假阶段验收化学测试题河北省石家庄市第二中学2022-2023学年高三下学期2月月考化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点3 盐类水解(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第4讲 盐类的水解山东省枣庄市第三中学2023-2024学年高三上学期10月月考化学试题辽宁省沈阳市第二中学2023-2024学年高三上学期开学考试化学试题山西省运城市河津中学2023-2024学年高二下学期开学考试化学试题(已下线)第04讲 氧化还原反应的基本概念和规律(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
2 . 超酸是一类比纯硫酸更强的酸,在石油重整中用作高效催化剂。某实验小组对超酸HSbF6的制备及性质进行了探究。由三氯化锑(SbCl3)制备HSbF6的反应如下: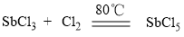 、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
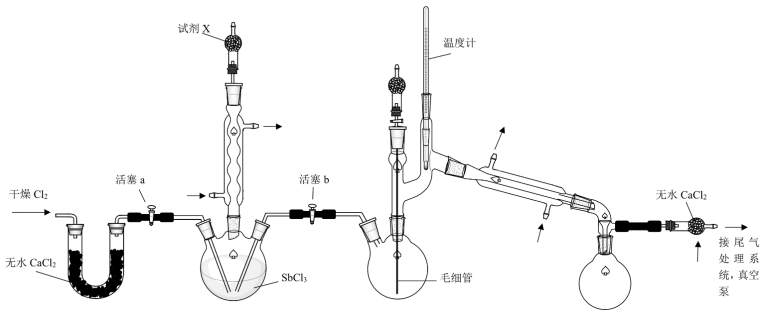
相关性质如表:
回答下列问题:
(1)实验装置中两个冷凝管___ (填“能”或“不能”)交换使用。
(2)试剂X的作用为___ 、___ 。
(3)反应完成后,关闭活塞a、打开活塞b,减压转移___ (填仪器名称)中生成的SbCl5至双口烧瓶中。用真空泵抽气减压蒸馏前,必须关闭的活塞是___ (填“a”或“b”);用减压蒸馏而不用常压蒸馏的主要原因是___ 。
(4)实验小组在由SbCl5制备HSbF6时,没有选择玻璃仪器,其原因为___ 。(写化学反应方程式)
(5)为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为___ 。
(6)实验小组在探究实验中发现蜡烛可以溶解于HSbF6中,同时放出氢气。已知烷烃分子中碳氢键的活性大小顺序为:甲基(—CH3)<亚甲基(—CH2—)<次甲基( )。写出2—甲基丙烷与HSbF6反应的离子方程式
)。写出2—甲基丙烷与HSbF6反应的离子方程式___ 。
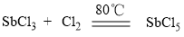 、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
相关性质如表:
| 物质 | 熔点 | 沸点 | 性质 |
| SbCl3 | 73.4℃ | 220.3℃ | 极易水解 |
| SbCl5 | 3.5℃ | 140℃分解79℃/2.9kPa | 极易水解 |
(1)实验装置中两个冷凝管
(2)试剂X的作用为
(3)反应完成后,关闭活塞a、打开活塞b,减压转移
(4)实验小组在由SbCl5制备HSbF6时,没有选择玻璃仪器,其原因为
(5)为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为
(6)实验小组在探究实验中发现蜡烛可以溶解于HSbF6中,同时放出氢气。已知烷烃分子中碳氢键的活性大小顺序为:甲基(—CH3)<亚甲基(—CH2—)<次甲基(
 )。写出2—甲基丙烷与HSbF6反应的离子方程式
)。写出2—甲基丙烷与HSbF6反应的离子方程式
您最近一年使用:0次
2021-10-09更新
|
8512次组卷
|
15卷引用:湖南省衡阳市衡阳县第一中学2021-2022学年高三下学期期中考试化学试题
湖南省衡阳市衡阳县第一中学2021-2022学年高三下学期期中考试化学试题2021年新高考湖北化学高考真题2021年湖北高考化学试题变式题11-19(已下线)回归教材重难点10 综合实验方案的设计与评价-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)押新高考卷16题 化学实验综合题-备战2022年高考化学临考题号押题(新高考通版)(已下线)2022年浙江省6月高考真题变式题26-31(已下线)专题17 化学实验综合题-三年(2020-2022)高考真题分项汇编(已下线)易错点31 化学实验常用仪器-备战2023年高考化学考试易错题(已下线)专题27 物质制备类综合性实验题(学生版)-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型179 气液、液液反应型制备实验(已下线)题型45 物质性质探究型综合实验(已下线)专题19 实验综合题(已下线)专题19 实验综合题福建省龙岩市连城县第一中学2023-2024学年高三上学期8月月考化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
3 . 为探究Na2SO3的性质,实验小组同学进行了如下实验:

| A.③和④中产生的气体成分完全相同 | B.②和⑥中沉淀的主要成分不同 |
| C.①→②和④→⑥均只发生了复分解反应 | D. 的还原性在酸性条件下增强 的还原性在酸性条件下增强 |
您最近一年使用:0次
2023-04-06更新
|
2589次组卷
|
11卷引用:北京市海淀区2022-2023学年高三下学期期中练习化学试题
北京市海淀区2022-2023学年高三下学期期中练习化学试题浙江省杭州第四中学2022-2023学年高一下学期期中考试化学试题(已下线)【2023】【高一下】【期中考】【杭四下沙】【高中化学】【罗梦宇收集】山东省东营市第一中学2023届高三下学期二模化学试题(已下线)题型35 微型成套装置实验流程(已下线)题型45 物质性质探究型综合实验山西省晋城一中2022-2023学年高一下学期第三次调研考试化学试题天津市滨海新区2023-2024学年塘沽第一中学高三上学期第二次月考化学试题(已下线)热点19 化学微型实验北京一零一中2023-2024学年高三上学期第一次月考(开学考)化学试卷 北京市顺义区第二中学2023-2024学年高三下学期开学测化学试题
名校
4 . 为探究物质的氧化性,某实验小组设计如图实验,在实验过程中,观察到氯化亚铁溶液变黄,四氯化碳溶液变为紫红色。下列说法错误的是(已知:碘单质易溶于四氯化碳,可得到紫红色溶液)


A.烧瓶中的反应为: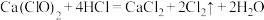 |
B.浸有 溶液的棉花起吸收尾气的作用 溶液的棉花起吸收尾气的作用 |
C. 可用淀粉溶液替换 可用淀粉溶液替换 |
D.试管下层出现紫红色,可证明氧化性: |
您最近一年使用:0次
2023-11-15更新
|
1006次组卷
|
7卷引用:辽宁省鞍山市第一中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
5 . 某研究性学习小组设计下列实验探究Zn和FeCl3溶液的反应,回答下列问题:
(1)由FeCl3固体配制未酸化的250mL0.5mol·L-1FeCl3溶液(pH=1.3),不需要使用的实验仪器有___________ (从下列图中选择,写出名称)。

(2)将Zn投入到未酸化的0.5mol·L-1FeCl3溶液(pH=1.3)中,在不同的实验条件下,实验现象如表:
①实验中产生的气体为___________ ,实验ii中产生气体的速率明显快于实验i,可能的原因是___________ (答出两点)。
②“滴加铁氰化钾溶液后,可见蓝色沉淀”说明混合溶液中存在Fe2+。生成Fe2+的离子方程式为___________ 。
(3)实验i和ii均先有气体生成,后有溶液颜色的变化。研究性学习小组猜想,可能是此实验条件下,氧化性:H+>Fe3+。
①为了检验上述猜想是否正确,查阅资料:可利用标准电极电势(用φθ表示)判断氧化性、还原性强弱,且电极电势越小,还原剂的还原性越强,已知(溶液中离子浓度的影响在此忽略不计):φθ(Fe3+ /Fe2+)=0.77 V,φθ (2H+ /H2)=0 V,φθ (Fe2+ /Fe)=—0.417 V,φθ (Zn2+ /Zn) =—0.76 V。则Fe3+、H+、Zn2+、Fe2+的氧化性大小关系为___________ 。
②研究小组进一步分析后,将锌粒改为锌粉,继续进行实验:
对比实验iii和iv,实验iv中“气泡不明显,红褐色褪色明显”的原因可能为___________ 。
③结合实验探究过程及现象分析,影响Zn与FeCl3溶液反应的条件有___________ (答两点即可的)。
(1)由FeCl3固体配制未酸化的250mL0.5mol·L-1FeCl3溶液(pH=1.3),不需要使用的实验仪器有

(2)将Zn投入到未酸化的0.5mol·L-1FeCl3溶液(pH=1.3)中,在不同的实验条件下,实验现象如表:
| 实验编号 | 条件 | 现象 |
| i | 锌粒18℃ | 刚开始无明显气泡,0.5min后有气体产生,一段时间后,溶液颜色加深。向反应后的溶液中滴加铁氰化钾溶液后,可见蓝色沉淀 |
| ii | 锌粒65℃ | 产生气泡较快,大约12 s后,气泡非常明显,溶液很快转为红棕色。较长时间后发现红棕色基本消失,最后产生红棕色沉淀 |
②“滴加铁氰化钾溶液后,可见蓝色沉淀”说明混合溶液中存在Fe2+。生成Fe2+的离子方程式为
(3)实验i和ii均先有气体生成,后有溶液颜色的变化。研究性学习小组猜想,可能是此实验条件下,氧化性:H+>Fe3+。
①为了检验上述猜想是否正确,查阅资料:可利用标准电极电势(用φθ表示)判断氧化性、还原性强弱,且电极电势越小,还原剂的还原性越强,已知(溶液中离子浓度的影响在此忽略不计):φθ(Fe3+ /Fe2+)=0.77 V,φθ (2H+ /H2)=0 V,φθ (Fe2+ /Fe)=—0.417 V,φθ (Zn2+ /Zn) =—0.76 V。则Fe3+、H+、Zn2+、Fe2+的氧化性大小关系为
②研究小组进一步分析后,将锌粒改为锌粉,继续进行实验:
| 实验编号 | 条件 | 现象 |
| iii | 锌粉18℃ 不振荡 | 大约3min可以看到明显的气泡,溶液颜色逐渐变深。向反应后的溶液中滴加铁氰化钾溶液后,可见蓝色沉淀 |
| iv | 锌粉65℃ 振荡 | 气泡不明显,红褐色褪色明显。向反应后的溶液中滴加铁氰化钾溶液后,可见蓝色沉淀 |
③结合实验探究过程及现象分析,影响Zn与FeCl3溶液反应的条件有
您最近一年使用:0次
2022-01-19更新
|
1229次组卷
|
5卷引用:福建省永安第九中学2022-2023学年高三上学期期中考试化学试题
福建省永安第九中学2022-2023学年高三上学期期中考试化学试题福建省漳州市2022届高三毕业班第一次质量检测化学试题(已下线)一轮巩固卷8-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)(已下线)易错点06 铁及其化合物-备战2023年高考化学考试易错题(已下线)专题六 金属元素及其化合物-实战高考·二轮复习核心突破
名校
6 . 用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )
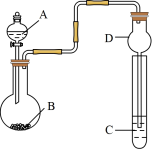
| A.若A为浓盐酸,B为Na2CO3,C中盛有Na2SiO3溶液,则C中溶液出现白色沉淀,证明酸性:H2CO3> H2SiO3 |
| B.若A为浓盐酸,B为KMnO4,C中盛石蕊试液,则C中溶液最终呈红色 |
| C.若A为较浓硫酸,B为Na2SO3固体,C中盛有Na2S溶液,则C中溶液变浑浊 |
| D.装置D起干燥气体作用 |
您最近一年使用:0次
2020-01-18更新
|
4070次组卷
|
16卷引用:广东省揭阳市揭西县河婆中学2020-2021学年高一下学期期中质量检测化学试题
广东省揭阳市揭西县河婆中学2020-2021学年高一下学期期中质量检测化学试题广东省汕头市金山中学2019-2020学年高一上学期期末考试化学试题【全国百强校】安徽省六安市第一中学2020届高三下学期自测(二)化学试题广东省珠海一中高一化学下学期综合测试试卷(已下线)小题必刷19 硫及其化合物——2021年高考化学一轮复习小题必刷(通用版)甘肃省兰州市第一中学2020-2021学年高一上学期期末考试化学(理)试题甘肃省嘉峪关市第一中学2021届高三上学期三模考试化学试题甘肃省天水市第一中学2021-2022高三上学期第三次考试化学试题辽宁省沈阳市第四十中学2021-2022年高一下学期4月份线上教学效果检测化学试题哈尔滨市第九中学校2021-2022学年高一下学期4月阶段性验收考试化学试题甘肃省靖远县第一中学2021-2022学年高一下学期4月月考化学试题新疆沙湾县第一中学2021-2022学年高一下学期期末考试化学试题河南省濮阳市元龙高级中学2021-2022学年高一下学期第二次质量检测化学试题湖南长沙麓山国际实验中学2022-2023学年高一上学期期末线上化学试题黑龙江省哈尔滨市第九中学校2021-2022学年高一下学期4月阶段性验收化学试题陕西省商洛市商州区高级中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
7 . I.某化学自主实验小组利用如图所示装置探究 能否被
能否被 还原
还原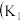 、
、 为止水夹,夹持固定装置略去)。
为止水夹,夹持固定装置略去)。________ 。 装置发生的化学反应方程式为
装置发生的化学反应方程式为_________ 。
(2)甲、乙分别是___________  填标号
填标号 。
。
a.硫酸、浓硫酸 b.碱石灰、无水氯化钙 c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)若 能够被
能够被 还原,写出发生反应的化学方程式:
还原,写出发生反应的化学方程式:___________ 。
(4)此实验装置存在一个明显的缺陷是___________ 。
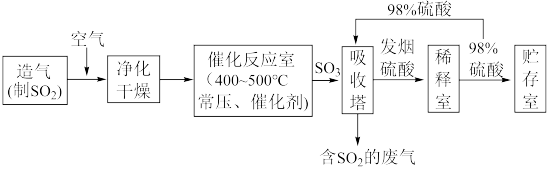
II.硫酸可用于生产化肥、农药、炸药、染料和盐类等。工业生产硫酸的流程图如下: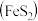 为原料来制备SO2,将黄铁矿粉碎的原因是:
为原料来制备SO2,将黄铁矿粉碎的原因是:___________ 。
(6)写出催化反应室中SO2被氧化为SO3的化学方程式___________ 。
(7)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,可用___________ 吸收。
 能否被
能否被 还原
还原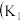 、
、 为止水夹,夹持固定装置略去)。
为止水夹,夹持固定装置略去)。
 装置发生的化学反应方程式为
装置发生的化学反应方程式为(2)甲、乙分别是
 填标号
填标号 。
。a.硫酸、浓硫酸 b.碱石灰、无水氯化钙 c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)若
 能够被
能够被 还原,写出发生反应的化学方程式:
还原,写出发生反应的化学方程式:(4)此实验装置存在一个明显的缺陷是
II.硫酸可用于生产化肥、农药、炸药、染料和盐类等。工业生产硫酸的流程图如下:
 为原料来制备SO2,将黄铁矿粉碎的原因是:
为原料来制备SO2,将黄铁矿粉碎的原因是:(6)写出催化反应室中SO2被氧化为SO3的化学方程式
(7)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,可用
您最近一年使用:0次
2024-02-24更新
|
769次组卷
|
5卷引用:河南省三门峡市渑池县第二高级中学2023-2024学年高一下学期4月期中考试化学试题
河南省三门峡市渑池县第二高级中学2023-2024学年高一下学期4月期中考试化学试题新疆克孜勒苏柯尔克孜自治州第二中学2022-2023学年高一下学期期末考试化学试题安徽省合肥市第一中学2023-2024学年高一下学期月考化学试题(一)广东省广州市黄广中学2023-2024学年高一下学期3月月考化学试题(已下线)期末押题卷01-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(天津专用)
8 . 草酸亚铁不溶于水,可用于制药工业。草酸亚铁晶体(FeC2O4·2H2O)呈淡黄色,可用作照相显影剂。某化学活动小组分别设计了相应装置进行实验。回答下列问题:
I.制备草酸亚铁晶体(装置如图所示):
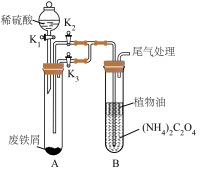
(1)盛放稀硫酸的仪器名称为___________ ;植物油的作用是___________ 。
(2)实验过程中,制备草酸亚铁的具体操作是___________ 。
(3)检验草酸亚铁晶体已洗净的操作方法为___________ 。
II.草酸亚铁晶体热分解产物的探究:
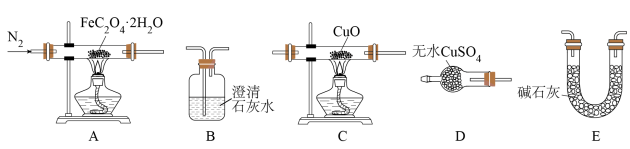
(4)按照气流从左到右的方向,上述装置的连接顺序为___________ →尾气处理装置(填图中字母,装置可重复使用)。
(5)实验结束后,C中黑色固体变为红色,B中澄清石灰水变浑浊,D中无水硫酸铜变为蓝色,A中残留FeO,则A处反应管中发生反应的化学方程式为___________ 。
III.运用热重分析法推测产物:
(6)称取54.0g草酸亚铁晶体(FeC2O4·2H2O)在隔绝空气的条件下加热,得到剩余固体质量随温度变化的曲线如图所示:
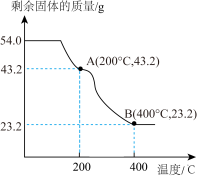
已知B点时,固体只含有一种铁的氧化物,根据上图可知B点固体物质的化学式为_______ 。
I.制备草酸亚铁晶体(装置如图所示):

(1)盛放稀硫酸的仪器名称为
(2)实验过程中,制备草酸亚铁的具体操作是
(3)检验草酸亚铁晶体已洗净的操作方法为
II.草酸亚铁晶体热分解产物的探究:

(4)按照气流从左到右的方向,上述装置的连接顺序为
(5)实验结束后,C中黑色固体变为红色,B中澄清石灰水变浑浊,D中无水硫酸铜变为蓝色,A中残留FeO,则A处反应管中发生反应的化学方程式为
III.运用热重分析法推测产物:
(6)称取54.0g草酸亚铁晶体(FeC2O4·2H2O)在隔绝空气的条件下加热,得到剩余固体质量随温度变化的曲线如图所示:

已知B点时,固体只含有一种铁的氧化物,根据上图可知B点固体物质的化学式为
您最近一年使用:0次
2023-11-14更新
|
831次组卷
|
4卷引用:河北省石家庄精英中学2023-2024学年高三上学期第二次调研(期中)考试化学试题
河北省石家庄精英中学2023-2024学年高三上学期第二次调研(期中)考试化学试题(已下线)实验探究题湖南省衡阳市衡阳县2023-2024学年高一上学期1月期末考试化学试题(已下线)T15-实验综合题
9 . 用图所示装置进行实验,探究硝酸与铁反应的产物。
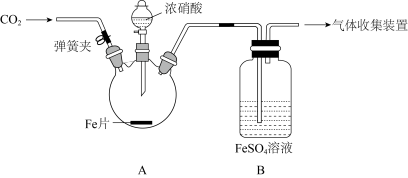
已知:FeSO4+NO=Fe(NO)SO4(棕色) ∆H<0 。
下列说法正确的是

| 主要实验操作 | 实验现象 |
| 打开弹簧夹,通入一段时间CO2后,滴入浓硝酸后无明显现象,加热烧瓶,反应开始后停止加热。 | ①A 中有红棕色气体产生,一段时间后,气体颜色逐渐变浅;反应停止后,A 中无固体剩余。 ②B 中溶液变棕色。 |
| 取少量A 中溶液,加几滴氯水,再滴入硫氰化钾溶液 | ③溶液变为红色 |
| 取少量 B 中溶液,加热 | ④B中棕色溶液变浅,有无色气体逸出,且在空气中变为红棕色 |
下列说法正确的是
| A.滴入浓硝酸加热前没有明显现象的原因是:温度低,反应速率太慢 |
| B.实验现象③说明反应后A 中溶液含有 Fe2+ |
| C.实验现象④说明 A 中有 NO 生成 |
D.可用浓 NaOH 溶液和湿润的红色石蕊试纸检验硝酸的还原产物中是否有 NH |
您最近一年使用:0次
2021-05-21更新
|
1908次组卷
|
8卷引用:辽宁省实验中学2021-2022学年高一下学期期中阶段测试化学试题
辽宁省实验中学2021-2022学年高一下学期期中阶段测试化学试题湖北省武汉市汉阳一中2021届高三下学期三模化学试题(已下线)第29讲 化学综合实验(精讲)-2022年一轮复习讲练测(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点12 氮及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题13 氮及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练 山西省长治市2022届高三上学期九月份质量监测化学试题(已下线)第四章 非金属及其化合物 第23练 硝酸 含氮化合物的转化关系
解题方法
10 . 下列关于氮及其化合物性质的探究,实验结论正确的是
| 选项 | 操作和现象 | 结论 |
| A | 将灼热的木炭伸入浓硝酸中,木炭燃烧,产生大量红棕色气体 | 木炭和硝酸发生反应生成了 和 和 |
| B | 向 悬浊液中加浓 悬浊液中加浓 溶液,沉淀溶解 溶液,沉淀溶解 | 主要原因是铵根水解显酸性、中和 促进反应 促进反应 |
| C | 向含有等物质的量 和 和 的混酸稀溶液加入过量铜粉,生成气体,溶液变蓝色 的混酸稀溶液加入过量铜粉,生成气体,溶液变蓝色 | 反应结束后溶液中的溶质是 和 和 |
| D | 将Al粉加入强碱性的 溶液,微热,产生气体使湿润红色石蕊试纸变蓝 溶液,微热,产生气体使湿润红色石蕊试纸变蓝 |  在强碱性溶液中无氧化性 在强碱性溶液中无氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



