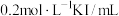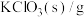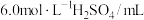回答下列问题:
(1)称取NaOH质量为
(2)在配制的过程中一定不需要使用到的仪器是
 填字母
填字母 ,还缺少的仪器有
,还缺少的仪器有A.烧杯 B.药匙 C.玻璃棒 D.托盘天平 E.锥形瓶 F.胶头滴管
(3)下列的实验操作可能导致配制的溶液浓度偏低的是
 填字母
填字母 。
。A.容量瓶内原来存有少量的水未进行干燥
B. 称量固体时,所用砝码已生锈
C. NaOH固体溶解后,未冷却至室温就开始进行转移
D. 定容时仰视视刻度线
E.定容时液面超过刻度线,用胶头滴管吸出
Ⅱ.某学习小组为探究CO2与过氧化钠反应时是否需要与水接触,设计了如下实验装置

步骤1:先打开K2,关闭K1,然后打开分液漏斗活塞加入盐酸,一段时间后,将带火星的木条放在a处。
步骤2:先打开K1,关闭K2,然后打开分液漏斗活塞加入盐酸,一段时间后,将带火星的木条放在a处。
(4)装置②是为了除去CO2中的HCl气体,所选试剂是
A.浓H2SO4 B.饱和Na2CO3溶液 C.饱和NaHCO3溶液
(5)从上述试剂中选择,装置③中的试剂是
(6)甲同学根据实验现象认为:CO2与过氧化钠反应时需要与水接触。据此推断他观察到的步骤1和步骤2的a处的实验现象分别是
(7)乙同学对此结论提出质疑,他认为:上述实验不足以证明“有水存在时,过氧化钠与CO2发生了化学反应”。用化学方程式表示乙同学的理由

回答下列问题:
(1)装置Ⅰ中发生反应的化学方程式为
 :
:①
 中
中 元素的化合价为
元素的化合价为②实验进行一段时间后,可观察到装置Ⅱ中的品红溶液褪色,其中
 属于
属于③仪器
 的名称为
的名称为④从其组成的阳离子来看,
 属于
属于(2)在装置Ⅳ和装置Ⅴ中:
①装置Ⅴ中发生反应的离子方程式为
②装置Ⅴ中可观察到的现象为
③实验进行一段时间后,可观察到装置Ⅳ中的品红溶液褪色,下列说法正确的是
A.起漂白作用的一定是

B.反应结束后,装置Ⅳ中溶液的
 小于7
小于7C.装置Ⅳ可能观察到
 生成速率的快慢
生成速率的快慢(3)装置Ⅲ中生成硫酸盐反应的化学方程式为
【查阅资料】
i.Cu(NH3)42+呈深蓝色,[Cu(NH3)4]2+
 Cu2++4NH3;受热易分解,放出氨气。
Cu2++4NH3;受热易分解,放出氨气。ii.Cu+在水溶液中不稳定,在溶液中只能以[Cu(NH3)2]+等络合离子的形式稳定存在;[Cu(NH3)2]+无色,易被氧气氧化为[Cu(NH3)4]2+。
【实验1】制备Cu(NH3)4SO4
向盛有2mL0.1mol•L-1CuSO4溶液的试管中滴加2mL1mol•L-1氨水,观察到溶液中立即出现浅蓝色沉淀;随后沉淀逐渐溶解,得到深蓝色溶液,经分离得到Cu(NH3)4SO4晶体。
(1)资料表明,向CuSO4溶液中滴加氨水,可能会生成浅蓝色Cu2(OH)2SO4沉淀。
①该小组同学取实验1中浅蓝色沉淀,洗涤后,
 。
。②补全实验1中生成Cu2(OH)2SO4沉淀的离子方程式:2Cu2++
 =Cu2(OH)2SO4↓+
=Cu2(OH)2SO4↓+(2)甲同学设计实验证明深蓝色溶液中含Cu(NH3)4SO4;加热深蓝色溶液并检验逸出气体为氨气。你认为此方案
【实验2】探究用Cu(NH3)4SO4和氨水的混合液浸取单质铜得到[Cu(NH3)2]2SO4的原理。
| 编号 | 实验装置及部分操作 | 烧杯中溶液 | 实验现象 |
| 2-1 | 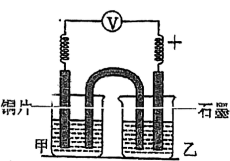 实验开始,先读取电压表示数,后迅速将其换成电流表,继续实验,10min内记录甲烧杯中的现象 | 甲:0.05mol•L-1Na2SO4 乙:0.05mol•L-1Cu(NH3)4SO4 | 电压表指针迅速偏转至0.1V;甲中溶液无明显变化 |
| 2-2 | 甲:0.05mol•L-1Na2SO4 乙:0.05mol•L-1CuSO4 | 电压表指针迅速偏转至0.3V;甲中溶液无明显变化 | |
| 2-3 | 甲:0.1mol•L-1Na2SO4与1mol•L-1氨水等体积混合 乙:溶液A | 电压表指针迅速偏转至0.35V;甲中溶液无明显变化 | |
| 2-4 | 甲:0.1mol•L-1Na2SO4与1mol•L-1氨水等体积混合 乙:0.05mol•L-1CuSO4 | 电压表指针迅速偏转至0.65V;几分钟后,甲烧杯中溶液逐渐由无色变蓝色 |
(3)溶液A为
(4)对比实验2-1和2-2,可以得到的结论是
(5)实验2~4中,甲烧杯中溶液由无色变为蓝色的原因是
(6)结合上述实验分析,用Cu(NH3)4SO4和氨水的混合液浸取单质铜的过程中,Cu(NH3)4SO4和氨水的作用分别是:
 和NaClO,并探究其性质。
和NaClO,并探究其性质。实验一、制备
 和NaClO
和NaClO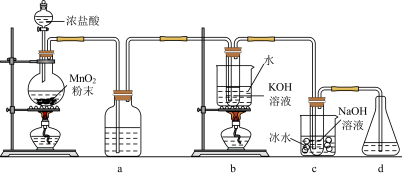
(1)盛装浓盐酸的仪器名称
 的产率会
的产率会(2)b中发生反应的化学方程式是
实验二、探究NaClO的性质。
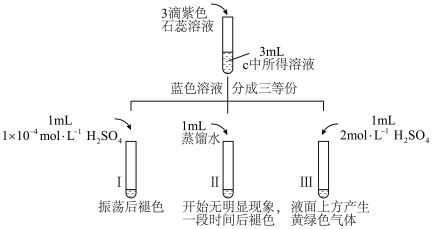
(3)①Ⅰ中溶液短时间褪色的原因是
②Ⅲ中产生黄绿色气体的原因是
实验三、氯酸钾与碘化钾反应的研究
(4)在不同条件下
 可将KI氧化为
可将KI氧化为 或
或 。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录如下(实验在室温下进行):
。该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录如下(实验在室温下进行):试管编号 | 1 | 2 | 3 | 4 |
| 1.0 | 1.0 | 1.0 | 1.0 |
| 0.10 | 0.10 | 0.10 | 0.10 |
| 0 | 3.0 | 6.0 | 9.0 |
蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
实验现象 |
②设计1号试管实验的作用是
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为
5 . 已知反应: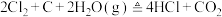 。某实验小组用高锰酸钾与浓盐酸反应制取氯气,并验证已知反应产物中的
。某实验小组用高锰酸钾与浓盐酸反应制取氯气,并验证已知反应产物中的 ,装置连接如下:
,装置连接如下:
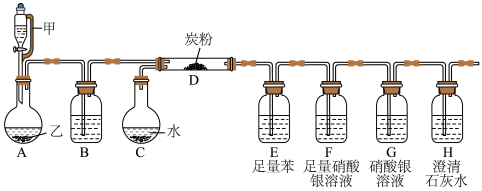
已知:氯气易溶于苯中。
回答下列问题:
(1)装置
 中仪器甲的名称是
中仪器甲的名称是(2)装置
 中的试剂是
中的试剂是(3)设计装置
 的目的是
的目的是 的作用是
的作用是(4)判断产物中含有
 的实验现象是
的实验现象是(5)用双线桥表示该反应电子转移的方向和数目:
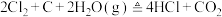
 与水的反应,实验如下(实验中加入的溶液均过量):
与水的反应,实验如下(实验中加入的溶液均过量):
已知:i.
 是二元弱酸,能电离出
是二元弱酸,能电离出 和
和
ii.②中发生反应:
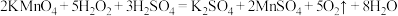
iii.
 可以溶解在稀
可以溶解在稀 中
中下列说法中不正确的是
A.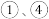 中均只发生了氧化还原反应 中均只发生了氧化还原反应 |
B.白色沉淀的主要成分是 |
C.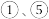 中产生的气体能使带火星的木条复燃 中产生的气体能使带火星的木条复燃 |
D.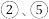 中 中 与 与 的作用不相同,产生气体的量也不同 的作用不相同,产生气体的量也不同 |
7 . 硫酸铜主要用作纺织品媒染剂、农业杀虫剂等,其晶体(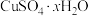 )在不同温度下会逐步失去结晶水甚至分解。周南化学社对硫酸铜晶体受热分解的产物成分进行探究,请回答下列问题:
)在不同温度下会逐步失去结晶水甚至分解。周南化学社对硫酸铜晶体受热分解的产物成分进行探究,请回答下列问题:
Ⅰ.探究硫酸铜晶体的分解产物
为探究硫酸铜晶体的分解产物,某同学设计了如下实验:
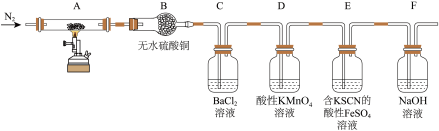
观察到的实验现象有: 中有固体残留;
中有固体残留; 中无水硫酸铜变蓝;
中无水硫酸铜变蓝; 中产生白色沉淀;
中产生白色沉淀; 中溶液颜色变浅、无沉淀产生;
中溶液颜色变浅、无沉淀产生; 中溶液变为红色。
中溶液变为红色。
(1)装有无水硫酸铜的仪器名称为
(2)
 中产生的沉淀的化学式为
中产生的沉淀的化学式为 中现象证明硫酸铜晶体的分解产物中含有
中现象证明硫酸铜晶体的分解产物中含有(3)
 中
中 发生反应的离子方程式为
发生反应的离子方程式为(4)为探究
 中残留固体的成分(假设硫酸铜已完全分解),某同学查阅资料:铜有
中残留固体的成分(假设硫酸铜已完全分解),某同学查阅资料:铜有 、
、 价,且分解产物中不含0价的铜。
价,且分解产物中不含0价的铜。 在酸性条件下不稳定,发生反应:
在酸性条件下不稳定,发生反应: 。验证
。验证 中固体产物中是否有
中固体产物中是否有 的实验方案为
的实验方案为Ⅱ.测定硫酸铜晶体中结晶水含量
实验步骤:
①称取 硫酸铜晶体,用适量蒸馏水溶解,再滴加几滴盐酸酸化。
硫酸铜晶体,用适量蒸馏水溶解,再滴加几滴盐酸酸化。
②向①所得溶液中滴加足量 溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为
溶液,得到白色沉淀,将所得沉淀过滤、洗涤、干燥,称得其质量为 。
。
(5)步骤②中检验沉淀是否洗涤干净的方法是:
(6)根据实验数据,硫酸铜晶体(
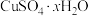 )中
)中
 、
、 的代数式表示)。
的代数式表示)。
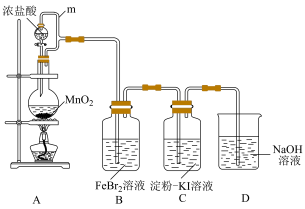
8 . 某化学活动小组利用如下装置制备氯气并进行相关的性质验证。
已知:
① 易溶于有机溶剂四氯化碳(
易溶于有机溶剂四氯化碳( ),且所得溶液呈橙红色;
),且所得溶液呈橙红色;
② 不溶于水,密度比水大。
不溶于水,密度比水大。
(1)装置A中发生反应的化学方程式为
(2)m的作用是
(3)装置C中的现象是
(4)装置D中发生反应的离子方程式为
(5)取少量反应后的B中溶液,向其中加入
 ,振荡后静置,若出现
,振荡后静置,若出现 被氧化。
被氧化。(6)另取少量反应后的B中溶液于试管中,向其中加入少量
 被氧化。
被氧化。(7)已知氧化性
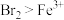 ,向200mL 0.1mol/L
,向200mL 0.1mol/L  溶液中通入标准状况下0.56L
溶液中通入标准状况下0.56L  时反应的离子方程式为
时反应的离子方程式为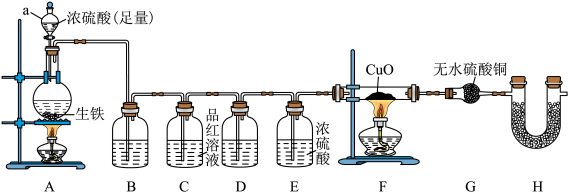
(1)仪器a的名称为
(2)为验证并吸收SO2装置B中加入的试剂为
(3)装置D的作用为
(4)若装置F和G亦有明显的现象,解释其原因
(5)待生铁(反应前为m g)完全溶解后,停止加热, 拆下装置D(装置中试剂足量并吸收完全)并称重。若装置D增重bg且装置C无明显变化,则生铁中铁的质量分数为
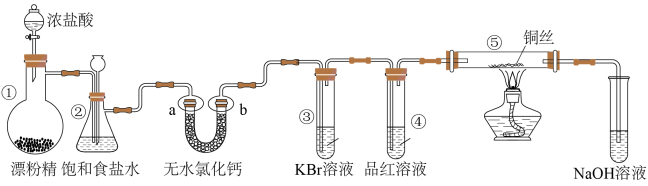
| A.用MnO2代替装置中的漂粉精也可以达到实验目的 |
| B.a、b处分别放干燥和湿润的有色布条,无法说明干燥的Cl2不具有漂白性 |
| C.反应开始后可观察到③中溶液变黄,④中溶液褪色,说明氯水具有氧化性和漂白性 |
| D.反应开始后点燃酒精灯,可在⑤号硬质玻璃管中观察到棕黄色烟 |