解题方法
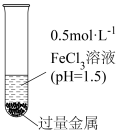
1 . 以 溶液为实验对象,研究物质之间反应的复杂多样性。实验如下:
溶液为实验对象,研究物质之间反应的复杂多样性。实验如下:
如表格,金属与 溶液反应
溶液反应
(1)配制 溶液,需要
溶液,需要 将固体先溶于浓盐酸,再稀释至指定浓度,原因是
将固体先溶于浓盐酸,再稀释至指定浓度,原因是___________ 。
(2)根据实验ⅰ中的现象,推测红褐色液体为胶体,通过___________ 可以快速判断其是否为胶体。
(3) 溶液与Cu反应的离子方程式为
溶液与Cu反应的离子方程式为___________ ,实验ⅰ和ⅱ均先有气体生成,后有溶液颜色的变化,甲同学认为产生该现象的原因可能是此实验条件下氧化性: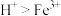 ,乙同学认为可以根据ⅲ判断氧化性:
,乙同学认为可以根据ⅲ判断氧化性: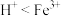 ,理由是
,理由是__________ 。
 溶液为实验对象,研究物质之间反应的复杂多样性。实验如下:
溶液为实验对象,研究物质之间反应的复杂多样性。实验如下:| 装置 | 序号 | 金属 | 现象及产物检验 |
| ⅰ | 镁条 | 立即产生大量气体,溶液颜色变红棕色; 片刻后气泡减少,金属表面产生红褐色沉淀。 |
| ⅱ | 锌粒 | 开始时无明显气泡,半分钟后有气体产生,溶液颜色慢慢加深;一段时间后,金属表面产生红棕色沉淀 | |
| ⅲ | 铜粉 | 无气体产生,溶液逐渐变为蓝绿色 |
 溶液反应
溶液反应(1)配制
 溶液,需要
溶液,需要 将固体先溶于浓盐酸,再稀释至指定浓度,原因是
将固体先溶于浓盐酸,再稀释至指定浓度,原因是(2)根据实验ⅰ中的现象,推测红褐色液体为胶体,通过
(3)
 溶液与Cu反应的离子方程式为
溶液与Cu反应的离子方程式为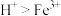 ,乙同学认为可以根据ⅲ判断氧化性:
,乙同学认为可以根据ⅲ判断氧化性: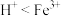 ,理由是
,理由是
您最近一年使用:0次
名校
2 . 二氧化氯(ClO2)具有强氧化性,是优良的饮用水消毒剂。ClO2常温下为黄绿色气体,熔点-59℃,沸点11℃,极易溶于水且不与水反应,浓的ClO2受热时易爆炸。我国广泛使用的方法是用干燥的Cl2与NaClO2固体反应制取ClO2,实验室模拟制备ClO2装置如图所示:
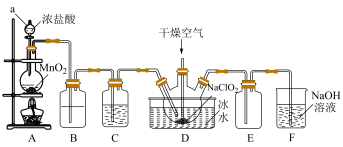
(1)仪器a的名称是:___________ ,装置A中反应的离子方程式为:___________ 。
(2)装置B中盛装的试剂是___________ ,装置C中试剂的作用是:___________ 。
(3)为防止ClO2制备装置发生爆炸,实验中采取的措施:①将装置置于冰水浴中降温,②___________ 。
(4)装置E为ClO2的收集装置,应将其置于___________ 水浴中(填“热”或“冰”)。
(5)装置F为氯气的尾气吸收装置,小组同学用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的NaOH溶液中,当滴到一定量时,红色突然褪去,小组同学对褪色原因提出假设:
假设1:___________ 。
假设2:可能是氯水中存在HClO具有强氧化性,漂白褪色。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许褪色后的溶液于试管中,滴加足量的NaOH溶液,若___________ (填“实验现象”),则假设1成立。

(1)仪器a的名称是:
(2)装置B中盛装的试剂是
(3)为防止ClO2制备装置发生爆炸,实验中采取的措施:①将装置置于冰水浴中降温,②
(4)装置E为ClO2的收集装置,应将其置于
(5)装置F为氯气的尾气吸收装置,小组同学用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的NaOH溶液中,当滴到一定量时,红色突然褪去,小组同学对褪色原因提出假设:
假设1:
假设2:可能是氯水中存在HClO具有强氧化性,漂白褪色。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许褪色后的溶液于试管中,滴加足量的NaOH溶液,若
您最近一年使用:0次
2023-11-06更新
|
649次组卷
|
2卷引用:宁夏银川市第二中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
3 . 学习小组在实验室中利用下图所示装置制备SO2并进行相关性质的探究。回答下列问题:
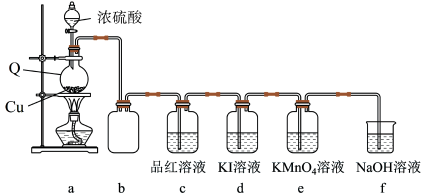
(1)仪器Q的名称为___________ ;装置 中品红溶液褪色,可证明SO2具有
中品红溶液褪色,可证明SO2具有___________ 性,装置b的作用是___________ 。
(2)向分液漏斗中滴加浓硫酸之前,需先通入一段时间N2,此操作的目的是___________ 。
(3)装置a中反应的化学方程式为___________ 。
(4)探究:探究SO2在KI溶液体系中的反应产物
实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应:SO2+4I-+4H+=S↓+2I2+2H2O。但有同学提出上述反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO +2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
Ⅰ.取适量装置d中浊液,向其中滴加几滴___________ ,振荡,无明显变化,浊液中无I2。
a.高锰酸钾溶液 b.淀粉溶液 c.氢氧化钠溶液
Ⅱ.将装置d中浊液进行分离,得淡黄色固体和澄清溶液;取适量分离后的澄清溶液于试管中,___________ ,出现白色沉淀,产物溶液中存在SO 。
。
综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为___________ 。

(1)仪器Q的名称为
 中品红溶液褪色,可证明SO2具有
中品红溶液褪色,可证明SO2具有(2)向分液漏斗中滴加浓硫酸之前,需先通入一段时间N2,此操作的目的是
(3)装置a中反应的化学方程式为
(4)探究:探究SO2在KI溶液体系中的反应产物
实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在反应:SO2+4I-+4H+=S↓+2I2+2H2O。但有同学提出上述反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO
 +2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。Ⅰ.取适量装置d中浊液,向其中滴加几滴
a.高锰酸钾溶液 b.淀粉溶液 c.氢氧化钠溶液
Ⅱ.将装置d中浊液进行分离,得淡黄色固体和澄清溶液;取适量分离后的澄清溶液于试管中,
 。
。综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为
您最近一年使用:0次
名校
解题方法
4 . 下图是实验室制备氯气并进行一系列相关实验的部分装置(夹持设备已略)。
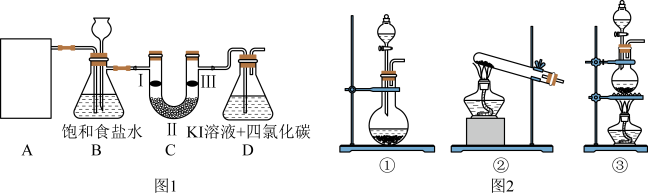
(1)实验室可以用 与浓盐酸反应制备氯气,发生反应的化学方程式为
与浓盐酸反应制备氯气,发生反应的化学方程式为_______ 。该实验中,A部分的发生装置可选图2中的_______ (填序号)。
(2)装置B中饱和食盐水的作用是_______ ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,写出发生堵塞时B中的现象_______ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,则C中I、Ⅱ、Ⅲ应依次放入_______ (填字母)。
(4)设计装置D的目的是比较氯、碘单质的氧化性。当向D中缓缓通入一定量氯气时,观察到D中_______ ,即可证明 氧化性大于
氧化性大于 。
。
(5)该实验装置存在明显的缺陷,应进行的改进措施是_______ (用离子方程式表示)。

(1)实验室可以用
 与浓盐酸反应制备氯气,发生反应的化学方程式为
与浓盐酸反应制备氯气,发生反应的化学方程式为(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,则C中I、Ⅱ、Ⅲ应依次放入
| 选项 | a | b | c | d |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 浓硫酸 | 碱石灰 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
 氧化性大于
氧化性大于 。
。(5)该实验装置存在明显的缺陷,应进行的改进措施是
您最近一年使用:0次
2023-07-31更新
|
331次组卷
|
3卷引用:宁夏回族自治区银川市宁夏育才中学2023-2024学年高一上学期1月期末考试化学试题
宁夏回族自治区银川市宁夏育才中学2023-2024学年高一上学期1月期末考试化学试题陕西省汉中市2020-2021学年高一上学期期末考试化学试题(已下线)期末测试卷02-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
5 . 莫尔盐是硫酸盐的一种复盐,是一种重要的化学试剂,有如图所示的反应;它的水溶液中加入KSCN不显红色,溶液C中加入KSCN显红色。
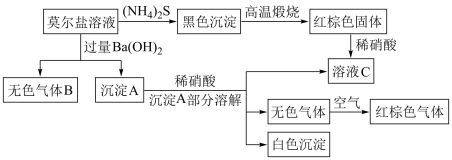
根据以上关系,按要求填空:
(1)写出沉淀A中的成分的化学式___________ 和___________ 。
(2)莫尔盐存在的阳离子为___________ 和___________ 。
(3)部分沉淀A与稀 反应的离子方程式是
反应的离子方程式是___________ 。
(4)古代硫酸的制法是隔绝空气煅烧绿矾( ),将蒸气冷却可制得一种无色黏稠的液体“绿矾油”,剩余的固体为红棕色。(已知
),将蒸气冷却可制得一种无色黏稠的液体“绿矾油”,剩余的固体为红棕色。(已知 的熔点是16.8℃,沸点是44.8℃,在加热条件下
的熔点是16.8℃,沸点是44.8℃,在加热条件下 具有比较强的氧化性)现某小组同学欲利用下图所示装置探究绿矾受热分解的产物。
具有比较强的氧化性)现某小组同学欲利用下图所示装置探究绿矾受热分解的产物。
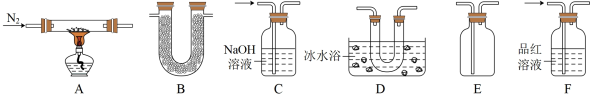
①装置的连接顺序为A→B→___________ →E→___________ →C
②B的作用是验证该反应有水生成,其中的试剂为___________ ,实验过程中发现F中溶液褪色,证明有___________ 气体生成,硬质玻璃管中剩余的固体是___________ 。

根据以上关系,按要求填空:
(1)写出沉淀A中的成分的化学式
(2)莫尔盐存在的阳离子为
(3)部分沉淀A与稀
 反应的离子方程式是
反应的离子方程式是(4)古代硫酸的制法是隔绝空气煅烧绿矾(
 ),将蒸气冷却可制得一种无色黏稠的液体“绿矾油”,剩余的固体为红棕色。(已知
),将蒸气冷却可制得一种无色黏稠的液体“绿矾油”,剩余的固体为红棕色。(已知 的熔点是16.8℃,沸点是44.8℃,在加热条件下
的熔点是16.8℃,沸点是44.8℃,在加热条件下 具有比较强的氧化性)现某小组同学欲利用下图所示装置探究绿矾受热分解的产物。
具有比较强的氧化性)现某小组同学欲利用下图所示装置探究绿矾受热分解的产物。
①装置的连接顺序为A→B→
②B的作用是验证该反应有水生成,其中的试剂为
您最近一年使用:0次
名校
6 . 某课外小组在实验室制备氨气,并进行有关氮气的性质探究。
(1)该小组同学加热生石灰与氯化铵的混合物制取并收集干燥的氨气。

①应该选用的仪器及装置有(填字母)___________ 。
②生石灰与氯化铵反应生成氨气的化学方程式为___________ 。
(2)该小组同学设计如图所示装置探究氨气的还原性。
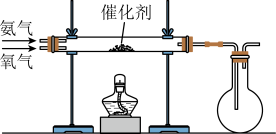
将催化剂加热至红热,撤去酒精灯,可观察到催化剂继续保持红热,有红棕色气体产生及少量白烟生成,在上述过程会同时发生多个反应,根据现象判断氨气的催化氧化为___________ (放热或吸热)反应,白烟的化学式为___________ 。
(3)该小组同学以氨气和二氧化碳为原料制备碳酸氢铵。
①甲同学先将二氧化碳通入水中,充分溶解后,再通入氨气;乙同学先将氨气通入水中,充分溶解后,再通入二氧化碳。合适的方案是___________ (填“甲”或“乙”);
②检验产物中有 的方法为
的方法为___________ 。
(1)该小组同学加热生石灰与氯化铵的混合物制取并收集干燥的氨气。

①应该选用的仪器及装置有(填字母)
②生石灰与氯化铵反应生成氨气的化学方程式为
(2)该小组同学设计如图所示装置探究氨气的还原性。

将催化剂加热至红热,撤去酒精灯,可观察到催化剂继续保持红热,有红棕色气体产生及少量白烟生成,在上述过程会同时发生多个反应,根据现象判断氨气的催化氧化为
(3)该小组同学以氨气和二氧化碳为原料制备碳酸氢铵。
①甲同学先将二氧化碳通入水中,充分溶解后,再通入氨气;乙同学先将氨气通入水中,充分溶解后,再通入二氧化碳。合适的方案是
②检验产物中有
 的方法为
的方法为
您最近一年使用:0次
名校
解题方法
7 . 硫酸亚铁(FeSO4)加热至高温会分解,生成一种金属氧化物和两种非金属氧化物。
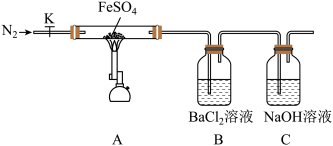
组装好仪器(已省略夹持仪器),在一定温度下按上述图示装置进行实验。
(1)组装好实验装置后,要进行的下一步操作是_____ ;实验开始时通入氮气的目的是_____ 。
(2)B中实验现象证明分解产物中含有_____ (写化学式)。依据实验2硬质玻璃管中加热冷却后的固体性质确定分解产物有_____ (写化学式)。
(3)某同学欲通过下列实验验证分解产物中含有的另一种非金属氧化物。

①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A→_____ 。
②能证明生成了另一种非金属氧化物的现象是_____ 。该现象体现了该物质的_____ 性。写出该条件下硫酸亚铁受热分解的化学方程式_____ 。
(4)硫酸亚铁溶液在保存时需要加入少量铁粉,原因是:_____ (用离子方程式表示)。

组装好仪器(已省略夹持仪器),在一定温度下按上述图示装置进行实验。
| 序号 | 操作步骤 | 实验现象 |
| 1 | 打开K,通入一段时间的N2,关闭活塞K,加热A中的玻璃管一段时间 | B中产生大量白色沉淀 |
| 2 | A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却 | 硬质玻璃管中最终可以看到红棕色固体物质 |
(2)B中实验现象证明分解产物中含有
(3)某同学欲通过下列实验验证分解产物中含有的另一种非金属氧化物。

①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A→
②能证明生成了另一种非金属氧化物的现象是
(4)硫酸亚铁溶液在保存时需要加入少量铁粉,原因是:
您最近一年使用:0次
8 . 实验室用下图装置(夹持装置已略去)制备NH3,并探究其性质。其中a、b为湿润的红色石蕊试纸。
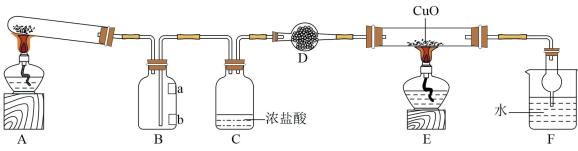
回答下面问题:
(1)写出装置A中发生反应的化学方程式:_______ 。
(2)装置B的作用是探究氨气和空气密度的相对大小,首先变色的试纸是_______ 。
(3)装置C中出现的现象是_______ 。
(4)装置D中盛放的固体药品是_______ (填名称)。
(5)装置E中黑色的CuO最后变为紫红色的Cu单质,装置F中有气泡冒出,经检验是N2。该现象证明氨气具有_______ (选填“氧化性”、“还原性”)。
(6)装置F中干燥管的作用是_______ 。

回答下面问题:
(1)写出装置A中发生反应的化学方程式:
(2)装置B的作用是探究氨气和空气密度的相对大小,首先变色的试纸是
(3)装置C中出现的现象是
(4)装置D中盛放的固体药品是
(5)装置E中黑色的CuO最后变为紫红色的Cu单质,装置F中有气泡冒出,经检验是N2。该现象证明氨气具有
(6)装置F中干燥管的作用是
您最近一年使用:0次
9 . 实验室用如图装置制备无水FeCl3。

已知:FeCl3固体易升华,易吸收水分而潮解变质。请回答下列问题:
(1)连接好仪器后首先应进行的操作是_______ ;A装置中连接分液漏斗与烧瓶之间的导管的作用是_______ 。
(2)请写出A装置中反应的离子方程式_______ 。
(3)实验室还可用KMnO4和浓盐酸反应制取氯气:2KMnO4+l6HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,在上述反应中,生成56LCl2(标准状况下),转移电子的个数为_______ 。
(4)写出工业制取漂白粉的化学方程式_______ 。
(5)装置B中长颈漏斗可以检验后续装置是否堵塞,其中饱和食盐水的作用是_______ ,D装置与E装置之间用弧形粗弯管连接而不是普通的直角玻璃导管,其目的是_______ 。
(6)F中所装试剂为_______ ,有学生提出:装置F和G二者可以简约用一个球形干燥管来代替,为了达到相同的作用,球形干燥管内盛放的试剂是_______ 。

已知:FeCl3固体易升华,易吸收水分而潮解变质。请回答下列问题:
(1)连接好仪器后首先应进行的操作是
(2)请写出A装置中反应的离子方程式
(3)实验室还可用KMnO4和浓盐酸反应制取氯气:2KMnO4+l6HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,在上述反应中,生成56LCl2(标准状况下),转移电子的个数为
(4)写出工业制取漂白粉的化学方程式
(5)装置B中长颈漏斗可以检验后续装置是否堵塞,其中饱和食盐水的作用是
(6)F中所装试剂为
您最近一年使用:0次
10 . 学习小组在实验室中利用如图所示装置制备SO2并进行相关性质的探究。
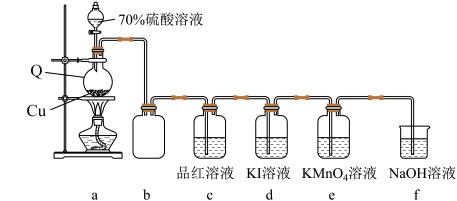
回答下列问题:
(1)实验用70%的硫酸而不用浓硫酸的原因是___________________________________ ;装置b的作用是________________
(2)装置e中出现_________ (填现象)可证明SO2具有还原性,反应离子方程式为_________________
(3)实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:SO2+4I-+4H+ S↓+2I2+2H2O。
S↓+2I2+2H2O。
探究:SO2在KI溶液体系中的反应产物
有同学提出上述可逆反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO +2I-+4H+。
+2I-+4H+。
为进一步探究体系中的产物,完成下列实验方案。
综上可知,SO2在KI溶液中发生了歧化反应,其反应的离子方程式为:______________________

回答下列问题:
(1)实验用70%的硫酸而不用浓硫酸的原因是
(2)装置e中出现
(3)实验开始后,发现装置d中的溶液迅速变黄,继续通入SO2,装置d中出现乳黄色浑浊。该小组同学查阅资料得知,存在可逆反应:SO2+4I-+4H+
 S↓+2I2+2H2O。
S↓+2I2+2H2O。探究:SO2在KI溶液体系中的反应产物
有同学提出上述可逆反应生成的I2可与SO2发生反应:SO2+I2+2H2O=SO
 +2I-+4H+。
+2I-+4H+。为进一步探究体系中的产物,完成下列实验方案。
方案 | 操作 | 预期现象 | 结论 |
ⅰ | 取适量装置d中浊液,向其中滴加几滴① | 无明显变化 | 浊液中无I2 |
ⅱ | 将装置d中浊液进行分离 | 得淡黄色固体和澄清溶液 | |
| 取适量分离后的澄清溶液于试管中, ② | ③ | ④ |
您最近一年使用:0次