解题方法
1 . 下图是元素①~⑤在元素周期表中的位置。
(1)⑤在周期表中的位置是第_______ 周期第_______ 族,其最高价氧化物对应的水化物与②的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(2)③的一种核素的中子数是9,表示该核素的符号是_______ 。
(3)非金属性:④_______ ⑤(填“>”或“<”),从原子结构角度解释其原因:_______ 。
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程_______ 。
(5)下列关于①的说法正确的是_______ (填字母)。
a.原子结构示意图为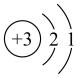
b.其单质可以和水反应生成
c.在同主族的元素中,①的金属性最强
(6)为研究②单质(X)的性质,进行如下实验:
下列说法中,正确的是_______(填字母)。
| ① | ③ | ④ | |||||
| ② | ⑤ | ||||||
(1)⑤在周期表中的位置是第
(2)③的一种核素的中子数是9,表示该核素的符号是
(3)非金属性:④
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程
(5)下列关于①的说法正确的是
a.原子结构示意图为

b.其单质可以和水反应生成

c.在同主族的元素中,①的金属性最强
(6)为研究②单质(X)的性质,进行如下实验:
| 实验 | ||
| 装置 | 液体a | 现象 |
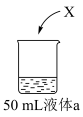 | 蒸馏水 | Ⅰ.X浮在液面上,剧烈反应,产生少量白雾 |
 盐酸 盐酸 | Ⅱ.X浮在液面上,反应比Ⅰ中剧烈,产生白雾 | |
| 浓盐酸 | Ⅲ.X浮在液面上,反应比Ⅰ中缓慢,产生大量白雾,烧杯底部有白色固体 | |
| A.Ⅰ中现象说明X与水反应放热 |
B.Ⅱ中反应的离子方程式为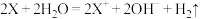 |
| C.Ⅲ中白雾比Ⅱ中多,说明Ⅲ中反应放热比Ⅱ中更多 |
D.推测Ⅲ中反应缓慢可能与 以及生成的白色固体有关 以及生成的白色固体有关 |
您最近一年使用:0次
2 . 某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计了如下装置进行实验。

请按要求回答下列问题:
(1)盛装浓盐酸仪器的名称为_______ ,圆底烧瓶中发生反应的离子方程式为_______
(2)KI溶液中观察到的现象是_______ ,反应的化学方程式为_______ 。
(3)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放的是_______ (填名称)。
(4)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84”消毒液(主要成分是NaClO)而发生氯气中毒事件。请写出两者发生反应的离子方程式:_______ 。
(5)该兴趣小组用 与足量的浓盐酸制备氯气,则理论上产生的气体在标况下的体积为
与足量的浓盐酸制备氯气,则理论上产生的气体在标况下的体积为_______ L。

请按要求回答下列问题:
(1)盛装浓盐酸仪器的名称为
(2)KI溶液中观察到的现象是
(3)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放的是
(4)曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84”消毒液(主要成分是NaClO)而发生氯气中毒事件。请写出两者发生反应的离子方程式:
(5)该兴趣小组用
 与足量的浓盐酸制备氯气,则理论上产生的气体在标况下的体积为
与足量的浓盐酸制备氯气,则理论上产生的气体在标况下的体积为
您最近一年使用:0次
3 . 为验证过氧化钠可在呼吸面具和潜水艇中用作供氧剂,某同学设计了如下实验装置:
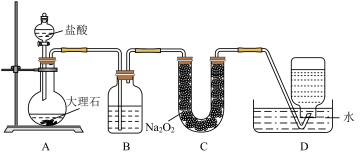
回答下列问题:
(1)装置A中发生反应的离子方程式是_______ 。
(2)B中盛放的试剂是_______ ,目的是为了_______ 。
(3)写出 与
与 反应的化学反应方程式
反应的化学反应方程式_______ 。
(4)有同学认为D中收集到的氧气可能混有 ,于是对该套装置作了改进,具体操作可以是
,于是对该套装置作了改进,具体操作可以是_______ 。
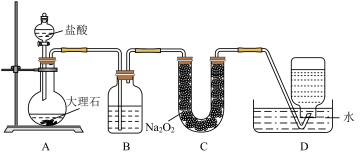
回答下列问题:
(1)装置A中发生反应的离子方程式是
(2)B中盛放的试剂是
(3)写出
 与
与 反应的化学反应方程式
反应的化学反应方程式(4)有同学认为D中收集到的氧气可能混有
 ,于是对该套装置作了改进,具体操作可以是
,于是对该套装置作了改进,具体操作可以是
您最近一年使用:0次
4 .  与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐。某兴趣小组利用如图装置以
与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐。某兴趣小组利用如图装置以 分别与KOH溶液和NaOH溶液反应为原理,制备
分别与KOH溶液和NaOH溶液反应为原理,制备 和NaClO,并探究
和NaClO,并探究 和NaClO的部分性质。
和NaClO的部分性质。
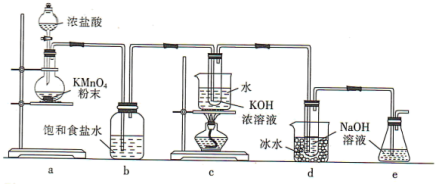
回答下列问题:
(1)a装置所用玻璃仪器的名称为______ (任意写一种);发生反应的离子方程式为____________ 。
(2)b装置的作用是____________ ;e装置的作用是____________ 。
(3)已知:c装置中得到的是 ,d装置中得到的是NaClO。
,d装置中得到的是NaClO。
①由此判断氯气与碱反应时,影响产物的因素有____________ 。
②NaClO溶液常温时稳定,受热时会生成两种盐,NaBrO溶液在0℃时稳定,常温时会生成两种盐,则常温时, 与KOH溶液反应的离子方程式为
与KOH溶液反应的离子方程式为____________ 。
(4)取少量c、d装置中生成的 和NaClO溶液(两溶液均调至碱性),分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液。1号试管溶液颜色不变;2号试管溶液颜色变为棕色,加入
和NaClO溶液(两溶液均调至碱性),分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液。1号试管溶液颜色不变;2号试管溶液颜色变为棕色,加入 ,振荡、静置后
,振荡、静置后 层显
层显_______ 色。由此可推知,在碱性条件下, 的氧化能力
的氧化能力______ (填“>”或“<”)NaClO的氧化能力。
(5)该兴趣小组在40℃条件下,将一定量的 通入600 mL
通入600 mL  NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和
NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为______ mol。
 与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐。某兴趣小组利用如图装置以
与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐。某兴趣小组利用如图装置以 分别与KOH溶液和NaOH溶液反应为原理,制备
分别与KOH溶液和NaOH溶液反应为原理,制备 和NaClO,并探究
和NaClO,并探究 和NaClO的部分性质。
和NaClO的部分性质。
回答下列问题:
(1)a装置所用玻璃仪器的名称为
(2)b装置的作用是
(3)已知:c装置中得到的是
 ,d装置中得到的是NaClO。
,d装置中得到的是NaClO。①由此判断氯气与碱反应时,影响产物的因素有
②NaClO溶液常温时稳定,受热时会生成两种盐,NaBrO溶液在0℃时稳定,常温时会生成两种盐,则常温时,
 与KOH溶液反应的离子方程式为
与KOH溶液反应的离子方程式为(4)取少量c、d装置中生成的
 和NaClO溶液(两溶液均调至碱性),分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液。1号试管溶液颜色不变;2号试管溶液颜色变为棕色,加入
和NaClO溶液(两溶液均调至碱性),分别置于1号和2号试管中,向两试管中分别滴加等量且适量的KI溶液。1号试管溶液颜色不变;2号试管溶液颜色变为棕色,加入 ,振荡、静置后
,振荡、静置后 层显
层显 的氧化能力
的氧化能力(5)该兴趣小组在40℃条件下,将一定量的
 通入600 mL
通入600 mL  NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和
NaOH溶液中,NaOH恰好反应完全,得到的产物中含有NaCl、NaClO和 ,则参加反应的
,则参加反应的 的物质的量为
的物质的量为
您最近一年使用:0次
2022-07-12更新
|
113次组卷
|
2卷引用:贵州省黔西南布依族苗族自治州2021-2022学年高二下学期期末质量检测化学试题
5 . 某校化学兴趣小组为研究氯气的性质,设计用如图所示的装置进行实验,其中a为干燥的红色试纸,b为湿润的红色试纸。

回答下列问题:
(1)装置I中仪器c的名称是______ ,实验室用二氧化锰和浓盐酸制备氯气的化学方程式为_______ 。
(2)装置V的作用是_______ 。
(3)若产生的 足量,实验过程中装置IV中的实验现象是
足量,实验过程中装置IV中的实验现象是________ 。
(4)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“装置II中a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置I与II之间添加下图中的装置________ (填序号)。

(5)有一种“地康法”制取氯气的反应原理如图所示:

在450℃条件下,反应II的化学方程式为_________ 。

回答下列问题:
(1)装置I中仪器c的名称是
(2)装置V的作用是
(3)若产生的
 足量,实验过程中装置IV中的实验现象是
足量,实验过程中装置IV中的实验现象是(4)实验结束后,该组同学在装置III中观察到b的红色褪去,但是并未观察到“装置II中a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置I与II之间添加下图中的装置

(5)有一种“地康法”制取氯气的反应原理如图所示:

在450℃条件下,反应II的化学方程式为
您最近一年使用:0次
解题方法
6 . 某化学兴趣小组为了探究铜与稀硝酸反应产生的气体主要是NO而设计了下列实验,装置如图所示(部分装置已略去)。图中K为止水夹,M是半空的注射器。请回答有关问题:

(1)装置A的目的是利用生成的 将整个装内的空气排尽。避免空气的干扰,装置A中所发生反应的离子方程式为
将整个装内的空气排尽。避免空气的干扰,装置A中所发生反应的离子方程式为_______ ;当装置内空气已经排尽时。可观察到的现象是_______ 。
(2)B装置中稀硝酸发生反应主要表现出的化学性质有_______ 。
(3)为实现装置C的作用,应采用的操作和观察到的现象为_______ 。
(4)将28.8g铜与140mL一定浓度的硝酸反应,铜完全溶解。产生的NO和 混合气体在标准状况下的体积为11.2L,其中NO的体积为
混合气体在标准状况下的体积为11.2L,其中NO的体积为_______ L。

(1)装置A的目的是利用生成的
 将整个装内的空气排尽。避免空气的干扰,装置A中所发生反应的离子方程式为
将整个装内的空气排尽。避免空气的干扰,装置A中所发生反应的离子方程式为(2)B装置中稀硝酸发生反应主要表现出的化学性质有
(3)为实现装置C的作用,应采用的操作和观察到的现象为
(4)将28.8g铜与140mL一定浓度的硝酸反应,铜完全溶解。产生的NO和
 混合气体在标准状况下的体积为11.2L,其中NO的体积为
混合气体在标准状况下的体积为11.2L,其中NO的体积为
您最近一年使用:0次
7 . 草酸亚铁晶体( FeC2O4·2H2O)是一种淡黄色粉末,可用作照相显影剂。某课外小组利用如下实验装置对草酸亚铁晶体分解产物进行探究,并设计实验测定草酸亚铁晶体样品纯度。
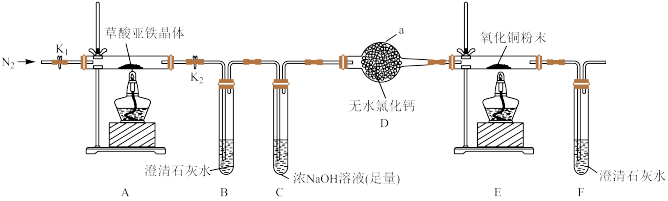
回答下列问题:
(1)仪器a的名称为_____ ;装置B中澄清石灰水变浑浊,说明气体分解产物中含有_____ ;
(2)实验前先通一段时间N2目的是________ ;装置C中浓NaOH溶液的作用是______ ;
(3)证明草酸亚铁晶体分解产物中含有CO的实验现象是______ ;
(4)充分反应后,将装置A硬质玻璃管中的残留固体溶于足量的稀硫酸中,无气泡产生,滴加几滴KSCN溶液,溶液不变红,说明固体分解产物是______ (填化学式);根据上述实验现象写出草酸亚铁晶体分解的化学方程式_______ ;
(5)所给实验装置存在明显的设计缺陷,该缺陷是______ ;
(6)草酸亚铁晶体样品纯度的测定:准确称取12. 000 g某草酸亚铁晶体样品,在一定条件下溶于稍过量的硫酸中,配成250 mL溶液。取25.00 mL上述溶液,用0.100 mol/L KMnO4标准溶液滴定,达到滴定终点时, 消耗35.00 mL KMnO4标准溶液,滴定反应为:FeC2O4·2H2O + KMnO4+ H2SO4→Fe2(SO4)3+CO2↑+ MnSO4 + K2SO4 + H2O(未配平)。则该草酸亚铁晶体样品的纯度为________ (已知该草酸亚铁晶体样品中不含其他与高锰酸钾反应的还原性杂质)。

回答下列问题:
(1)仪器a的名称为
(2)实验前先通一段时间N2目的是
(3)证明草酸亚铁晶体分解产物中含有CO的实验现象是
(4)充分反应后,将装置A硬质玻璃管中的残留固体溶于足量的稀硫酸中,无气泡产生,滴加几滴KSCN溶液,溶液不变红,说明固体分解产物是
(5)所给实验装置存在明显的设计缺陷,该缺陷是
(6)草酸亚铁晶体样品纯度的测定:准确称取12. 000 g某草酸亚铁晶体样品,在一定条件下溶于稍过量的硫酸中,配成250 mL溶液。取25.00 mL上述溶液,用0.100 mol/L KMnO4标准溶液滴定,达到滴定终点时, 消耗35.00 mL KMnO4标准溶液,滴定反应为:FeC2O4·2H2O + KMnO4+ H2SO4→Fe2(SO4)3+CO2↑+ MnSO4 + K2SO4 + H2O(未配平)。则该草酸亚铁晶体样品的纯度为
您最近一年使用:0次
解题方法
8 . 氯化亚铜(CuCl) 为白色粉末,其露置于空气中易被氧化为绿色的碱式氯化铜Cu2(OH)3Cl]。某兴趣小组高温加热分解氯化铜晶体(CuCl2·xH 2O)制备CuCl,其装置如下(加热仪器、夹持仪器省略)

回答下列问题:
(1)装有无水硫酸铜的仪器名称为______ ,装置 D 的作用是______ 。
(2)通入 HCl 气体的主要作用是______ 。
(3)实验过程中,装置C 中的现象为______ 。
(4)硬质玻璃管A 中发生主要反应的化学方程式为__________ 。
(5)为测定 CuCl2·xH 2O 中结晶水的数目 x,实验步骤如下:
a 用电子天平称取一定质量的氯化铜晶体;
b 在坩埚中充分灼烧;
c 在干燥器中冷却;
d 称量所得黑色固体质量;
e 重复 b~d 操作直至连续两次称量差值不超过 0.001g。
①若氯化铜晶体质量为 3.384g,最终得到黑色固体质量为 1.600g,则 x=______ (精确到 0.1)。
②若加热时有固体溅出坩埚,则测得x 值______ 填“偏大”“不变”或“偏小”)。

回答下列问题:
(1)装有无水硫酸铜的仪器名称为
(2)通入 HCl 气体的主要作用是
(3)实验过程中,装置C 中的现象为
(4)硬质玻璃管A 中发生主要反应的化学方程式为
(5)为测定 CuCl2·xH 2O 中结晶水的数目 x,实验步骤如下:
a 用电子天平称取一定质量的氯化铜晶体;
b 在坩埚中充分灼烧;
c 在干燥器中冷却;
d 称量所得黑色固体质量;
e 重复 b~d 操作直至连续两次称量差值不超过 0.001g。
①若氯化铜晶体质量为 3.384g,最终得到黑色固体质量为 1.600g,则 x=
②若加热时有固体溅出坩埚,则测得x 值
您最近一年使用:0次
2020-05-25更新
|
132次组卷
|
3卷引用:贵州省黔西南州兴义市义龙新区2021-2022高三上学期期末考试化学试题
9 . 实验是学习化学的基础,某课外兴趣小组在学了苯与液溴的反应以后,对该反应的类型提出了猜想。
(1)甲组认为苯与液溴的反应是加成反应,乙组则认为苯与液溴的反应是___ ,对此问题你认为该怎样去证明,说出你的方法:___ 。
为了证明他们的猜想是否正确,按照如图的实验装置(夹持装置省略)进行实验。
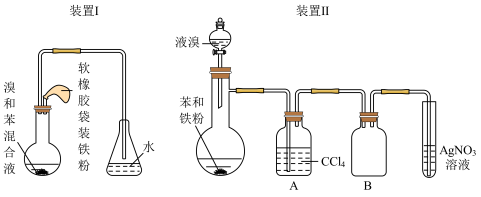
(2)比较装置Ⅰ和装置Ⅱ,选择___ (装置Ⅰ或装置Ⅱ),装置Ⅱ的A中CCl4溶液的作用是___ 。
(3)装有苯和铁粉的仪器名称是___ ,B集气瓶的作用是___ ,若试管中出现___ 现象乙组猜想正确。
(4)写出铁与液溴反应的化学方程式___ ,苯和液溴反应的化学方程式___ 。
(5)简要叙述除去溴苯中溴的方法:___ 。
(1)甲组认为苯与液溴的反应是加成反应,乙组则认为苯与液溴的反应是
为了证明他们的猜想是否正确,按照如图的实验装置(夹持装置省略)进行实验。
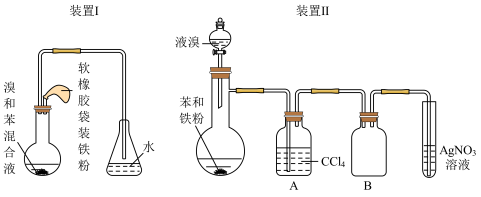
(2)比较装置Ⅰ和装置Ⅱ,选择
(3)装有苯和铁粉的仪器名称是
(4)写出铁与液溴反应的化学方程式
(5)简要叙述除去溴苯中溴的方法:
您最近一年使用:0次
名校
解题方法
10 . 研究金属与硝酸的反应,实验如下。
(1)Ⅰ中的无色气体是_________ 。
(2)Ⅱ中生成H2的离子方程式是______________ 。
(3)研究Ⅱ中的氧化剂
①甲同学认为该浓度的硝酸中H+的氧化性大于 ,所以
,所以 没有发生反应。乙同学依据Ⅰ和Ⅱ证明了甲的说法不正确,其实验证据是
没有发生反应。乙同学依据Ⅰ和Ⅱ证明了甲的说法不正确,其实验证据是____________ 。
②乙同学通过分析,推测出 也能被还原,依据是
也能被还原,依据是_____________ ,进而他通过实验证实该溶液中含有 ,其实验操作是
,其实验操作是____________ 。
(4)根据实验,金属与硝酸反应时,影响硝酸还原产物不同的因素有__________ ;试推测还可能有哪些因素影响_________ (列举1条)。
| 实验(20°C) | 现象 |
| Ⅰ.过量铜粉、2mL0.5mol/L HNO3 | 无色气体(遇空气变红棕色),溶液变为蓝色 |
| Ⅱ.过量铁粉、2mL0.5mol/ HNO3 | 6mL无色气体(经检测为H2),溶液几乎无色 |
(2)Ⅱ中生成H2的离子方程式是
(3)研究Ⅱ中的氧化剂
①甲同学认为该浓度的硝酸中H+的氧化性大于
 ,所以
,所以 没有发生反应。乙同学依据Ⅰ和Ⅱ证明了甲的说法不正确,其实验证据是
没有发生反应。乙同学依据Ⅰ和Ⅱ证明了甲的说法不正确,其实验证据是②乙同学通过分析,推测出
 也能被还原,依据是
也能被还原,依据是 ,其实验操作是
,其实验操作是(4)根据实验,金属与硝酸反应时,影响硝酸还原产物不同的因素有
您最近一年使用:0次
2020-02-15更新
|
223次组卷
|
6卷引用:贵州省黔南布依族苗族自治州瓮安第二中学2019-2020学年高一上学期期末考试化学试题



